Óxido de sodio
| Óxido de sodio | ||
|---|---|---|
 | ||
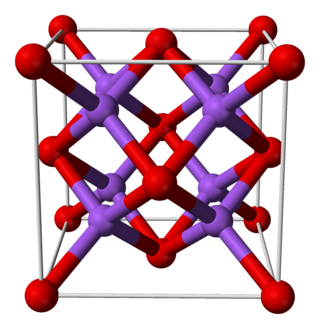 | ||
| Nombre IUPAC | ||
| Óxido de sodio | ||
| General | ||
| Fórmula semidesarrollada | Na2O | |
| Fórmula molecular | ? | |
| Identificadores | ||
| Número CAS | 1313-59-3[1] | |
| ChemSpider | 66599 | |
| PubChem | 73971 | |
| UNII | 3075U8R23D | |
| Propiedades físicas | ||
| Apariencia | Blanco | |
| Masa molar | 61,9789 g/mol | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
El óxido de sodio es un compuesto químico cuya fórmula es Na2O. Se utiliza en la fabricación de cerámicas y vidrios, aunque no en bruto. En presencia de agua reacciona formando hidróxido de sodio.
- Na2O + H2O → 2 NaOH
Preparación
El óxido de sodio se produce por la reacción del sodio con el hidróxido de sodio, peróxido de sodio o nitrito de sodio[2] iónico- 2N+1[:O:]-1
- 2 NaOH + 2 Na → 2 Na2O + H2
- Na2O2 + 2 Na → 2 Na2O
- 2 NaNO2 + 6 Na → 4 Na2O + N2
La mayoría de estas reacciones dependen de la reducción de algo por sodio, sea este hidróxido, peróxido o nitrito. La combustión del sodio en aire puede producir Na2O y aproximadamente 20% peróxido de sodio Na2O2.
6 Na + 2 O2 → 2 Na2O + Na2O2
Usos

Fabricación de vidrio
El óxido de sodio (Na2O) es un componente importante en cristales y vidrios el cual es añadido en forma de "soda" (carbonato sódico). El óxido de sodio no se encuentra explícitamente como tal en los cristales modernos, ya que los mismos son polímeros complejos interconectados. El cristal generalmente contiene un 15% de óxido de sodio, 70% de silicio (dióxido de silicio) y un 9% de cal (óxido cálcico). El carbonato de sodio "soda" sirve como fundente que permite disminuir la temperatura a la cual se funde el silicio. El cristal de soda funde a una temperatura menor que el silicio puro y posee una elasticidad algo mayor. Estos cambios se deben a que el dióxido de silicio y la soda reaccionan formando silicatos de sodio con la siguiente fórmula general: Na2[SiO2]x[SiO3].
- Na2CO3 → Na2O + CO2
- Na2O + SiO2 → Na2SiO3
Referencias
- ↑ Número CAS
- ↑ Greenwood, N. N.; & Earnshaw, A. (1997). Chemistry of the Elements (2nd Edn.), Oxford:Butterworth-Heinemann. ISBN 0-7506-3365-4.
Enlaces externos