Embarazo ectópico
| Embarazo ectópico | ||
|---|---|---|
 Ectópico, ilustración de Regnier de Graaf | ||
| Especialidad |
matronería ginecología | |
| Síntomas | Dolor abdominal, hemorragia vaginal. | |
| Factores de riesgo | Enfermedad pélvica inflamatoria, tabaquismo, cirugía tubárica previa, historia de infertilidad, uso de técnicas de reproducción asistida, embarazos con DIU[1] | |
Un embarazo ectópico (del gr. ἐκ, "fuera", y τόπος, "lugar") es una complicación del embarazo en la que el óvulo fertilizado o blastocito se desarrolla en los tejidos distintos de la pared uterina,[2] ya sea en la trompa de Falopio (lo más frecuente), en el ovario, en el canal cervical, en la cavidad pélvica o en la abdominal. Cuando el embarazo ocurre en el endometrio del útero se le conoce como embarazo eutópico.[3] El embarazo ectópico se produce por un trastorno en la fisiología de la reproducción humana que lleva a la muerte fetal,[4][5] y es la principal causa de morbilidad fetal y materna en el primer trimestre con 2 o 3 semanas del embarazo.[6]
El feto produce las enzimas que le permiten implantarse en diversos tipos de tejidos y, por tanto, un embrión implantado en otras partes del útero puede causar grandes daños a los tejidos en sus esfuerzos por alcanzar un suministro suficiente de sangre. Un embarazo ectópico es una emergencia médica y, si no se trata adecuadamente, puede poner en peligro la vida de la mujer.[5]
En los últimos años, la exactitud del diagnóstico del embarazo ectópico se ha incrementado notablemente por la mejoría de la sensibilidad de la determinación de la fracción beta de la hormona gonadotropina coriónica (β-hCG) y por la introducción de la ecografía transvaginal que permiten un diagnóstico precoz.[7]
Aproximadamente la mitad de los embarazos ectópicos se resuelven sin tratamiento. Estos son los llamados abortos tubáricos. El advenimiento del metotrexato para el tratamiento de un embarazo ectópico ha reducido la necesidad de cirugía, pero una intervención quirúrgica sigue siendo necesaria en los casos en que la trompa de Falopio se ha roto o está en peligro de hacerlo. Esta intervención puede ser laparoscópica o mediante una incisión más grande, conocida como laparotomía.[4]
Historia

El embarazo ectópico fue descrito por primera vez en el siglo XI, y hasta mediados del siglo XVIII era una patología generalmente fatal. John Bard informó la primera intervención quirúrgica exitosa para el tratamiento de un embarazo ectópico en la ciudad de Nueva York en 1759. La tasa de supervivencia a principios del siglo XIX era muy baja. Un informe demostró que, de un total de 30 pacientes, solo 5 sobrevivieron a la operación abdominal. Curiosamente, la tasa de supervivencia en los pacientes que se dejaron sin tratamiento fue de 1 de cada 3 casos.[5]
Epidemiología
Según estudios,[8] el 1,6 por ciento de los embarazos es ectópico, y de éstos, el 98 por ciento se producen en las trompas de Falopio. Por motivos no demasiado claros, cada vez resultan más frecuentes.[3] Son factores de riesgo: infecciones abdominales previas (enfermedad pélvica inflamatoria), una enfermedad en la trompa de Falopio, un embarazo ectópico previo, ser portadora de DIU, la exposición fetal al dietilestilbestrol o una ligadura de trompas fallida (un procedimiento de esterilización en el que se corta u obstruye la trompa de Falopio), la endometriosis. En los raros casos en que una mujer queda embarazada con un dispositivo intrauterino (DIU) colocado, el riesgo de tener un embarazo ectópico es elevado.
Cuando ocurren, los embarazos ectópicos suelen desarrollarse en una de las trompas de Falopio (embarazo tubárico). Son infrecuentes los embarazos en el canal cervical, en el ovario o en la cavidad abdominal o pélvica. Un embarazo ectópico constituye un riesgo para la vida, por lo que debe ser interrumpido lo antes posible. Según algunas estadísticas, 1 de cada 826 mujeres con embarazos ectópicos muere por complicaciones. En España se estima que el embarazo ectópico constituye aproximadamente el 2,3 por ciento del número total de embarazos.[3]
Etiología

Hay una serie de factores que predisponen a los embarazos ectópicos. A pesar de ello, en una tercera parte o hasta la mitad de los embarazos ectópicos no se identifican factores de riesgo predisponentes.[9] En teoría, cualquier cosa que dificulte la migración del embrión hacia la cavidad endometrial podría predisponer a las mujeres a la gestación ectópica.
La superficie interna de las trompas de Falopio está revestida de cilios vellosos que llevan el huevo fertilizado al útero. Los daños a la cilios o la obstrucción de las trompas de Falopio pueden dar lugar a un embarazo ectópico.
Enfermedad pélvica inflamatoria
Las mujeres con enfermedad pélvica inflamatoria (EPI) tienen una alta incidencia de embarazos ectópicos.[7] La causa más frecuente es el antecedente de infección causada por Chlamydia trachomatis. Los pacientes con infección por clamidias tienen una gama de presentaciones clínicas, desde una cervicitis asintomática hasta una salpingitis florida y una enfermedad inflamatoria pélvica. Esto genera una acumulación de tejido cicatrizal en las trompas de Falopio, lo que causa daños a los cilios. Sin embargo, si los dos tubos se ven ocluidos por la EPI, el embarazo no se produce, y esto representaría una protección contra un embarazo ectópico. La cirugía de trompas por tubos dañados puede quitar esta protección y aumentar el riesgo de la aparición de un embarazo ectópico.
Más del 50 por ciento de las mujeres que han sido infectadas no se enteran de que tuvieron la exposición. Otros organismos causantes de EPI, como la Neisseria gonorrhoeae, aumentan el riesgo de embarazo ectópico. Una historia de salpingitis aumenta el riesgo de embarazo ectópico unas cuatro veces.[9] La incidencia de daño tubárico aumenta después de los episodios sucesivos de EPI, es decir, un 13 por ciento después de 1 episodio, 35 por ciento después de dos episodios y 75 por ciento después de tres episodios.[5]
Antecedentes quirúrgicos
La cirugía tubárica, como la ligadura de trompas, puede predisponer a un embarazo ectópico.[7] Setenta por ciento de los embarazos después de un cauterio tubárico son ectópicos, mientras que el 70 por ciento de los embarazos después de pinzar las trompas resultan intrauterino. Las mujeres que se han sometido a una cirugía de recanalización tubárica con el fin de volver a quedar embarazadas también tienen un mayor riesgo de embarazo ectópico.[4] Este riesgo es mayor si se emplearon métodos más destructivos para la ligadura de trompas, como el cauterio de trompas o la eliminación parcial de los tubos. La explicación parece estar fundamentada en la formación de fístulas que permiten el paso de espermatozoides.
Antecedentes ectópicos
Una historia de embarazo ectópico aumenta el riesgo de futuros casos de aproximadamente el 7-10 por ciento.[9] Este riesgo no se reduce por la eliminación de los tubos afectados, aunque el otro tubo parece normal. El mejor método para el diagnóstico de la presente es hacer una ecografía. En general, una paciente con previo embarazo ectópico tiene una probabilidad entre 50-80 por ciento de tener un subsecuente embarazo intrauterino, y un 10-25 por ciento de probabilidad de un futuro embarazo tubárico.
Antecedentes etarios
Las pacientes están en mayor riesgo de embarazo ectópico con la edad avanzada. La mayor tasa de embarazos ectópicos se produce en las mujeres de 35-44 años, quienes tienen un riesgo 3-4 veces mayor de desarrollar un embarazo ectópico, en comparación con las mujeres de 15-24 años.[9] Una explicación propuesta implica la actividad eléctrica muscular en la trompa de Falopio, que es responsable de la motilidad tubárica. El envejecimiento puede generar una pérdida progresiva de la actividad mioeléctrica a lo largo de la trompa de Falopio.
Tabaquismo

Se ha señalado que el tabaquismo está asociado con riesgo de embarazo ectópico.[10] Algunos estudios han demostrado alto riesgo, 1.6-3.5 veces mayor en las pacientes fumadoras.[2] En este caso también se ha sugerido un efecto dosis-respuesta, es decir, que el riesgo de embarazo ectópico incrementa paulatinamente con el número de cigarros fumados al día.[2] Basado en estudios de laboratorio en seres humanos y animales, los investigadores han postulado varios mecanismos por los cuales el tabaquismo podría jugar un papel en los embarazos ectópicos. Estos mecanismos incluyen una o más de las siguientes: retraso en la ovulación, alteración de la motilidad uterina y las trompas o alteración en la inmunidad. Hasta la fecha, ningún estudio ha prestado apoyo a un mecanismo específico por el que el tabaquismo afecta a la ocurrencia de un embarazo ectópico.
Otros factores de riesgo
Algunos autores afirman que las duchas vaginales aumentan los embarazos ectópicos, una hipótesis que es aún especulativa. Las mujeres expuestas a dietilestilbestrol (DES) en el útero tienen también un elevado riesgo de embarazo ectópico, hasta tres veces el riesgo de las mujeres no expuestas. Ocasionalmente, se observa que existe un cuerpo amarillo en el lado contralateral del sitio de implantación, lo que hace suponer que son casos de migración demasiado larga para alcanzar el útero.[3]
Algunos embarazos ectópicos pueden deberse a:[4]
- Defectos congénitos en las trompas de Falopio
- Complicaciones de una apendicitis
- Endometriosis
- Complicaciones de una salpingitis
- Tabaquismo. En comparación con las mujeres que no fuman, las fumadoras que se embarazan tienen el doble de probabilidades de sufrir este trastorno, ya que la nicotina de los cigarrillos paraliza los cilios del revestimiento de la trompa de Falopio.
También el inicio de las relaciones sexuales antes de los 18 años eleva discretamente el riesgo, probablemente condicionados en parte por la enfermedad pélvica inflamatoria.[7]
Patogenia

El ovario libera un óvulo que es succionado por una de las trompas de Falopio, donde es impulsado por diminutos cilios similares a pelos hasta que, varios días después, llega al útero. Normalmente, la fecundación del óvulo se efectúa en la trompa de Falopio, pero la implantación tiene lugar en el útero. Sin embargo, si la trompa se obstruye (por ejemplo, debido a una infección previa) o si hay daño en la motilidad tubárica, el óvulo puede desplazarse lentamente o incluso quedar atascado.[2] El óvulo fecundado quizá nunca llegue al útero y, en consecuencia, se produce un embarazo ectópico.
En un típico de un embarazo ectópico, el embrión no llega al útero, pero, en cambio, se adhiere a la mucosa de la trompa de Falopio. El embrión implantado se encaja activamente en el revestimiento de trompas. Más comúnmente invade vasos sanguíneos y causa sangrado. Este sangrado intratubal suele expulsar a la implantación fuera de las trompas en la forma de un aborto espontáneo. Algunas mujeres tienden a pensar que están teniendo un aborto involuntario cuando realmente tienen un aborto tubárico. No suele haber inflamación de la trompa en un embarazo ectópico. El dolor es causado por las prostaglandinas liberadas en el sitio de implantación, y por la sangre en la cavidad peritoneal, por ser un irritante local. A veces, el sangrado puede ser suficientemente fuerte para amenazar a la salud o incluso la vida de la mujer. Por lo general, este grado de hemorragia es debido a la demora en el diagnóstico, pero a veces, especialmente si la implantación es en la porción proximal de la trompa, es decir, justo antes de que entre en el útero, puede invadir la arteria vecina, y provocar sangrado antes de lo habitual.
Cuadro clínico
La clásica tríada clínica de embarazo ectópico incluye: dolor, amenorrea y sangrado vaginal. Los síntomas se pueden presentar desde las primeras semanas de embarazo. Normalmente, el dolor suele ser abdominal, lo cual puede parecer un común dolor de estómago o cólicos. La diferencia es que el dolor es muy fuerte y se localiza en la parte baja del abdomen. También es posible sentir dolor al orinar o al hacer un movimiento brusco. Lamentablemente, solo el 50 por ciento de las pacientes presentan signos clásicos. Las pacientes pueden presentar otros síntomas comunes a los embarazos precoces: náuseas, sensación de plenitud, fatiga, dolor abdominal bajo, cólicos fuertes, dolor en el hombro y dispareunia reciente.

Una forma de confirmar el embarazo es con una prueba de ultrasonido; habitualmente puede verse el saco gestacional desde la cuarta semana. Si no se encuentra saco gestacional en el útero, pero se padecen los síntomas mencionados, es probable que sea un embarazo ectópico.
El dolor abdominal es el síntoma más común, el cual se presenta generalmente en las fosas ilíacas e hipogastrio, pero puede afectar cualquier parte del abdomen y asociarse con dolor en el hombro por irritación diafragmática. Le sigue la amenorrea con algún grado de sangrado vaginal.
Sin embargo, solo el 40-50 por ciento de las pacientes con un embarazo ectópico presentan sangrado vaginal, el 50 por ciento tienen una masa palpable de anexos, y el 75 por ciento pueden tener dolor abdominal.[5] Aproximadamente el 20 por ciento de las pacientes con embarazos ectópicos están hemodinámicamente comprometidas en la presentación inicial, que es altamente sugestiva de rotura. Afortunadamente, con el uso de las técnicas modernas de diagnóstico, la mayor parte de los embarazos ectópicos pueden ser diagnosticados antes de la ruptura.
Muchos trastornos pueden tener una presentación similar a un embarazo extrauterino. Los más comunes son la apendicitis, la salpingitis, la ruptura de un quiste del cuerpo lúteo o folículo ovárico, un aborto espontáneo o la amenaza de aborto, la torsión de ovario y una infección urinaria.
Diagnóstico
Al inicio de un embarazo intrauterino normal, algunas mujeres suelen presentar signos y síntomas similares a los encontrados en pacientes con embarazos ectópicos u otros problemas ginecológicos o gastrointestinales. La disponibilidad de diversas herramientas bioquímicas, ecográficas y modalidades quirúrgicas pueden ayudar al proveedor de salud a ofrecer un diagnóstico definitivo y la distinción de condiciones.
Con el fin de reducir la morbilidad y la mortalidad asociadas con el embarazo ectópico, hay que tratarlo antes de que el embarazo curse las ocho semanas, ya que es en este tiempo cuando ocurre la ruptura del tubo uterino (trompa de Falopio) y produce sangrado, que es interno, y puede llevar a la paciente a un choque hipovolémico. Por lo tanto, ante la posible sospecha, se vigila a partir de la quinta semana, haciendo sonografía abdominal. Se puede hacer también una sonografía vaginal a la tercera o cuarta semana de gestación.
Ni los factores de riesgo ni el cuadro clínico de un embarazo ectópico son lo suficientemente sensibles o específicos para establecer un diagnóstico definitivo. Por lo tanto, cualquier paciente en edad reproductiva debe ser estudiada si presenta dolor abdominal, cólicos o sangrado vaginal durante su embarazo.
Estudios de laboratorio
En los últimos años se han desarrollado pruebas para la subunidad beta de la gonadotropina coriónica humana (β-hCG) en el plasma sanguíneo y en la orina para detectar un embarazo antes de desaparecer el primer ciclo menstrual. Si bien algunos paquetes comerciales de análisis de orina pueden detectar la β-hCG a comienzos de la gestación, éstos están asociados con diferentes tasas de falsos negativos. Además, la necesidad de un valor cuantitativo hace que la prueba del β-hCG en el suero sanguíneo sea el criterio estándar para las pruebas bioquímicas.[3]
Se mide la gonadotropina coriónica humana en la sangre, junto con la sonografía. Si está a niveles mayores de 1500 mUI/ml (entre la tercera y cuarta semana) o 5000 mUI/ml (entre la quinta y sexta semana) y si no se visualiza el feto en el saco, o si este último no está presente, se confirma entonces el diagnóstico.[11]
Los niveles de progesterona en sangre representan otra herramienta utilizada en predecir las posibilidades evolutivas de la gestación y no para la diferenciación entre gestaciones anormales y embarazos intrauterinos saludables.[7] Los niveles sanguíneos de progesterona no dependen de la edad gestacional, pero siguen siendo relativamente constantes durante el primer trimestre del embarazo normal y anormal, no retornan a los valores de referencia si comenzaron fuera del rango y no se correlacionan con niveles de β-hCG. Sin embargo, no hay consenso sobre un valor específico que distingue entre un embarazo normal de uno anormal. Varios autores han propuesto diferentes puntos de corte en relación con la sensibilidad y especificidad de este examen de sangre. Un valor de progesterona superior a 25 ng/ml demostró una exclusión de embarazo ectópico con 97,4 por ciento de certeza en un estudio.[5] Además, los niveles iguales o inferiores a 5 ng/ml indican un embarazo inviable,[11] bien sea intrauterino o ectópico, y excluyen el embarazo normal con una sensibilidad del 100 por ciento.[5]
Actualmente, se están estudiando otros marcadores en la sangre y en la orina, a fin de ayudar a distinguir los embarazos normales y anormales. Por ejemplo, el estradiol sérico, la inhibina, la proteína A asociada al embarazo, el glucurónido de pregnanediol, las proteínas de la placenta, la creatina quinasa y un perfil cuádruple que consiste en progesterona sérica, β-hCG, estriol y alfa-fetoproteína.
En la actualidad, el uso de cada uno de estos marcadores solo se indica como una herramienta de investigación hasta que aparezcan evidencias clínicas considerables que demuestren su aplicación clínica.
Diagnóstico por la imagen
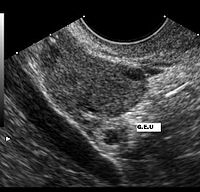
El ultrasonido es probablemente la herramienta más importante en el diagnóstico de un embarazo extrauterino, especialmente si se combina con otros métodos. Con mayor frecuencia, se utiliza para confirmar un embarazo intrauterino.[12] La visualización de un saco intrauterino, con o sin actividad cardíaca fetal, a menudo es suficiente para excluir un embarazo ectópico.[11] La excepción es en el caso de un embarazo heterotópico, la combinación de embarazos intra y extrauterino que, aunque es una situación excepcional, se ven cada vez más frecuentes, entre 1 de 4000 a 1 de cada 30 000 embarazos espontáneos. El estudio de los anexos uterinos por un ultrasonido es obligatorio en pacientes sometidas a estimulación ovárica y la reproducción asistida a pesar de la visualización de un embarazo intrauterino, porque son pacientes que tienen 10 veces mayor riesgo de embarazo heterotópico.
El ultrasonido transvaginal tiene mayor resolución que el abdominal y puede ser usado para visualizar un embarazo intrauterino 24 días después de la ovulación o 38 días después del último período menstrual, que suele ser alrededor de 1 semana antes de los que es posible visualizar un ultrasonido transabdominal. El saco gestacional —un término ecográfico y no anatómico— es la primera estructura que se reconoce en un ultrasonido transvaginal.[11] Se ve en el ultrasonido como una zona ecogénica gruesa en torno a un centro hipogénico correspondiente a la reacción decidual trofoblástica que rodea el saco coriónico. Las estructuras que representan a un embrión en desarrollo aún no se pueden reconocer sino hasta una mayor edad gestacional.[13]
Diagnóstico diferencial
Un 50 % de las pacientes que acuden al hospital con un embarazo ectópico presentan el trío de síntomas: sangrado vaginal, dolor y amenorrea. El otro 50 % acuden por otros motivos y acaban siendo diagnósticas. Es, sin embargo, el primer 50 % el que nos concierne.
Estos síntomas también pueden aparecer en pacientes con, principalmente, apendicitis. Pero también en pacientes que sufran de torsión ovárica, abscesos tubo-ováricos, hemorragias del cuerpo lúteo, roturas de quistes ováricos, amenazas de aborto o abortos incompletos, enfermedad pélvica inflamatoria o, incluso, cálculos renales.
El comienzo de un diagnóstico diferencial está en la historia del paciente y los exámenes físicos pertinentes. De estos exámenes físicos tendremos que prestar especial atención a la situación hemodinámica de la paciente hasta que sea posible la realización de un ultrasonido, el cual nos permitirá un diagnóstico casi con total seguridad certero.[14]
Tratamiento
Históricamente, el tratamiento de un embarazo ectópico se limitaba a la cirugía. Con la evolución y la experiencia con el metotrexato, el tratamiento de algunos embarazos ectópicos ha cambiado de curso.[6][15] El tratamiento médico de un embarazo ectópico es preferido sobre las opciones quirúrgicas por una serie de razones, incluida la eliminación de la morbilidad de la cirugía y la anestesia general, potencialmente menos daño tubario, y menos costo y necesidad de hospitalización.
Metotrexato
El metotrexato es un agente quimioterapéutico antimetabolito que se une a la enzima dihidrofolato reductasa, la cual participa en la síntesis de nucleótidos purinas. Esto interfiere con la síntesis del ADN y perturba la multiplicación celular. Su eficacia en el tejido trofoblástico ha sido demostrada y se deriva de la experiencia adquirida en el uso de metotrexato en el tratamiento de molas hidatidiformes y coriocarcinomas. El metotrexato se usa en el tratamiento de un embarazo ectópico en una o múltiples inyecciones intramusculares.
Este medicamento se utiliza también otro tipo de patologías como por ejemplo el cáncer, puesto que su mecanismo de acción se basa en inhibir la proliferación celular. En la práctica clínica se pueden seguir dos regímenes de tratamiento diferentes, ambos con un elevado éxito:
- Metotrexato y leucovorin en días alternos hasta que se produzca la bajada de la hormona gonadotropina coriónica humana. El leucovorin es un medicamento cuyo principio activo no es más que ácido fólico que se utiliza en este caso para poder compensar la inhibición por metotrexato. Este primer régimen de tratamiento tiene una tasa de éxito de hasta el 93 %.
- Única dosis de Metotrexato. Esta dosis es una dosis elevada y esperamos durante 4-7 días para ver si se produce la bajada de la hormona gonadotropina coriónica humana. En caso de que no se produzca una bajada significativa, son necesarias segundas y terceras dosis. Este régimen de tratamiento tiene una tasa de éxito de hasta el 90 %.
La elección de un régimen u otro depende de la práctica clínica habitual que tenga el centro hospitalario.
Cirugía
Con los avances en la capacidad de hacer un diagnóstico precoz y las mejoras en las técnicas de microcirugía, la cirugía conservadora ha sustituido a la laparotomía con salpingectomía del pasado. En las últimas dos décadas se ha recomendado el abordaje quirúrgico más conservador para un embarazo ectópico no roto usando cirugía mínimamente invasiva, para preservar la función de las trompas y permitir a la paciente la oportunidad de mantener la fertilidad.[11] Estas medidas incluyen la salpingectomía lineal y el ordeño del producto gestacional fuera de la ampolla distal.[3] El abordaje más radical incluye la resección del segmento de las trompas de Falopio que contiene la gestación con o sin la reanastomosis.[11]

La laparoscopia se ha convertido en el enfoque recomendado en la mayor parte de los casos. La laparotomía se suele reservar para las pacientes que se encuentren hemodinámicamente inestables o pacientes con embarazos ectópicos cornuales. También es un método preferido por cirujanos sin experiencia en laparoscopía y en pacientes donde es difícil el abordaje laparoscópico, por ejemplo, secundaria a la presencia de múltiples y densas adherencias fibrosas, la obesidad o hemoperitoneo masivo. Múltiples estudios han demostrado que el tratamiento laparoscópico de un embarazo ectópico da como resultado un menor número de adherencias postoperatorias que la laparotomía. Además, la laparoscopía se asocia con una pérdida significativamente menor de sangre y una menor necesidad de analgesia. Por último, la laparoscopia reduce el costo, la duración de la hospitalización y la del período de convalecencia.
Si la mujer quiere un embarazo en el futuro y está hemodinámicamente estable, el tratamiento de elección es la salpingostomía lineal, un abordaje a lo largo de la cara antimesentérica de la trompa afectada con la subsecuente extracción de los productos de la concepción.[7] Los embarazos ectópicos ubicados en la ampolla tubárica se encuentran por lo general entre la luz de la trompa y la serosa, y, por lo tanto, son candidatos ideales para la salpingostomía lineal.
En algunos casos es preferible la resección del segmento de la trompa que contiene el producto de la gestación o una salpingectomía total y no una salpingostomía.[3] Es el caso de pacientes con un embarazo ístmico o en pacientes con ruptura tubárica.[11]
Véase también
Referencias
- ↑ «Embarazo ectópico: MedlinePlus enciclopedia médica». medlineplus.gov. Consultado el 20 de diciembre de 2022.
- ↑ a b c d Solano Sánchez, Salvador Rafael; Patricia Maldonado Miranda y Eduardo Ibarrola Buen Abad (2005). «Tabaquismo como factor de riesgo para embarazo ectópico. Estudio de casos y controles en el Centro Médico ABC». MG An Med Asoc Med Hosp ABC 50 (2): 58-61. Consultado el 6 de mayo de 2009.
- ↑ a b c d e f g h Botella Llusiá, José; José A. Clavero Núñez (1993). Tratado de ginecología (14ª edición). Ediciones Díaz de Santos. ISBN 8479780924.
- ↑ a b c d e por MedlinePlus (febrero de 2008). [[1] «Emabarzo ectópico»]. Enciclopedia médica en español. Consultado el 6 de mayo de 2009.
- ↑ a b c d e f g Sepilian, Vicken P.; Ellen Wood (agosto de 2007). «Ectopic pregnancy». Obstetrics and Gynecology (en inglés). eMedicine.com. Consultado el 6 de marzo de 2009.
- ↑ a b Mahboob, U., Mazhar, S. B. (2006). «Management of ectopic pregnancy: a two-year study». Journal of Ayub Medical College, Abbottabad: JAMC 18 (4): 34-7. PMID 17591007.
- ↑ a b c d e f g González-Merlo, Jesús (2006). «Capítulo 28: Embarazo ectópico». Obstetricia (5ta edición). Elsevier España. ISBN 8445816101.
- ↑ Tayal, V. S.; Cohen, H.; Norton, H. J. (2004). Outcome of patients with an indeterminate emergency department first trimester pelvic ultrasound to rule out ectopic pregnancy. Acad Emerg Med 11: 912-7.
- ↑ a b c d Smith, Roger P.; Frank Netter (2004). Netter Obstetricia, Ginecologia y salud de la mujer. España: Elsevier. p. 247. ISBN 8445813110.
- ↑ AGUIRRE C., Viviana. Tabaquismo durante el embarazo: Efectos en la salud respiratoria infantil (en español). Rev. chil. enferm. respir. [online]. 2007, vol. 23, no. 3 [citado 2009-05-06], pp. 173-178. ISSN 0717-7348.
- ↑ a b c d e f g Gilbert, Elizabeth Stepp; Judith S. Harmon (2003). Manual de embarazo y parto de alto riesgo (3ra edición). Elsevier, España. ISBN 8481746894.
- ↑ Jaime, Botero Uribe; Alfonso Júbiz Hazbún y Guillermo Henao (2004). [[2] Obstetricia y ginecología: Texto integrado] (5ta edición). Corporación para Investigaciones Biológicas. p. 84. ISBN 9583358339.
- ↑ Callen, P. W. Ecografía en obstetricia y ginecología (5ta edición). Elsevier España. p. 227. ISBN 8445819348.
- ↑ Mummert T, Gnugnoli DM. (2020 Nov 20). «Ectopic Pregnancy». StatPearls.
- ↑ Clark, L., Raymond, S., Stanger, J., Jackel, G. (1989). «Treatment of ectopic pregnancy with intraamniotic methotrexate--a case report». The Australian & New Zealand journal of obstetrics & gynaecology 29 (1): 84-5. PMID 2562613. doi:10.1111/j.1479-828X.1989.tb02888.x.
 Wikimedia Commons alberga una categoría multimedia sobre Embarazo ectópico.
Wikimedia Commons alberga una categoría multimedia sobre Embarazo ectópico.