Gas
- Artikulu hau materiaren egoerari buruzkoa da; beste esanahietarako, ikus «Gas (argipena)».

Gasa[1] materiaren lau egoera nagusietako bat da. Ez dauka forma eta bolumen definiturik, eta libreki higitzen diren atomo edo molekulez osatua dago[2]. Materiaren egoera solidoarekin eta likidoarekin alderatura, gasak dentsitate eta likatasun txikiagoa dauka. Gas baten bolumena aldatu egiten da tenperatura edo presioa aldatzean, gas idealen legeak dioen bezala. Gasen beste ezaugarri nabarmen bat abiadura handiz hedatzeko gaitasuna da, edozein edukiontziren espazioa uniformeki bete arte[3].
Gas bat osatzen duten molekulek ia ez dituzte elkarrengana erakartzen, eta, beraz, hutsean mugitzen dira abiadura handian eta elkarrengandik oso bereizita, propietateak honela azalduz[3]:
- Gas baten molekulak ia libre daude, eta, beraz, gai dira horiek dauden espazio osoan banatzeko. Molekulen arteko grabitate[4]- eta erakarpen-indarrak gutxiesgarriak dira molekulak mugitzen diren abiadurarekin alderatuta.
- Gasek osorik hartzen dute horiek gordetzen dituen ontziaren bolumena.
- Gasek ez dute forma zehatzik, eta gasak gordetzen dituzten ontziena hartzen dute.
- Erraz konprima daitezke molekula batzuen eta besteen artean espazio huts handiak daudelako.
Lurrunek eta plasmak propietateak partekatzen dituzte gasekin, eta nahaste homogeneoak sor ditzakete, adibidez, ur- eta aire-lurruna; oro har, gas-gorputz, gas-egoera[5] edo gas-fase gisa ezagutzen dira.
Oinarrizko gasak

Baldintza estandarretan egonkorrak diren gas molekular diatomiko homonuklearrak diren elementu kimiko bakarrak hidrogenoa (H2), nitrogenoa (N2), oxigenoa (O2) eta bi halogeno dira: fluorra (F2) eta kloroa (Cl2). Gas noble monatomikoekin —helioarekin (He), neonarekin (Ne), argonarekin (Ar), kriptona (Kr), xenonarekin (Xe) eta radonarekin (Rn)— elkartzen direnean, oinarrizko gas esaten zaie gas horiei.
Izena
Gas hitza neologismoa da, Jan Baptist van Helmont kimikari flandriarrak proposatua XVII. mendean, grezierazko chaos (kaos) hitzaren nederlanderako ahoskatzearen idazkera fonetiko gisa. Euskaraz beste neologismo bat ere sortu zen XX. mendean, laspel, baina gaur egun ez da ia erabiltzen.
Historia
1648an, Jan Baptista van Helmont kimikariak, kimika pneumatikoaren aitatzat hartzen denak, gas hitza sortu zuen (denbora batez egoera aeriformea ere erabili zen), grezierazko kaos (nahasketa) hitzetik abiatuta, anhidrido karbonikoaren ezaugarriak definitzeko. Izendapen hori, gero, gas-gorputz guztietara hedatu zen, fluido elastikoak, fluido konprimagarriak edo aireak ere deituak, eta materiaren egoeretako bat izendatzeko erabiltzen da.
Gasek solidoen eta likidoen aldean duten ezaugarri nagusia da ezin direla ikusi eta ukitu, baina, haiek bezala, atomoz eta molekulez konposatuak daude.
Gasaren izaeraren zioa molekuletan dago, bata bestearengandik oso bereizita eta ausazko mugimenduekin. Materiaren beste bi egoerekin gertatzen den bezala, gasa ere likido bihur daiteke tenperatura oso baxuak jasaten baditu. Prozesu horri kondentsazioa esaten zaio lurrunen kasuan, eta likuefakzioa gas perfektuen kasuan.
Gas gehienek, kondentsazioa lortzeko, tenperatura oso baxuak behar dituzte. Adibidez, oxigenoaren kasuan, behar den tenperatura -183 °C-koa da[6].
Gasen lehen legeak XVII. mendearen amaieratik garatu ziren, zientzialariak konturatzen hasi zirenean gas lagin baten presio, bolumen eta tenperaturaren arteko erlazioetan, sistema itxi batean, gas guztientzat baliagarria izango zen formula bat lor zitekeela. Horiek antzera jokatzen dute baldintza ugaritan, molekulak elkarrengandik aldenduago daudelako, eta, gaur egun, gas ideal baten egoera ekuazioa teoria zinetikotik dator. Orain, gasen lehengo legeak gas idealaren ekuazioaren kasu berezitzat hartzen dira, konstante mantendutako aldagai batekin edo gehiagorekin.
Enpirikoki, tenperaturaren, presioaren eta bolumenaren arteko erlazio proportzionalak ikusten dira, gas idealen legea eragiten dutenak eta Émile Clapeyronek, 1834an, lehen aldiz ondorioztatua.
Ezaugarri fisikoak

Gasa osatzen duten atomoak edo molekulak modu independentean mugitzen dira (solido edo likido batekoak baino modu askeagoan), haiek batera mantenduko dituen edo sakabanatuko dituen indarrik gabe. Partikulen arteko elkarrekintza bakarrak talka bakan eta ausazkoak dira; bakoitza ausazko norabidean eta abiadura handian higitzen da. Abiadura tenperaturaren araberakoa da eta Maxwell-Boltzmann banaketaren bidez definitzen da. Beraz, gas fasea egoera guztiz kaotikoa da.
Gas baten egoera termodinamikoak hiru propietate dauzka: bolumena, tenperatura eta presioa. Aldagai hauen arteko erlazioa gas idealen funtsezko legearen bidez azaltzen da: gas ideal baten presioa bere tenperaturarekiko eta molekula-kopuruarekiko proportzionala eta bere bolumenarekiko alderantziz proportzionala da.
Likidoak eta plasmak bezala, gasak ere fluido isurkor eta askeak dira. Higitu ondoren, ez dira beren jatorrizko konfiguraziora itzultzen. Likidoek ez bezala, huts-ingurune batean gordetako gas askeek ez dute bolumen finkorik betetzen; horren ordez, espazio osoa bete arte hedatzen dira. Kontuan izan behar da baldintza hau soilik gertatzen dela huts-inguruneetan. Esaterako, aire zabalean karbono dioxidoa isurtzen bada, gasa ez da hedatuko eta lurrera eroriko da, airea dentsoagoa delako.
Gasen portaera makroskopikoa
Gas bat behatzean, ohikoa da erreferentzia-marko bat edo luzera-eskala bat zehaztea. Luzera handiagoko eskala gasaren ikuspuntu makroskopiko edo global bati dagokio. Alde horrek (bolumena) gas-partikulen lagin handi bat edukitzeko adinako tamaina izan behar du. Lagin-tamaina horren ondoriozko estatistika-analisiak aldean dauden gas-partikula guztien batez besteko portaera sortzen du (hau da: abiadura, tenperatura edo presioa). Aitzitik, luzera txikiagoko eskala ikuspuntu mikroskopiko bati edo partikulen ikuspuntu bati dagokio.
Makroskopikoki, gasaren ezaugarriak gasaren partikulen (abiadura, presioa edo tenperatura) edo ingurunearen (bolumena) arabera neurtzen dira. Adibidez, Robert Boylek kimika pneumatikoa ikasi zuen bere ikasketa-ibilbidearen zati txiki batean. Bere esperimentuetako batek presioaren propietate makroskopikoak eta gas baten bolumena erlazionatu zituen. Bere esperimentuan, J hodi-manometro bat erabili zuen, J hizkiaren formako saiakuntza-hodi bat dirudiena. Boylek gas inerte bat harrapatu zuen saiakuntza-hodiaren mutur itxian merkurio-zutabe batekin, eta horrek partikula-kopurua eta tenperatura konstanteak izatea eragiten du. Gasaren presioa handitzen zenean, harrapatutako gasaren bolumena murriztu egiten zela ikusi zuen zutabeari merkurio gehiago gehitzean (horri, alderantzizko erlazioa esaten zaio). Gainera, Boylek behaketa bakoitzaren presioa eta bolumena biderkatu zituenean, produktua konstantea izan zen. Harreman hori mantendu zen Boylek behatutako gas bakoitzerako, eta horrek (PV=k) legera eraman zuen, arlo horretan berak egindako lanaren omenez izendatua.
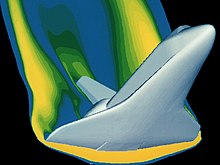
Tresna matematiko asko daude gasen propietateak aztertzeko. Gasak muturreko baldintzen mende dauden heinean, tresna horiek konplexuagoak bihurtzen dira: fluxu ez likatsurako Eulerren ekuazioetatik hasi eta efektu likatsuak erabat azaltzen dituzten Navier-Stokesen ekuazioetaraino[7]. Ekuazio horiek kasuan kasuko gas-sistemaren baldintzetara egokitzen dira. Boyleren laborategiko taldeak algebra erabiltzea ahalbidetu zuen bere emaitza analitikoak lortzeko. Emaitzak, gasak aztertzen ari zelako presio nahiko baxuko egoeretan, posible izan ziren modu ezin hobean jokatzen zutelako. Erlazio ideal horiek erabiltzen diren materialetan, hainbat hegaldi-baldintzatarako segurtasun-kalkuluei aplikatzen zaizkie. Gaur egun erabiltzen den goi teknologiako ekipoa ingurune operatibo exotikoenak segurtasunez esploratzen laguntzeko diseinatu zen, non gasek jada ez duten modu ezin hobean jokatzen. Matematika aurreratu horrek estatistikak eta aldagai anitzeko kalkulua barne hartzen ditu, eta aukera ematen du egoera dinamiko konplexuak konpontzeko, hala nola ibilgailu espazialak berriz sartzea. Adibidez, irudian agertzen den espazio-anezkaren birsarreraren analisia karga baldintza horren behean materialaren propietateak egokiak direla bermatzeko. Hegaldi-erregimen horretan, gasak jada ez du modu ezin hobean jokatzen.
Gasen legeak
Lege askok aztertzen dute gasen presioa, bolumena eta tenperatura arteko erlazioa.
Boyle-Mariotteren legea
Boyle-Mariotteren legea gas idealen legeetako bat da, prozesu isotermoa aztertzen duena hain zuzen ere. Robert Boylek Oxforden (1664) eta Edme Mariottek Parisen (1676), bakoitzak bere aldetik, aurkituriko legea da.
Legeak dioenez, gas baten sartu-irtenik gabe gasaren tenperatura konstante mantentzen bada gas honen gaineko presioa eta gasaren bolumena alderantziz proportzionalak dira. Hau da:
Ikurrak:
- = Hasierako presioa (atm)
- = Hasierako bolumena (litro)
- = Amaierako presioa (atm)
- = Amaierako bolumena (litro)
Boyleren saiakuntza

Hau da Boylek egin zuen esperimentua. Tenperatura konstante mantenduz, presioa handitu ahala bolumena jeisten zela ikusi zuen, baina, beti ere, bien arteko biderkaketa konstante mantentzen zen. Horretarako, ontzi batean, gasa sartu zuten, eta, goiko aldean, enbolo batekin hermetikoki itxi. Enboloan pisua jarriz, hura jeitsi eta bolumena txikitzen zenean, ontzi barruko gasaren presioa igo egiten zen; aldiz, enboloa jasoz, presioa txikitu egiten zen bolumena handitzean.
Azalpena
Bolumena txikitzerakoan, gas molekulek toki gutxiago dute mugitzeko, eta maizago jotzen dituzte ontziaren hormak. Aldiz, bolumena handitzerakoan, molekulek toki gehiago dute, eta hormen kontrako talkak gutxiagotu egiten dira.
Charlesen legea
Charlesen legea
Charlesen legea Jacques Charles fisikari frantziarrak 1787an azaldutako legea da, baina ez zen ezagutarazi 1802 arte, Gay-Lussacek beronen berri eman zuen arte. John Dalton kimikari ingelesak, bere aldetik, lege bera lortu zuen 1801ean (oraindik, Charlesen legea publikatu gabe zegoen), baina Charlesek, lehenago aurkitzeaz gain, askoz hobeto dokumentatua zuenez beronen izena darama legeak.[8].
Legea
Legeak dioenez, gas baten sartu-irtenik gabe gasaren presioa konstante mantentzen bada, gas horren bolumena eta gasaren tenperatura zuzenki proportzionalak dira. Hau da:
Ikurrak:
- = Hasierako bolumena (litro)
- = Hasierako tenperatura (ºK)
- = Amaierako bolumena (litro)
- = Amaierako tenperatura (ºK)
Saiakuntza

Charlesek, ontzi batean, gas bat sartu zuen goian enbolo batek hermetikoki ontzia ixten zuelarik. Orduan, ontzia berotzerakoan enboloa igo egiten zela (bolumena handitzearen ondorioz) ikusi zuen, eta berriz hozten uzterakoan enboloa jeisti egiten zela.
Azalpena
Gasa berotzerakoan, gasaren molekulek abiadura handiagotzen dute, eta hormen kontrako talkak ugaritzen dira ontziaren berneko presioa handituz. Enboloak gora jotzen du presio atmosferikoarekin berdintzen den arte.
Gay-Lussacen legea

Gay-Lussacen legea Louis Joseph Gay-Lussac kimikari frantziarrak 1805ean azaldutako legea da. Gas idealen legeetako bat da.[9]:
Legea
Legeak dioenez, gas baten sartu-irtenik gabe gasaren bolumena konstante mantentzen bada, gas horren presioa eta gasaren tenperatura zuzenki proportzionalak dira. Hau da:
Ikurrak:
- = Hasierako presioa (atm)
- = Hasierako tenperatura (ºK)
- = Amaierako presioa (atm)
- = Amaierako tenperatura (ºK)
Saiakuntza
Gay-Lussacek gas bat sartu zuen ontzi itxi batean. Ontziaren azpian, pizgailua jarriz gasa berotu, eta ontziaren hormen kontrako presioa handitu zela ikusi zuen. Bero iturria itzaltzerakoan, presioa jeisten joan zen hasierako egoerara iritsi arte.
Azalpena
Gasaren molekulak berotzerakoan azkarrago mugitzen dira, eta, beraz, hormen aurka egiten dituzten talkak ugaritu egiten dira. Aldiz, tenperatura jeistean, molekulak moteldu egiten dira, eta hormen aurkako talkak, gutxitu.
Gasen lege orokorra
Gasen lege orokorrak presio, tenperatura eta bolumen aldagaiekiko hauen portamoldea argitzen du. Honela, gas masa konstante batean, aldagai hauen arteko erlazioa hurrengo berdinketak ezartzen du:
Gas idealen legeak
Txantiloi:Sakontzeki Gas idealen legeak gas idealek presio, bolumen eta tenperaturaren artean dituzten erlazioak azaltzen dituzten legeak dira.
Legeak argitzen duenez, aldagai osagarrien doitze bat eragingo du hasierako egoera betako (1) gas batean aldagai baten magnitude bat aldatzean berdintasuna mantentzeko amaiera egoeran (2).
Tenperatura konstante mantentzen bada (T1=T2), posible da berau ekuaziotik kentzea. Beraz berdintasuna presio eta bolumen arteko aldaketen bidez mantentzen da.

Gas idealen ekuazioa
Émile Clapeyronek azaldu zuen lehenengo aldiz, 1834ean. Aurretik Boyle, Mariotte, Charles eta Gay-Lussacek eginiko lanak bateratu ostean lortu zuen ekuazioa sortzea. Ekuazioa honako hau da:
Ikurrak:
- = Presio absolutua (atmosferatan neurtua)
- = Bolumena (litrotan)
- = Gas molak
- = gas idealen konstante unibertsala (0'082)
- = Tenperatura absolutua (Kelvinetan)
Legeak argitzen duenez, aldagai osagarrien doitze bat eragingo du hasierako egoera betako (1) gas batean aldagai baten magnitude bat aldatzean berdintasuna mantentzeko amaiera egoeran (2).
Tenperatura konstante mantentzen bada (T1=T2), posible da berau ekuaziotik kentzea. Beraz berdintasuna presio eta bolumen arteko aldaketen bidez mantentzen da.
Daltonen legea
Daltonen legeak gas nahasketa baten guztirako presioa gas bakoitzak bolumen osoa okupatuko balitz eragiten dituzten presioen batzea dela argitzen du.
- or
Lege hau presio partzialen legea bezala ere ezagutzen da, gas batek X presioan batean duen presio partziala nahasketan dagoen gasen proportzioarekin zuzenki proportzionala baita.
Hau da, gas nahasketa batean osagai batek P presioan nahasketaren bolumenaren %20 betetzen badu, osagai horrek 0,2 Pko presio partzial bat du.
Henry legea (gasen disoluzioa)
Henry-ren legea: Disoluzio diluitu ideal batean, solutu baten lurrunaren presioa ematen digu. Disolbatzailearentzat Roult-en legea erabiltzen jarraitzen da: PA=xAP∗A
Gas bat likido batekin harremanetan ipintzean, gasaren molekulak (bere energia termodinamikoa -presio eta tenperatura- dela eta) gas-likido interfasean sartu, eta haren barnean banatzen dira. Egoera horri gasen disoluzioa esaten zaio, hau da, gas-likido disoluzio baten eraketa. Gas bat fase likidoan disolbaturik dagoenean, gasaren kontzentrazioari, (c) esaten zaio fase gaseosoan dagoenean eta presio partzialarentzako (p) erabiltzen den bitartean. Bada, Henry-ren legeak, bi adierazpen erlazionatzeko, Henryren konstantea erabiltzen du, horrela desio den presioa kalkulatzea ahalbidetuz.

Horretarako, disolbatzaile bat eta solutuak dituen disoluzio diluitu ideal bat dagoenean, solutuek gas fasean eragiten duen presioa kalkulatzen da.
- Behin oreka lortuta:
μi,l(T,P)=μi,v(T,P) (1)
- Potentzial kimikoak, bere baloreengatik ordezkatuz:
μ0i,l(T,P)+RTlnxi=μ0i,v(T)+RTlnPiP0 (2)
- Terminoak elkartuz eta propietate logaritmiko nepertarrak erabiliz:
μ0i,l(T,P)−μ0i,v(T)RT=lnPixiP0 (3)
- Bakanduz
P0eμ0i,l(T,P)−μ0i,v(T)RTKH=Pixi (4)
- KH Henry-ren konstantea
Pi=KHxi (5)
Henry legeak argitzen duenez, tenperatura jakin batean eta saturazioa egoeran, likido batean disolbatzen den gas kopurua gasak likidoaren azalean eragiten duen presioarekiko zuzenki proportzionala da.
Henry legean izendatzen duen saturazio kontzeptuak gasaren presioren (gas egoeran) eta bere tentsioaren (likido egoeran) dagoen orekaz ari da. Presioa tentsioa baino handiago denean, azpisaturazio egoera esaten zaio; berdinak direnean, saturazio esaten zaio, eta presioa disolbaturiko gasaren tentsioa baino txikiagoa denean, supersaturazioa esaten zaio. Azpisaturazioan dagoen likido batek gas egoerako gasa disolbatuko du oreka (saturazio) iritsi arte. Supersaturazio egoeran, disolbaturiko gasa botako du oreka (saturazio) egoerara iritsi arte.
Grahamen legea (gasen zabalkundea)
Bi gasen arteko zabalkunde fenomenoa. Lege horrek gasak nahasteko abiadura argitzen du. Oinarrian, tenperatura eta presio egoera beretan, bi gasen arteko zabalkundea gasen masa molarren erro karratuarekiko alderantziz proportzionala dela dio.
non:
- v1 = 1 gasaren zabalkunde abiadura
- v2 = 2 gasaren zabalkunde abiadura
- d1 = 1 gasaren dentsitatea
- d2 = 2 gasaren dentsitatea
Beste era batera esanda, tenperatura eta presio berean, molekula arinak dituen gas baten zabalkunde abiadura molekula astunak dituena baino handiago da.
Fick legea (gasen zabalkundea)
Gas batek zuntz bat (edo ehun kapa bat) zeharkatzeko duen transferentzia tasa azaltzen du. Hura, ageriko superfiziearekiko eta bere bi egoeren arteko ezberdintasunarekiko, proportzionala da, eta, zuntz/ehunaren lodierarekiko, alderantziz proportzionala da. Zabalkunde abiadura, gainera, zabalkunde konstantearekiko (parte hartzen duten ehun eta gas bakoitzerako bakarra), proportzionala da.
Gas erreala
Gas erreal bat, gas ideal baten aurrean, gas idealen legea erabiliz erabat azaldu ezin diren propietateak erakusten dituen gasa da. Gas errealen portaera ulertzeko, honako hau hartu behar da kontuan:
- konprimagarritasun-efektuak
- Bero-ahalmen espezifiko aldakorra
- Van der Waalsen indarrak
- Orekarik ezaren efektu termodinamikoak
- Disoziazio molekularra eta konposizio aldakorreko oinarrizko erreakzioak dituzten gaiak.
Aplikazio gehienentzat, hain analisi zehatza ez da beharrezkoa, eta gasaren hurbilketa ideala arrazoizko zehaztasunez erabil daiteke. Bestalde, gas errealaren ereduak gasen kondentsazio-puntutik gertu erabili behar dira, puntu kritikoetatik gertu, presio oso altuetan, eta, beste kasu batzuetan, ez dira hain ohikoak.
Gehiago findu nahi bada edo portaera idealari ihes egiten dion gasen portaera neurtu nahi bada, gas errealen ekuazioetara jo beharko da, askotarikoak eta konplikatuagoak baitira zenbat eta zehatzagoak izan.
Gas errealak ez dira infinituki hedatzen, bolumen gehiago hartuko ez luketen unea iritsiko bailitzateke. Horren arrazoia da bere partikulen artean, atomoak zein gas nobleetan edo molekuletan (O2) (gas gehienetan bezala), nahiko indar txikiak ezartzen direla karga elektrostatikoen ausazko aldaketen ondorioz, Van der Waalsen indarrak deitutakoak.
Zenbat eta errazagoa izan bere formula kimikoa eta zenbat eta txikiagoa izan bere erreaktibotasuna (loturak sortzeko joera), orduan eta gehiago egiten du bat gasaren portaerak portaera idealarekin. Horrela, adibidez, gas nobleek, molekula monoatomikoak direnez eta erreaktibotasun oso txikia dutenez (batez ere helioak), idealetik nahiko hurbil dagoen portaera izango dute. Ondoren, gas diatomikoak etorriko dira, bereziki hidrogeno arinena. Ez dira hain idealak izango triatomikoak, karbono dioxidoa bezala; ur-lurrunaren kasua are okerragoa da; polarra denez, hidrogenozko zubiak ezartzeko joera dute molekulek, eta horrek idealtasuna are gehiago murrizten du. Gas organikoen barruan, portaera egokiena metanoak izango du, karbono-katea koipeztatu ahala idealtasuna galduz. Horrela, butanoa idealtasunetik urrun samar egongo dela espero izatekoa da. Hau da, gasa osatzen duen partikula zenbat eta handiagoa izan, orduan eta probabilitate handiagoa elkarren artean talka egiteko eta elkarreragiteko, eta faktore horrek idealtasuna murrizten du. Gas horietako batzuk nahiko ondo hurbil daitezke ekuazio idealen bidez; beste kasu batzuetan, berriz, parametroen doikuntzatik enpirikoki askotan kendutako ekuazio errealetara jo beharko da.
Idealtasuna ere muturreko baldintzetan galtzen da, hala nola presio altuetan edo tenperatura baxuetan. Bestalde, idealtasunarekiko bat-etortzea areagotu egin daiteke presio baxuetan edo tenperatura altuetan lan egiten badugu. Baita egonkortasun kimikoagatik ere.
Portaera eskala mikroskopikoan
Gas bat mikroskopio baten bidez behatu ahal izango balitz hura osatzen duten partikulak (molekulak, atomoak, ioiak) ikusteko bezain indartsu batekin, modu aleatorioan edo gutxi-asko mugituz ikusiko genituzke. Gasa osatzen duten partikula horiek mugimenduaren norabidea soilik aldatzen dute beste partikula batekin edo edukiontziko hormen kontra talka egiten dutenean. Talka horiek guztiz elastikoak direla uste badugu, substantzia gas idealtzat har dezakegu. Partikulen portaera, maila mikroskopikoan, gasen teoria zinetikoak deskribatzen du.
Gasen teoria zinetikoa


Teoria zinetiko molekularrak gasen portaera eta propietateak adierazten ditu. Teoria zinetiko molekularra Daniel Bernoulli, Ludwig Boltzmann eta James Clerk Maxwellen ikerketei esker garatu zen XIX. mendearen bigarren zatian.
Teoria zinetikoak gasen propietate makroskopikoei buruzko informazioa ematen du, konposizio molekularra eta mugimendua kontuan hartuta. Momentuaren eta energia zinetikoaren definizioekin hasita, momentuaren kontserbazioa eta kubo baten erlazio geometrikoak erabil daitezke tenperatura- eta presio-sistemaren propietate makroskopikoak molekula bidezko energia zinetikoaren propietate mikroskopikoarekin lotzeko. Teoriak, bi propietate hauentzako, batez besteko balioak ematen ditu.
Gasen teoria zinetikoak sistemak (gas-partikulen bilduma kontuan hartuta) nola erantzuten dien tenperatura-aldaketei azaltzen lagun dezake, dagokion energia zinetikoaren aldaketarekin.
Adibidez: imajina dezagun gas-partikula kopuru finko bat duen tamaina finkoko ontzi zigilatu bat dugula (bolumen konstantea); zero absolututik abiatuta (atomoek edo molekulek energia termikorik ez duten tenperatura teorikoa; hau da, ez dira mugitzen, eta ez dute bibratzen), sistemari energia gehitzen hasten gara ontzia berotuz barneko partikuletara energia transferitzeko. Bere barne energia zero puntuko energiaren gainetik dagoenean, hau da, bere energia zinetikoa (energia termikoa ere esaten zaio) zero ez denean, gas partikulak edukiontziaren inguruan mugitzen hasiko dira. Ontzia gehiago berotu ahala (energia gehiago gehitu ahala), partikulen batez besteko abiadura handitu egiten da sistemaren barne-energia osoa handitu ahala. Partikula guztien batez besteko abiadura handiagoa denez, talkak abiadura handiagoan gertatzen dira (hau da, talka gehiago denbora-unitateko) partikulen eta edukiontziaren artean, bai eta partikulen artean ere.
Maila makroskopikoan, presioaren kantitate neurgarria partikula eskopikoen mikro talka horien eta gainazalaren arteko zuzeneko emaitza da. Horren gainean, molekula indibidualek indar txiki bat eragiten dute, eta bakoitzak eremu espezifiko baten barruan aplikatutako guztizko indarrari laguntzen dio.
Halaber, makroskopikoki neur daitekeen tenperatura kantitatea, horrenbestez, partikulek erakusten duten mugimenduaren edo energia zinetikoaren guztizko kantitatearen kuantifikazioa da.
Higidura browniarra

Higidura browniarra fluido batean esekitako partikulen ausazko mugimendua deskribatzeko erabiltzen den eredu matematikoa da. Gas-partikulen animazioak (partikula arrosak eta berdeak erabiliz) erakusten du portaera horrek gasen hedapena (entropia) eragiten duela. Gertakari horiek partikulen teoriaren bidez ere deskribatzen dira.
Banakako gas-partikulak (atomoak edo molekulak) behatzea egungo teknologiaren mugan (edo harantzago) dagoenez, kalkulu teorikoek bakarrik ematen dute horiek mugitzeko moduari buruzko iradokizuna, baina higidura browniarra ez bezalakoa da, higidura browniarrak arrastatze-indar leuna baitakar gas-molekula askoren marruskadura-indarraren ondorioz, gas-molekula batek (edo batzuek) partikularekin izandako talka bortitzen ondorioz puntuatua. Partikulak (normalean, milioika edo milaka milioi atomo ditu), horrela, ibilbide irregular batean mugitzen dira, baina ez gas molekula indibidual bat aztertuz gero espero litzatekeen bezain irregularra.
Molekula arteko indarrak
Gas bat konprimatzean, molekulen arteko indarrek, hala nola irudiaren ur-molekulen arteko hidrogeno-loturek, paper aktiboagoa izaten hasten dira.
Partikulen arteko une bateko atrakzioek edo aldaratzeek eragina dute gasaren dinamikan. Kimika fisikoan, molekulen arteko indarren izena Van der Waalsen indarra da. Indar horiek zeregin bat dute gas baten propietate fisikoak zehazteko, hala nola likatasun edo fluxu bolumetrikoa. Indar horiek, baldintza jakin batzuetan, alde batera uzten baditugu, gas erreal bat gas ideal bat balitz bezala tratatu ahal izango dugu, eta, horrela, gas idealen legea erabili ahal izango dugu. Gasekiko erlazio horiek behar bezala erabiltzeko, teoria zinetikora itzuli behar da. Gasaren partikulek karga magnetikoa edo molekulen arteko indarra dutenean, beste molekuletan duten eragina areagotu egiten da haien arteko espazioa murriztu ahala. Kargarik ez dagoenean, partikulen arteko espazioa puntu jakin batera behar adina murriztu denean, partikulen arteko talkak ezin dira saihestu tenperatura normal batean.
Gas baten partikulen arteko talka-kopurua handitzeko, beste bide bat litzateke gas-bolumen finko jakin bat berotzea, gainera, partikulen tenperatura handiagoa, beraz, talkak izateko probabilitate handiagoa. Horrek guztiak esan nahi du ekuazio ideal horiek arrazoizko emaitzak ematen dituztela presio edo tenperatura handiko kasuetan izan ezik (ionizazioa). Salbuespenezko baldintza horiek aukera ematen dute gasaren barruan energia transferitzeko, eta, hain zuzen ere, energiaren barne-transferentziarik ez egoteak ahalbidetzen du baldintza idealei buruz hitz egitea, energia-trukea sistemaren mugetan bakarrik gertatzen baita.
Gas errealek talka eta indar intermolekular horietako batzuk izaten dituzte, baina, estatistikoki gutxiesgarriak diren bitartean, ekuazio idealen emaitzak baliozkoak izaten jarraituko dute. Bestalde, gas baten partikulak elkarrengandik oso hurbil daudenez konprimatzen direnean, gasak likido baten antzekoago jokatzen du, eta energiaren barne-transferentziarik ezak baldintza idealei buruz hitz egitea ahalbidetzen digu, energia trukea sistemaren mugetan bakarrik gertatzen baita. Gas errealek talka eta molekula arteko indar horietako batzuk izaten dituzte, baina, estatistikoki gutxiesgarriak diren bitartean, ekuazio idealen emaitzak baliozkoak izaten jarraituko dute.
Gasen portaera
Materiaren partikulen portaera termikorako interes handikoak diren lau kantitate neurgarri daude: presioa, bolumena, tenperatura eta materialaren laginaren masa (edo are hobeto substantzia kantitatea, moletan neurtuta).
Edozein gas fluidotzat hartzen da jariakin gisa jokatzeko aukera ematen dioten propietateak dituelako.
Molekulek, etengabe mugitzen ari direla, elastikoki talka egiten dute beren artean eta gasa duen ontziaren hormen kontra, eta presio iraunkorra egiten dute haien aurka. Gasa berotzen bada, bero-energia hori molekulen energia zinetikoan inbertitzen da; hau da, molekulak azkarrago mugitzen dira, eta, beraz, ontziaren hormen aurkako talka-kopurua handitu egiten da kopuruari eta energiari dagokionez. Ondorioz, gasaren presioa handitu egiten da, eta, ontziaren paretak zurrunak ez badira, gasaren bolumena handitu egiten da.
Gas batek kimikoki aktiboa izateko joera du bere gainazal molekularra ere handia delako; hau da, bere partikulak etengabeko mugimenduan daudenez bata bestearekin talka egiten, errazagoa egiten du substantzia baten eta bestearen arteko kontaktua, erreakzio abiadura handituz likidoekin edo solidoekin alderatuta.
Gas baten portaera hobeto ulertzeko, beti gas idealari buruzko azterketak egiten dira, gas ideala inoiz existitzen ez bada ere, eta hauek dira gas idealaren propietateak:
- Substantzia gaseoso purua, hortaz, tamaina eta masa bereko molekulek osatzen dute. Substantzia gaseosoen nahasketa, beraz, tamaina eta masa desberdineko molekulek osatzen dute.
- Molekula batzuen eta besteen artean distantzia handia dagoenez eta abiadura handian mugitzen direnez, molekulen arteko erakarpen-indarrak gutxiesgarritzat jotzen dira.
- Gasaren molekulen tamaina oso txikia da; beraz, molekulek hartzen duten bolumena gutxiesgarria da ontziaren guztizko bolumenarekin alderatuta. Gas baten dentsitatea oso txikia da.
- Gas baten molekulak etengabe mugitzen dira abiadura handian, eta, beraz, elastikoki talka egiten dute beren artean eta horiek edukitzen dituen ontziaren hormen kontra.
Gasen portaera azaltzeko, teoria berriek, propietate edo mugako propietate desberdinetako gasekin (UF6 izenez ezagutzen den gasik astunena dena) esperimentatzeaz gain, estatistika zein teoria kuantikoa erabiltzen dituzte.
Gas batek ez du, ez formarik, ez bolumen finkorik ere; bere molekulen kohesio ia nulua eta energia zinetiko handia ditu ezaugarri, eta horiek mugitu egiten dira.
Dentsitatea
Tenperaturak eta presioak solidoengan eta likidoengan duten eragina oso txikia denez, likido edo solido baten konprimagarritasuna da: 10-6 bar-1 (1 bar=0,1 MPa), eta dilatazio-koefiziente termikoa da: 10-5 K-1.
Bestalde, presioak eta tenperaturak eragin handia dute gasen dentsitatean. Gas idealen legeak matematikoki deskribatzen du hiru magnitude hauen arteko erlazioa:
non gas idealen konstantea, gasaren presioa, masa molarra eta tenperatura absolutua den.
Horrek dakar 300 K (27 °C) eta 1 atm-ko gas ideal batek bere dentsitatea bikoiztuko duela presioa 2 atm-ra igotzen bada tenperatura konstantea mantenduz edo, txandaka, tenperatura 150 K-ra jaisten bada presio konstantea mantenduz.
Gasaren presioa
Teoria zinetikoaren esparruan, gas baten presioa gasaren molekulek edukiontziaren paretekin talka egiten duten indarren emaitza makroskopiko gisa azaltzen da. Presioa, beraz, gasaren propietate mikroskopikoei erreferentzia eginez defini daiteke.
Izan ere, N molekuladun gas ideal batentzat (bakoitza m masaduna eta vrms batez besteko ausazko abiadura V bolumen kubiko bateko edukian), gasaren partikulek ontziaren paretekin talka egiten dute, modu estatistikoan kalkula daitekeen moduan talka bakoitzean paretekin trukatuz momentu lineal eta area unitateko indar garbi bat eginez; bada, hura da, gainazal solidoan, gasak eragindako presioa.
Presioa honela kalkula daiteke:
(gas ideala)
Emaitza hori interesgarria eta esanguratsua da, ez bakarrik gas baten presioa kalkulatzeko modu bat eskaintzen duelako, baizik eta aldagai makroskopiko behagarri bat, presioa, molekula bidezko batez besteko energia zinetikoa, 1/2 mv rms², zuzenean ikus ezin daitekeen magnitude mikroskopikoa delako. Kontuan izan ontziaren bolumenak eragindako presioaren emaitza jasotako gas-molekulen guztizko energia zinetikoaren bi heren dela.
Topiko bereziak
Konprimatasuna

Termodinamikan ("Z") faktorea gas idealaren ekuazioa aldatzeko erabiltzen da gas errealen konprimagarritasun-efektuak kontuan hartzeko. Faktore horrek bolumen espezifiko errealen eta idealen arteko erlazioa adierazten du. Batzuetan, aldaketa-faktorea edo diseinu-helburuetarako gas idealen legearen tarte erabilgarria zabaltzeko zuzenketa esaten zaio. Normalean Z-ren balio hori unitatetik oso gertu dago. Konprimagarritasun-faktorearen irudiak, tenperatura oso hotzetan, Z nola aldatzen den erakusten du.
Reynolds zenbakia
Fluidoen mekanikan, Reynolds zenbakia inertzia-indarren (vsρ) eta indar likatsuen (μ/L) arteko erlazioa da. Zenbaki adimentsional garrantzitsuenetako bat da fluidoen dinamikan, eta, eskuarki, beste zenbaki adimentsional batzuekin batera, antzekotasun dinamikoa zehazteko irizpidea emateko erabiltzen da. Horrela, Reynolds zenbakiak modelaketaren emaitzen (diseinua) eta eskala handiko benetako baldintzen arteko lotura ematen du. Fluxua karakterizatzeko ere erabil daiteke[9].
Likatasuna
Likatasun edo biskositatea fluido guztiak duten propietate fisiko bat da, eta hori fluido batean aurkitzen diren eta abiadura ezberdinetan mugitzen diren partikulen arteko kolisioetatik sortzen da, mugimenduari erresistentzia indar bat sortuz teoria zinematikoaren arabera. Fluido bat tubo baten barnealdetik pasarazten denean, fluido horren partikulak azkarrago mugitzen dira tuboaren ardatzetik gertu eta geldoago tuboaren paretetatik gertu direnak. Horregatik, ezinbestekoa da indar ebakitzaileak existitzea marruskadura indarrak ezarritako erresistentzia indarrak gainditu eta fluidoa mugitu ahal izateko. Hori gertatuko ez balitz, ez litzateke mugimendurik existituko.
Turbulentzia
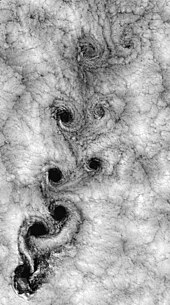
Fluidoen dinamikan, turbulentzia edo fluxu zurrunbilotsua fluxu-erregimen bat da, ezaugarri hauek dituena: une jakin bateko difusio txikia, konbekzio handia eta presio- eta abiadura-aldaketa espazial azkarrak. Zurrunbilotsuak ez diren fluxuei, fluxu laminar deitzen zaie. Fluxu bat laminarra edo zurrunbilotsua izan daiteke Reynolds zenbakiaren magnitude-ordena begiratuz.
Muga-geruza
Partikulak bere baitan mugitzen den objektu baten gainazalean itsasten dira. Partikula-geruza horri muga-geruza deitzen zaio. Objektuaren gainazalean, funtsean, estatikoa da gainazalaren marruskaduraren ondorioz. Objektua, bere muga-geruzarekin, objektuaren forma berria da, objektua hurbildu ahala gainerako molekulek ikusten dutena. Muga-geruza hori azaleratik bereiz daiteke funtsean azalera berri bat sortuz eta fluxuaren ibilbidea erabat aldatuz. Horren adibide klasikoa galeran sartzen den profil hegoarra da. Delta hegalaren irudiak argi eta garbi erakusten du muga-geruzaren lodiera, gasak eraso-ertzean zehar eskuinetik ezkerrera egiten duen heinean[9].
Entropia maximoaren printzipioa
Askatasun graduen kopuru osoa infinitura hurbiltzen den heinean, sistema aniztasun handienari dagokion makroegoeran aurkituko da. Printzipio hori irudikatzeko, begiratu metalezko barra izoztu baten gainazaleko tenperatura. Gainazaleko tenperaturaren irudi termikoa erabiliz, behatu gainazaleko tenperaturaren banaketa. Tenperaturaren hasierako behaketa horrek mikroegoera adierazten du. Etorkizuneko uneren batean, gainazaleko tenperaturaren bigarren behaketa batek bigarren mikroegoera sortzen du. Behaketa-prozesu horrekin jarraitzean, litekeena da barraren gainazalaren historia termikoa ilustratzen duten mikroegoera batzuk sortzea. Mikroegoeren serie historiko horren karakterizazioa posible da guztiak multzo bakar batean arrakastaz sailkatzen dituen makroegoera aukeratuz.
Oreka termodinamikoa
Sistema baten energia-transferentzia amaitzen denean, egoera horri, oreka termodinamikoa esaten zaio. Oro har, baldintza horrek esan nahi du sistema eta inguruak tenperatura berean daudela, eta, beraz, beroa ez da jada haien artean transferitzen. Era berean, kanpoko indarrak orekatuta daudela (bolumena ez da aldatzen) eta sistemaren barruko erreakzio kimiko guztiak osatuta daudela esan nahi du. Sistemaren arabera, kronograma aldatu egiten da gertaera horietarako. Giro-tenperaturan urtzen den izotz edukiontzi batek orduak eramango ditu; erdieroaleetan, berriz, gailua piztuta egotetik itzalita egotera doan trantsizioan gertatzen den bero-transferentzia nanosegundo gutxi batzuen ordenakoa izan liteke.
Ikus, gainera
Erreferentziak
- ↑ Euskaltzaindiaren hiztegia: Gas, Euskaltzaindia
- ↑ «Enlaces Moleculares» FÍSICA MODERNA (Noiz kontsultatua: 2023-04-17).
- ↑ a b (Gaztelaniaz) Alejandrina, GALLEGO PICÓ; María, GARCINUÑO MARTÍNEZ Rosa; José, MORCILLO ORTEGA Mª; Ángel, VÁZQUEZ SEGURA Miguel. (2013-12-04). QUÍMICA BÁSICA. UNED ISBN 978-84-362-6784-6. (Noiz kontsultatua: 2023-04-17).
- ↑ «Fuerza Gravitatoria» www.fisicalab.com (Noiz kontsultatua: 2023-04-17).
- ↑ (Gaztelaniaz) «Estado Gaseoso - EcuRed» www.ecured.cu (Noiz kontsultatua: 2023-04-17).
- ↑ (Gaztelaniaz) Giancoli, Douglas C.. (2005). Physics: Principles with Applications. Pearson Educación ISBN 978-970-26-0695-6. (Noiz kontsultatua: 2023-04-17).
- ↑ Anderson, 501. or.
- ↑ John, James (1984). Gas Dynamics. Allyn and Bacon. ISBN 978-0-205-08014-4
- ↑ a b c John, James (1984). Gas Dynamics. Allyn and Bacon. ISBN 978-0-205-08014-4
























