Rodentia
Rongeurs, Rodentiens
| Règne | Animalia |
|---|---|
| Embranchement | Chordata |
| Sous-embr. | Vertebrata |
| Super-classe | Tetrapoda |
| Classe | Mammalia |
| Sous-classe | Theria |
| Infra-classe | Placentalia |
| Super-ordre | Euarchontoglires |
Sous-ordres de rang inférieur
Les rongeurs ou Rodentiens (Rodentia) sont un ordre de mammifères placentaires (le plus grand ordre de mammifères, regroupant plus de 2 000 espèces). Ces animaux se caractérisent par leur unique paire d'incisives à croissance continue sur chacune de leurs mâchoires (ce qui les distingue des Lagomorphes), qui leur servent à ronger leur nourriture, à creuser des galeries ou à se défendre. Le reste de leur morphologie est relativement variable, mais la majorité des espèces sont de petite taille, avec un corps trapu, des pattes courtes et une longue queue. La plupart des rongeurs se nourrissent de graines ou d'autres matières végétales, mais d'autres ont des régimes alimentaires plus variés. Ce sont souvent des animaux sociaux et beaucoup d'espèces vivent en communauté au sein desquelles les individus interagissent et communiquent entre eux de façon complexe. Le mode de reproduction peut être monogame, polygyne ou avec promiscuité sexuelle. De nombreuses espèces ont des portées de petits peu développés et dépendants, quand d'autres donnent directement naissance à des jeunes déjà relativement bien développés.
Les rongeurs forment un groupe très diversifié, présent sur tous les continents à l'exception de l'Antarctique. C'est le seul ordre de mammifères placentaires à avoir colonisé l'Australie sans l'intervention humaine. Ils se sont adaptés à de très nombreux habitats terrestres, dont ceux anthropisés, et certaines espèces sont arboricoles, fouisseuses ou semi-aquatiques. L'ordre des Rodentia représente près de quarante pour cent des espèces de mammifères, ce qui en fait le plus diversifié devant celui des chauves-souris (Chiroptera). Parmi les espèces les plus connues de ce groupe sont les souris, les rats, les écureuils, les chiens de prairie, les porcs-épics, les castors, les cochons d'Inde et les hamsters. D'autres animaux tels que les lapins, les lièvres et les pikas, qui peuvent être pris pour des rongeurs et qui ont été placés dans cet ordre par le passé, constituent désormais l'ordre des Lagomorpha. Les données fossiles disponibles sur les rongeurs remontent jusqu'au Paléocène en Laurasia. Ce groupe connaît une grande diversification au cours de l'Éocène et se disperse sur tous les continents, parfois même en traversant les océans et rejoignant ainsi l'Amérique du Sud et Madagascar depuis l'Afrique.
Les rongeurs sont utilisés en tant que source de nourriture, pour la confection de vêtements, en tant qu'animaux de compagnie ou de laboratoire. Certaines espèces, comme le Surmulot (Rattus norvegicus), le rat noir (Rattus rattus) ou la souris grise (Mus musculus) sont de sévères ravageurs, mangeant ou dégradant les stocks de nourriture humains, ou agissant comme vecteurs de parasites (poux, tiques…) et de maladies infectieuses, souvent zoonotiques (touchant à la fois l'homme et l'animal)[1]. Les espèces de rongeurs introduites par accident deviennent souvent envahissantes, menaçant la survie d'espèces indigènes. C'est notamment le cas de nombreux oiseaux insulaires, auparavant privés de prédateurs et dont les couvées peuvent être prédatées.
Description
Crâne
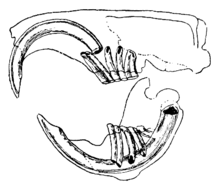
Les rongeurs se caractérisent par l'existence d'une unique paire d'incisives, acérées et à croissance continue, sur chacune de leurs mâchoires[2]. Ces dents sont munies d'épaisses couches d'émail sur l'avant, mais le sont peu sur l'envers[3]. Leur croissance ne cessant jamais, c'est leur usure perpétuelle qui leur évite de ne trop croître, et ainsi d'atteindre ou même de percer le crâne. Comme les incisives s'aiguisent les unes contre les autres, la dentine à l'arrière des dents s'use, ne laissant que l'émail, solide, taillé comme un ciseau[4]. La plupart des espèces ont jusqu'à 22 dents, sans canines ni prémolaires antérieures. Il y a un écart, ou diastème, entre les incisives et les molaires chez la plupart des espèces. Cela leur permet d'aspirer leurs joues ou leurs lèvres et protéger leur cavité buccale de copeaux de bois ou d'autres matières non comestibles, et de se débarrasser de ces déchets par les côtés de leur bouche[5]. Les chinchillas et les cobayes ont une alimentation riche en fibres, et leurs molaires n'ont pas de racines mais ont une croissance continue comme les incisives[6].
Chez beaucoup de rongeurs les molaires sont relativement grosses, très structurées et avec des cuspides ou des sillons très marqués, bien que chez d'autres, comme les espèces du genre Pseudohydromys, elles sont plus petites et plus simples. Les dents sont bien adaptées à broyer les aliments en petits morceaux[2]. La musculature de la mâchoire est forte. La mandibule est poussée vers l'avant pour ronger, et tirée vers l'arrière lors de la mastication[3]. Les différents groupes de rongeurs diffèrent, à la fois des autres mammifères et entre eux, par l'arrangement des muscles de leur mâchoire et par les structures du crâne associées à cette musculature. Les Sciuromorpha, qui comprennent les écureuils typiques, ont le faisceau profond de leur masséter particulièrement puissant, qui les rend efficaces pour mordre avec les incisives. Les Myomorpha, qui comprennent les souris, ont un muscle temporal élargi, qui leur permet de mastiquer puissamment avec les molaires. Le Hystricomorpha, comme les cochons d'Inde ou les porcs-épics, ont un faisceau superficiel de leur masséter plus grand et un faisceau profond plus petit que les souris ou les écureuils, les rendant peut-être moins efficaces à mordre avec les incisives, mais leur muscle ptérygoïdien intérieur plus puissant leur permet de bouger davantage leur mâchoire sur les côtés lors de la mastication[7].
Taille

Le plus petit rongeur existant est la gerboise Salpingotulus michaelis, qui mesure en moyenne 4,4 cm de longueur (tête et corps), avec des femelles adultes ne pesant que 3,75 g. La plupart des espèces de rongeurs pèsent moins de 100 g, mais le plus grand rongeur actuel, le Capybara (Hydrochoerus hydrochaeris), peut peser jusqu'à 66 kg. Du côté des taxons éteints, les ossements fossiles ont montré qu'il y a environ trois millions d'années vivait au sud de l'Amérique un rongeur bien plus grand (plus grand encore que Eumegamys paranensis ou que Phoberomys pattersoni, découvert au Venezuela et pouvant peser de 436 à 741 kg, précédents records en taille chez les rongeurs fossiles[8]) : Josephoartigasia monesi était aussi haut qu'un bison et pesait jusqu'à une tonne environ[9]. C'est le plus grand des rongeurs connus ayant vécu sur la Terre[10]. Plusieurs indices laissent à penser que sa mâchoire était dotée d'une force exceptionnelle[11],[12] (plus encore que celle du tigre ou du crocodile[13]). Ce rongeur géant pourrait avoir ressemblé au cochon d'Inde, mais de la taille d'un hippopotame[14].
La diversité des caractéristiques des rongeurs est grande, parfois même entre des espèces étroitement apparentées. Les caractéristiques de quelques espèces de rongeurs typiques sont données dans le tableau ci-dessous[15] :
| Espèce | Record de longévité (en années) † : en captivité |
Poids de l'adulte (en grammes) |
Durée de la gestation (en jours) |
Nombre de portées par an |
Nombre moyen de petits par portée (et extrêmes) |
|---|---|---|---|---|---|
| Souris grise (Mus musculus)[16] | 4,0† | 20 | 19 | 5,4 | 5,5 (3 à 12) |
| Rat-taupe nu (Heterocephalus glaber)[17] | 31,0 | 35 | 70 | 3,5 | 11,3 |
| Rat noir (Rattus rattus)[18] | 4,0† | 200 | 21 | 4,3 | 7,3 (6 à 12) |
| Rat brun (Rattus norvegicus)[19] | 3,8† | 300 | 21 | 3,7 | 9,9 (2 à 14) |
| Écureuil roux (Sciurus vulgaris)[20] | 14,8† | 600 | 38 | 2,0 | 5,0 (1 à 10) |
| Chinchilla à longue queue (Chinchilla lanigera)[21] | 17,2† | 642 | 111 | 2,0 | 2,0 (1 à 6) |
| Cochon d'Inde (Cavia porcellus)[22] | 12,0 | 728 | 68 | 5,0 | 3,8 (1 à 8) |
| Ragondin (Myocastor coypus)[23] | 8,5† | 7 850 | 131 | 2,4 | 5,8 (3 à 12) |
| Capybara (Hydrochoerus hydrochaeris)[24] | 15,1† | 55 000 | 150 | 1,3 | 4,0 (2 à 8) |
De nombreuses espèces de rongeurs présentent un dimorphisme sexuel. Chez certaines, les mâles sont plus gros que les femelles tandis que chez d'autres c'est l'inverse. Les gros mâles sont typiques chez les écureuils terrestres, les rats kangourous, les rats-taupes solitaires et les gaufres à poche, et ce dimorphisme est probablement apparu par sélection sexuelle et par l'existence de combat entre mâles. Les grosses femelles sont trouvées chez les tamias et les souris sauteuses. On ne sait pas pourquoi ce phénomène se produit, mais chez le Tamia amène (Tamias amoenus) il se pourrait que les mâles choisissent les femelles plus grosses qui auraient un meilleur succès reproducteur. Chez certains rongeurs, comme les campagnols, le dimorphisme sexuel peut varier d'une population à une autre. Chez le Campagnol roussâtre (Myodes glareolus), les femelles sont généralement plus grosses que les mâles, mais c'est l'inverse qui se produit chez les populations alpines, peut-être en raison du manque de prédateurs et des compétitions plus marquées entre mâles[25].
Morphologie générale

Les différents groupes de rongeurs ont des morphologies très variables, mais ont généralement des corps massifs, trapus avec des pattes courtes[2]. Les membres antérieurs ont généralement cinq doigts, dont un pouce opposable, tandis que les membres postérieurs ont trois à cinq doigts. Le coude donne à l'avant-bras une grande flexibilité[4]. La majorité des espèces sont plantigrades, marchant sur la sole de leurs pattes, et ont des ongles semblables à des griffes. Les ongles des espèces fouisseuses ont tendance à être longs et forts, tandis qu'ils sont plus courts et plus pointus chez les rongeurs arboricoles[26]. Les différentes espèces de rongeurs utilisent une grande variété de modes de locomotion, dont la marche quadrupède, la course, l'usage de galeries souterraines, la grimpe, le saut bipède (gerboises, rats-kangourous et souris sauteuses d'Australie), la natation ou même le vol plané. Les espèces de la famille des Anomaluridae et celles de la sous-famille des Pteromyinae, toutes appelées « écureuils volants », peuvent en effet planer d'arbre en arbre en utilisant des membranes qui s'étendent entre les membres antérieurs et postérieurs[27]. Les agoutis (Dasyprocta) sont des animaux rapides, étant munis d'ongles semblables à des sabots qu'ils utilisent en course digitigrade. La majorité des rongeurs sont munis de queues, qui peuvent être de formes et tailles variées. Certaines sont préhensiles, comme celle du Rat des moissons (Micromys minutus), et leur fourrure peut être touffue ou au contraire très réduite. Cet organe sert parfois à la communication, comme chez le castor qui claque sa queue sur la surface de l'eau ou la souris domestique qui l'ébranle pour signaler un danger. D'autres espèces ont des queues rudimentaires, ou pas de queue du tout[2]. Chez certaines espèces enfin, la queue est capable de régénération si elle est en partie coupée[4].
Sens et physiologie
Les rongeurs ont généralement les sens de l'odorat, de l'ouïe et de la vision bien développés. Les espèces nocturnes ont souvent de grands yeux et certaines sont sensibles à la lumière ultraviolette. De nombreuses espèces ont de longues vibrisses, qui leur servent à balayer l'environnement lors de la locomotion (avec des mouvements d'avant en arrière, le whisking). Certains rongeurs ont des abajoues, qui peuvent être doublées de fourrure. Chez de nombreuses espèces, la langue ne peut pas aller plus loin que les incisives. Le système digestif des rongeurs est efficace, absorbant près de 80 pour cent de l'énergie ingérée. Lorsqu'un rongeur consomme de la cellulose, la nourriture est d'abord prédigérée dans l'estomac puis passe dans le cæcum, où des bactéries la réduisent en glucides. Le rongeur pratique alors la coprophagie, consommant ses propres pelotes fécales, de sorte que les nutriments peuvent ensuite être absorbés par l'intestin. Ils produisent donc souvent des crottes dures et sèches[2]. Chez de nombreuses espèces, le pénis contient un os, le baculum. Les testicules peuvent être situés sur l'abdomen ou à l'aine[4].
Écologie et comportement
Alimentation

La plupart des rongeurs sont herbivores, se nourrissant exclusivement de graines, de tiges, de feuilles, de fleurs ou de racines. D'autres sont omnivores, et quelques-uns sont prédateurs[3]. Le Campagnol agreste (Microtus agrestis) est un exemple typique d'espèce herbivore, se nourrissant d'herbe, de tubercules, de mousses et d'autres végétaux. Il ronge de l'écorce au cours de l'hiver, et consomme occasionnellement des invertébrés comme des larves d'insectes[28]. Le Gaufre brun (Geomys bursarius) mange des végétaux trouvés sous terre lorsqu'il creuse des galeries, et collecte aussi de l'herbe, des racines et des tubercules dans ses abajoues et qu'il cache dans des chambres souterraines[29]. Le gaufre à poche Geomys personatus évite de sortir à la surface pour se nourrir, attrapant les racines de plantes avec ses mâchoires et les tirant vers le bas creusé dans son terrier. Il pratique aussi la coprophagie[30]. Le Cricétome de forêt (Cricetomys emini) cherche sa nourriture à la surface, collectant tout ce qui est comestible dans ses grosses abajoues, et ramène le tout dans son terrier pour le consommer[31].

Les agoutis (Dasyprocta sp.) sont des rares animaux qui arrivent à ouvrir les fruits du Noyer d'Amazonie (Bertholletia excelsa). Chaque fruit contenant de nombreuses noix, l'animal ne les consomme pas en une fois mais les transporte et les cache, aidant à la dispersion des graines qu'il ne retrouve pas. D'autres arbres à noix produisent de très nombreux fruits en automne, qui sont stockés dans des trous ou des crevasses par les écureuils. Dans certaines régions arides, les graines sont souvent disponibles pour de courtes périodes, et les rats-kangourous en collectent autant qu'ils peuvent pour les stocker dans des chambres souterraines[31]. Une autre stratégie pour tirer parti des abondances saisonnières sont les réserves de graisse. Elle est par exemple utilisée par les marmottes (Marmotta sp.), qui peuvent être de 50 % plus lourdes à l'automne qu'au printemps, utilisant leurs réserves durant leur longue hibernation[31]. Les castors se nourrissent de feuilles, de bourgeons et de l'écorce interne des arbres en croissance, ainsi que de plantes aquatiques. Durant l'automne, ces rongeurs coupent de petits arbres et des branches feuillues, et les immergent dans leur étang en plantant une extrémité dans la boue pour les fixer. L'hiver, ils peuvent accéder à ces réserves, même lorsque l'eau est gelée en surface[32].
Bien que les rongeurs ont par le passé été considérés comme des herbivores, un certain nombre d'espèces se montrent opportunistes et consomment à l'occasion des insectes, du poisson ou de la viande, et d'autres plus spécialisées ont besoin de ces ressources dans leur régime alimentaire. Une étude morphologique et fonctionnelle de la dentition des rongeurs suggère que les rongeurs primitifs étaient omnivores plutôt qu'herbivores. D'autres études montrent que de nombreuses espèces des sous-ordres des Sciuromorpha et des Myomorpha, et quelques membres des Hystricomorpha, incorporent naturellement de la matière animale dans leur régime alimentaire ou la consomme volontiers si ces aliments leur sont donnés en captivité. L'examen du contenu stomacal de Souris à pattes blanches (Peromyscus leucopus) en Amérique du Nord, espèce normalement considérée comme herbivore, a montré que la matière animale constituait 34 % de l'alimentation[33]. Parmi les rongeurs carnivores plus spécialisés, on compte les espèces du genre Rhynchomys aux Philippines, qui se nourrissent d'insectes et d'invertébrés mous, et le Rat d'eau australien (Hydromys chrysogaster), qui consomme des insectes aquatiques, des poissons, des crustacés, des moules, des escargots, des grenouilles, des œufs d'oiseaux et des oiseaux aquatiques[33],[34]. La Souris sauterelle (Onychomys leucogaster), qui peuple les régions sèches de l'Amérique du Nord, se nourrit d'insectes, de scorpions ou d'autres petites souris, et seulement un peu de matière végétale. Son corps est trapu et ses pattes et queue courtes, mais elle est agile et peut facilement maîtriser des proies aussi grandes qu'elle[35].
Comportement social


Les rongeurs présentent une multitude d'organisations sociales, allant du système de castes du Rat-taupe nu (Heterocephalus glaber), un des seuls cas connus d'eusocialité chez les mammifères[36], aux colonies denses des chiens de prairie partageant de grands réseaux de galeries (appelés « villes »)[37], en passant par les groupes familiaux ou le mode de vie solitaire du Loir gris (Glis glis). Si les loirs adultes peuvent avoir des zones d'alimentation se chevauchant, ils vivent dans des nids différents et se nourrissent séparément, les rencontres n'ayant lieu que pour la reproduction. Les gaufres à poche (Geomyidae) mènent aussi une vie solitaire en dehors de la saison de reproduction, chaque individu creusant son propre réseau de galerie et défendant son territoire[26].
Les gros rongeurs ont tendance à vivre en groupes familiaux au sein desquels les parents vivent avec leur progéniture jusqu'à ce que celle-ci se disperse. Les castors vivent en familles élargies, comptant généralement avec un couple d'adultes, les jeunes de l'année, ceux de l'année précédente et parfois d'années antérieures[38]. Le Rat brun vit généralement en petites colonies, avec jusqu'à six femelles partageant un terrier et un mâle défendant un territoire autour de celui-ci. Quand les densités de rats sont élevées, ce système est abandonné et les mâles utilisent un système hiérarchique de domination, avec des territoires qui se chevauchent. La progéniture femelle reste dans la colonie tandis que les jeunes mâles se dispersent[39]. Le Campagnol des Prairies (Microtus ochrogaster) est monogame et forme un couple uni pour la vie. En dehors de la saison de reproduction, il vit en proximité d'autres congénères en petites colonies. Un mâle n'est pas agressif envers les autres mâles jusqu'à ce qu'il se soit accouplé, après quoi il défend un territoire, une femelle et un nid contre les autres mâles. Les deux partenaires se blottissent l'un contre l'autre, se toilettent mutuellement, et participent ensemble à l'élevage des jeunes[40].
Les écureuils terrestres, comme les marmottes, figurent parmi les rongeurs les plus sociaux. Ils forment généralement des colonies de femelles apparentées, les mâles se dispersant après le sevrage pour mener une vie nomade. Les animaux d'une colonie peuvent coopérer à différents niveaux, en s'avertissant par des cris d'alarme, en défendant un territoire commun, en partageant leur nourriture ou en protégeant les zones de mise bas et les jeunes[38]. Le Chien de prairie à queue noire (Cynomys ludovicianus) forme des « villes » pouvant couvrir plusieurs hectares. Les galeries les composant ne sont pas interconnectées mais sont creusées et occupées par des familles territoriales appelées « coteries ». Ces dernières sont généralement constituées d'un mâle adulte, de trois ou quatre femelles adultes, de plusieurs jeunes non-reproducteurs et des petits de l'année. Les membres d'une coterie interagissent paisiblement entre eux mais se montrent hostiles aux membres externes[37].
Les exemples de comportement colonial des plus extrêmes chez les rongeurs sont probablement ceux des rongeurs eusociaux que sont le Rat-taupe nu (Heterocephalus glaber) et le Rat-taupe de Damaraland (Cryptomys damarensis). Le premier vit entièrement sous terre et peut former des colonies comptant jusqu'à 80 individus. Seule une femelle et jusqu'à trois mâles s'y reproduisent, tandis que les autres membres de la colonie sont plus petits, stériles et ont la fonction d'ouvriers. Certains individus sont de taille intermédiaire, et aident à l'élevage des jeunes et peuvent prendre la place des reproducteurs si l'un d'eux meurt[36]. Chez le Rat-taupe de Damaraland, il n'y a qu'un couple reproducteur. Les autres individus ne sont pas complètement stériles, mais ne deviennent fertiles que s'ils forment leur propre colonie[41].
Communication
Olfaction

Les rongeurs utilisent le marquage sensoriel dans divers contextes sociaux, comme la communication inter- et intra-spécifique, le marquage des passages et l'établissement de territoires. Leur urine donne des informations génétiques aux autres individus de l'espèce, comme le sexe ou l'identité, et des informations métaboliques sur le statut de dominance, le statut de reproduction et la santé. Des composés dérivés du complexe majeur d'histocompatibilité (CMH) sont liés à plusieurs protéines urinaires. L'odeur d'une prédateur conduit à réduire ce comportement de marquage sensoriel[42].
Les rongeurs sont capables de reconnaître des individus qui leur sont apparentés par l'odeur, et cela leur permet de se comporter plus favorablement envers leurs proches (« népotisme ») et d'éviter la consanguinité. Les animaux reconnaissent ainsi leurs proches par des signaux olfactifs à partir de l'urine, des fèces et des sécrétions glandulaires. Le principal facteur de détermination implique le CMH, puisque le degré de parenté entre deux individus est corrélé avec les gènes CMH qu'ils ont en commun. Dans la communication entre animaux qui ne sont pas apparentés, des marqueurs olfactifs plus permanents sont nécessaires, comme au niveau des limites de territoire, avec des protéines urinaires majeures non volatiles, dont la fonction de transporteurs de phéromones peut également être utilisée. Ces protéines urinaires majeures peuvent aussi indiquer l'identité de chaque individu, chaque mâle de Souris grise excrétant dans son urine une combinaison de 12 protéines spécifique à l'animal[43].
Les Souris domestiques déposent leur urine, qui contient des phéromones, pour marquer leur territoire, reconnaître les individus et pour des raisons d'organisation sociale. Cela peut prendre différentes formes[44] :
- l'effet Bruce : les phéromones d'un mâle adulte étranger conduisent à l'avortement de la femelle gestante[44],[45] ;
- l'effet Whitten : les phéromones de mâles familiers synchronisent les œstrus dans une population de femelles[44],[45] ;
- l'effet Vandenbergh : les phéromones de mâles matures extérieurs provoquent une entrée en œstrus précoce chez la souris femelle prépubère[44],[45] ;
- l'effet Lee–Boot : les phéromones de femelles matures provoquent le ralentissement voire l'arrêt des cycles œstraux des autres souris femelles quand elles sont maintenues en groupes et isolées des mâles[44],[45].
Des rongeurs territoriaux comme les castors ou les Écureuils roux (Sciurus vulgaris) analysent et s'habituent aux odeurs de leurs voisins et sont moins agressifs envers leurs intrusions qu'envers celles d'animaux errants ou étrangers[46],[47].
Ouïe

Plusieurs espèces de rongeurs, particulièrement celles qui sont diurnes et sociales, ont une large gamme de cris d'alarme qui sont émis quand ils perçoivent des menaces. Ces cris ont des bénéfices directs comme indirects. Ainsi, un prédateur potentiel peut s'arrêter à l'écoute de ce cri, considérant qu'il est repéré, et l'alarme ainsi donnée peut conduire les congénères de l'animal le produisant à se cacher pour éviter le danger[48]. Plusieurs espèces, par exemple les chiens de prairies, ont un système de cris d'alerte complexe. Ces espèces peuvent employer des cris différents suivant le prédateur (un cri pour les prédateurs terrestres et un pour les prédateurs aériens par exemple) et chacun donne des informations sur la nature exacte de la menace[49]. L'urgence de la menace peut également être indiquée par les propriétés acoustiques du cri[50].
Les rongeurs sociaux ont une plus large gamme de vocalisations que les espèces solitaires. Quinze différents cris d'alarme ont été reconnus chez l'adulte rat-taupe Fukomys micklemi et quatre chez les jeunes[51]. De la même manière, l'octodon, un autre rongeur social, qui creuse des terriers, a une vaste palette de moyens de communication et un répertoire vocal élaboré comprenant 15 différentes catégories de sons[52]. Les ultrasons jouent un rôle dans la communication des loirs et sont utilisés quand les individus sont hors de vue les uns des autres[53].
Les Souris grises utilisent à la fois des cris audibles et des ultrasons suivant le contexte. Les cris audibles peuvent généralement être entendus lors d'échanges agressifs, tandis que les ultrasons sont utilisés dans la communication sexuelle ainsi que par les jeunes quand ils tombent de leur nid[44].
Les rats de laboratoires (qui sont des Rats bruns, Rattus norvegicus) émettent des courtes vocalisations ultrasoniques à de hautes fréquences durant des expériences supposées agréables pour l'animal comme lorsqu'on lui administre une dose de morphine, lors de l'accouplement ou lorsqu'il est chatouillé. Le cri, décrit comme un « gazouillis » caractéristique, est comparé à un rire, et est interprété comme l'attente de quelque chose de bon. Dans des études cliniques, le « gazouillis » est associé à des sentiments positifs, et les liens sociaux naissent avec les chatouilles, qui sont donc recherchées par les rats. Toutefois au fur et à mesure que les rats vieillissent, ils sont de moins en moins enclins à « gazouiller ». Comme la plupart des vocalisations des rats, le « gazouillis » se fait à des fréquences trop hautes pour que les humains les entendent sans équipement spécial, et un récepteur approprié est donc utilisé pour ce type d'études[54].
Il a été démontré que le Rat brun pouvait utiliser les ultrasons pour faire de l'écholocation[44]. La gamme de fréquences écoutée par les rongeurs diffère entre les espèces. Le tableau ci-dessous montre la gamme entendue par différentes espèces[55].
| Espèce | Limite inférieure (Hz) | Limite supérieure(Hz) | Cris spécifiques |
|---|---|---|---|
| Homme | 64 | 23 000 | |
| Rat | 200 | 76 000 | Cri de « plaisir » ultrasonique émis à 50 kHz |
| Souris | 1 000 | 91 000 | Cri de détresse des jeunes émis à 40 kHz |
| Gerbille | 100 | 60 000 | |
| Cochon d'Inde | 54 | 50 000 | |
| Chinchilla | 90 | 22 800 |
Vue
Les rongeurs, comme les autres mammifères placentaires à l'exception des primates, ont deux types de cônes pour capter la lumière au niveau de leur rétine[56], des cônes S sensibles aux courtes longueurs d'onde qui permettent de percevoir la couleur bleue et des cônes M qui possèdent un photopigment sensible aux moyennes longueurs d'onde et permettent de capter la couleur verte. Ce sont donc des animaux dichromates. Toutefois, ils sont sensibles au spectre ultraviolet, et c'est pourquoi ils peuvent voir des choses que l'Homme ne voit pas. Le rôle de cette sensibilité aux ultraviolets n'est pas toujours clairement connu. Chez les octodons, par exemple, le ventre reflète plus de lumière ultraviolette que le dos. C'est pourquoi, quand un octodon se dresse sur ses pattes arrière, ce qu'il fait en cas d'alerte, il expose son ventre aux autres octodons et la vision ultraviolette pourrait servir à communiquer l'alarme. Quand il se tient à quatre pattes, sa faible réflectance des rayons ultraviolets pourrait le rendre moins visible pour les prédateurs[57]. La lumière ultraviolette est abondante durant la journée mais pas la nuit. Il y a une forte augmentation du taux de rayons ultraviolets par rapport à la lumière visible à l'aube et au crépuscule. Certains rongeurs sont particulièrement actifs à ces heures de la journée, et la sensibilité aux ultraviolets leur donne alors un avantage[58].
L'urine de plusieurs rongeurs (par exemple les campagnols, les octodons, les rats et les souris) reflète fortement la lumière ultraviolette et cela pourrait être un moyen de communication laissant un marquage à la fois visuel et olfactif[59]. Toutefois, la quantité d'ultraviolets reflétée diminue avec le temps, ce qui dans certaines circonstances peut constituer un désavantage pour les animaux ; le Faucon crécerelle (Falco tinnunculus) peut faire la différence entre un passage récent de rongeur et un passage plus ancien, ce qui lui donne un avantage lorsqu'il chasse[60].
Toucher

Les vibrations émises par certaines espèces sur le sol peuvent informer leurs congénères sur certains de leurs comportements. Le rat-taupe Nannospalax ehrenbergi est le premier mammifère pour lequel la communication par vibrations a été observée. Ce rongeur fouisseur cogne sa tête contre les parois de ses tunnels. Ce comportement, que l'on pensait tout d'abord faire partie du processus de construction du tunnel, génère des signaux utiles pour la communication avec d'autres rats-taupes sur de longues distances[61].
Certains rongeurs frappent le sol avec leurs pattes pour alerter de la présence d'un prédateur ou pour se défendre. Ce comportement est principalement utilisé par des rongeurs fouisseurs ou semi-fouisseurs[62]. Dipodomys spectabilis émet de cette manière différents types de bruits en frappant le sol avec ses pattes, l'un d'eux servant par exemple en cas de rencontre avec un serpent. Ce bruit peut alerter les congénères et la progéniture de celui qui donne l'alerte, mais repousse de lui-même le prédateur, qui comprend qu'il est repéré[61],[63]. Plusieurs études ont montré l'utilisation délibérée des vibrations du sol comme moyen de communication durant la parade nuptiale chez le Rat-taupe du Cap (Georychus capensis)[64].
Stratégies reproductrices

Certaines espèces de rongeurs sont monogames, un mâle et une femelle formant un couple qui dure dans le temps. La monogamie peut être obligatoire ou facultative. Dans le premier cas, les deux parents s’occupent de la progéniture, et jouent un rôle important de la survie des jeunes. C’est par exemple le cas chez la Souris de Californie, la Souris de plage, le Rat sauteur géant de Madagascar et les castors. Dans ces espèces, les mâles se reproduisent généralement exclusivement avec leurs partenaires. En plus de permettre une attention plus importante apportée aux jeunes, ce type de monogamie profite aux mâles en leur évitant de rester trop longtemps sans trouver de partenaire, ou de se reproduire avec une femelle infertile. Dans le cas de la monogamie facultative, les mâles ne s’occupent pas directement des jeunes mais ils restent avec la même femelle car ils n’ont pas accès aux autres du fait d’une grande dispersion des animaux. Les Campagnols des prairies constituent un exemple caractéristique de ce type de monogamie, les mâles défendant et gardant les femelles situées à proximité d’eux[65].
Chez les espèces polygames, les mâles essaient de monopoliser et de s’accoupler avec plusieurs femelles. Comme pour la monogamie, on en observe deux formes, une incluant la défense d’un territoire et des femelles l’occupant et l’autre non. Dans le premier cas, les mâles occupent des territoires qui contiennent des ressources susceptibles d’attirer les femelles. C’est le cas notamment chez les espèces de la tribu des Marmotini comme la Marmotte à ventre jaune, le Spermophile de Californie, le Spermophile du Columbia et le Spermophile de Richardson. Dans le cas des marmottes, les mâles qui détiennent un territoire le perdent rarement, et remportent leurs combats contre ceux qui tentent de s’en emparer. Certaines espèces défendent directement les femelles présentes sur leur territoire, et les combats qui s’ensuivent peuvent causer d’importantes blessures. Chez les espèces polygames qui ne défendent pas de territoire, les mâles ne sont pas territoriaux et errent à la recherche de femelles. Ces mâles établissent des hiérarchies entre eux, le mâle le plus dominant ayant accès au plus grand nombre de femelles. C’est le cas chez des espèces comme le Spermophile de Belding et certains écureuils arboricoles[65].

Enfin, chez d’autres espèces, mâles et femelles ont des partenaires multiples. Chez des espèces comme la Souris à pattes blanches, les femelles donnent naissance à des portées d’animaux ayant différents pères. Ce type de comportement conduit à une plus grande compétition spermatique et les mâles tendent à avoir de plus grands testicules. Chez l'Écureuil de terre du Cap, les testicules du mâle peuvent représenter 20 % de la longueur de son corps (queue exclue)[65]. Plusieurs espèces de rongeurs ont des systèmes de reproduction qui peuvent varier entre les différents types de comportements cités auparavant : monogamie, polygamie et promiscuité[65].
Les femelles rongeurs jouent un rôle actif dans le choix de leur partenaire. Leur préférence se fait suivant différents critères, qui peuvent comprendre la taille, la dominance et la taille du territoire du mâle[66]. Chez les Rats-taupes nus, une seule femelle s'accouple avec au moins trois mâles[36].
Pour la plupart des espèces de rongeurs, comme les Rats bruns et les Souris communes, l’ovulation a lieu à cycles réguliers, tandis que pour d’autres, comme les campagnols, elle est induite par la copulation. Durant l'accouplement, les mâles de certaines espèces de rongeurs déposent un bouchon spermatique dans les voies génitales de la femelle, à la fois pour éviter la fuite de sperme et pour prévenir le fait que d’autres mâles pourraient ensuite inséminer la femelle. Les femelles peuvent retirer ce bouchon, mais doivent pour cela le faire immédiatement ou après quelques heures[66].
Naissance et élevage des jeunes

Les rongeurs peuvent naître nidicoles (aveugles, sans poils et relativement peu développés) ou nidifuges (en partie munis de fourrure, les yeux ouverts et assez bien développés) selon l’espèce. Le stade nidicole est caractéristique des écureuils et des souris, tandis que les cochons d’Inde et les porcs-épics sont nidifuges. Les femelles qui ont des jeunes nidicoles construisent généralement des nids bien aménagés avant de donner naissance à leur progéniture, et les maintiennent jusqu’au sevrage de celle-ci. La femelle donne naissance à ses petits en position assise ou couchée, et les nouveau-nés naissent dans la direction vers laquelle elle regarde. Les nouveau-nés sortent pour la première fois du nid quelques jours après avoir ouvert leurs yeux et dans un premier temps ils y retournent très régulièrement. Au fur et à mesure qu’ils grandissent, ils rentrent de moins en moins souvent au nid, avant de le quitter définitivement au moment du sevrage[67].
Chez les espèces nidifuges, les femelles ne construisent qu’un nid sommaire, voire pas de nid du tout. La femelle donne naissance à ses petits en se tenant debout, et ceux-ci naissent derrière elle. Elle garde contact avec ses petits qui sont déjà très mobiles par de petits cris caractéristiques. Bien que relativement indépendants et pouvant être sevrés au bout de quelques jours, les jeunes peuvent continuer à être soignés et nourris par leur mère un peu plus longtemps. La taille des portées chez les rongeurs varient beaucoup, et de façon générale les femelles avec de petites portées passent plus de temps dans le nid que celles qui ont de grandes portées[67].

Les femelles rongeurs s’occupent de leurs petits directement en les allaitant, les soignant et les récupérant quand ils sortent du nid, et indirectement en attrapant de la nourriture, bâtissant le nid et les protégeant[67]. Chez plusieurs espèces sociales, les jeunes peuvent être élevés par des animaux autres que leurs parents, une pratique connue sous le nom de reproduction communautaire. C’est notamment le cas chez le Chien de prairie à queue noire et le Spermophile de Belding, où les femelles ont des nids communs et ne font pas la différence entre leurs petits et les autres. On ne sait pas réellement si les femelles peuvent distinguer leur propre progéniture dans ce cas. Dans le cas du Mara, les jeunes sont aussi placés dans des garennes communes, mais les femelles n’allaitent pas les petits qui ne sont pas issus de leur portée[68].
Les infanticides existent chez diverses espèces de rongeurs et peuvent être causés par des congénères adultes des deux sexes. Plusieurs raisons peuvent expliquer ce comportement, parmi lesquelles un stress nutritionnel, la compétition pour les ressources et, dans les cas des mâles, permettre à la femelle de devenir réceptive sexuellement plus rapidement. Cette dernière raison, si elle est largement reconnue chez les primates et les lions, ne fait pas l’unanimité pour les rongeurs[69]. Les infanticides sont très fréquents chez les Chiens de prairie à queue noire, et sont notamment le fait de mâles envahissant le territoire, ou de femelles s’y installant, mais peuvent aussi prendre la forme d’un cannibalisme de leur propre progéniture[70]. Pour se prémunir des infanticides par les autres adultes, les femelles rongeurs peuvent éviter ou attaquer directement les adultes potentiellement dangereux pour leur portée, s’accoupler avec différents mâles ou défendre leur territoire[69]. Des fœticides peuvent également avoir lieu chez les rongeurs ; chez la Marmotte des Alpes, les femelles dominantes ont tendance à empêcher le bon déroulement du cycle de reproduction de leurs subordonnées en les agressant alors qu’elles sont en gestation. Le stress qui en résulte cause parfois l’avortement du fœtus[71].
Cognition
Distribution et habitat

Les rongeurs sont l'un des groupes de mammifères les plus répandus, étant présents sur tous les continents à l'exception de l'Antarctique. Ils sont les seuls mammifères placentaires terrestres qui aient colonisé l'Australie et la Nouvelle-Guinée sans l'intervention humaine. L'humain a cependant introduit des espèces, comme le Rat polynésien (Rattus exulans), sur de nombreuses îles océaniques isolées[4]. Les rongeurs se sont adaptés à presque tous les habitats terrestres, de la toundra froide (où ils peuvent vivre sous la neige) aux déserts chauds. Certaines espèces comme les écureuils et les porcs-épics du Nouveau Monde sont arboricoles, tandis que d'autres, tels que les gaufres à poche et les rats-taupes, mènent une vie presque entièrement souterraine, où ils construisent des réseaux de galeries complexes. D'autres vivent sur la surface, mais ont un terrier dans lequel ils peuvent se retirer. Les castors et les rats musqués sont semi-aquatiques[2], mais le rongeur le plus adapté à la vie aquatique est probablement le rat Crossomys moncktoni de Nouvelle-Guinée[72]. Les rongeurs prospèrent également dans certains environnements créés par l'homme, tels que les zones cultivées et urbaines[73].

Bien que certaines espèces soient des nuisibles pour l'humain, les rongeurs jouent aussi un rôle écologique important[2], et certains rongeurs sont considérés comme des espèces clé de voûte ou ingénieures de leurs habitats respectifs. Dans les Grandes Plaines d'Amérique du Nord, les terriers des chiens de prairie jouent un rôle important dans l'aération du sol et dans la redistribution des éléments nutritifs, augmentant la teneur en matière organique du sol ainsi que l'absorption d'eau. Ils maintiennent ces prairies[74], et quelques grands herbivores comme le Bison d'Amérique du Nord (Bison bison) et l'Antilope d'Amérique (Antilocapra americana) préfèrent paître près des colonies de chiens de prairie en raison de la qualité nutritionnelle accrue des pâturages[75]. Les chiens de prairie peuvent toutefois également contribuer à la perte de la biodiversité locale et régionale, par leur déprédation des semences et la création et la propagation d'arbustes envahissants[74]. Les terriers des rongeurs peuvent manger les sporophores de champignons et propager leurs spores dans leurs excréments, ce qui permet aux champignons de se disperser et de former des relations symbiotiques avec les racines des plantes (qui, généralement, ne peuvent pas prospérer sans eux). Ainsi, ces rongeurs peuvent jouer un rôle dans le maintien de forêts saines[76]. Dans de nombreuses régions tempérées, les castors jouent un rôle essentiel pour l'hydrologie, leurs constructions de barrages et huttes modifiant le cours des ruisseaux et rivières[77], et en générant de grandes zones humides. Une étude a estimé que l'action des castors augmentait d'un tiers le nombre d'espèces de plantes herbacées à proximité des rivières[78], une autre que la présence des castors augmentait les effectifs de populations de saumons sauvages[79].
Classification





D'après Carleton (1984), il existe plus de 2000 espèces vivantes classées en 30 familles, mais aujourd'hui au XXIe siècle, il n'y en a plus qu'un peu plus de 1700[80].
Classification selon Mammal Species of the World
Liste de sous-ordres et familles selon Mammal Species of the World (version 3, 2005) (8 octobre 2012)[81] :
- sous-ordre Anomaluromorpha
- famille Anomaluridae — écureuils volants
- famille Pedetidae — lièvre sauteur
- sous-ordre Castorimorpha
- famille Castoridae — castors
- famille Geomyidae — gaufres à poche
- famille Heteromyidae — souris-kangourous et souris à poche épineuse
- sous-ordre Hystricomorpha
- infra-ordre Ctenodactylomorphi
- famille Ctenodactylidae — goundis
- infra-ordre Hystricognathi
- famille Abrocomidae — rats-chinchillas
- famille Bathyergidae — rats-taupes

- famille Capromyidae — hutias
- famille Caviidae — cobayes
- famille Chinchillidae — chinchillas et viscaches

- famille Ctenomyidae — Tuco-tuco
- famille Cuniculidae — pacas
- famille Dasyproctidae — agoutis et acouchis
- famille Dinomyidae — pacarana et espèces éteintes
- famille Echimyidae — rats épineux
 et, selon certains auteurs, le ragondin
et, selon certains auteurs, le ragondin - famille Erethizontidae — porcs-épics du nouveau monde
- famille Heptaxodontidae — hutias géants (éteints)
- famille Hystricidae — Porcs-épics de l'ancien monde
- famille Myocastoridae — ragondin
- famille Octodontidae — octodons, chozchoz, coruro, rat-viscache roux d'Argentine et des rats des rochers

- famille Petromuridae — rat des rochers

- famille Thryonomyidae — aulacode
- infra-ordre Ctenodactylomorphi
- sous-ordre Myomorpha
- super-famille Dipodoidea
- super-famille Muroidea
- famille Platacanthomyidae — loirs orientaux, loirs épineux
- famille Spalacidae — rats et rats-taupes
- famille Calomyscidae — hamsters souriciformes
- famille Nesomyidae — rats
- famille Cricetidae — campagnols, lemmings, souris, rats et hamsters
- famille Muridae — rats, gerbilles, souris
- sous-ordre Sciuromorpha
- famille Aplodontiidae — Castor de montagne
- famille Gliridae — loirs, lérots, lérotins, muscardins et quelques souris
- famille Sciuridae — écureuils volants, écureuils, chiens de prairies, marmottes, spermophiles, tamias et diverses souris
Groupes fossiles
Selon Paleobiology Database (20 mars 2015)[82], l'ordre contient les groupes fossiles suivants :
- † Alagomyidae
- † Allomyidae
- † Anomalomyidae
- † Aplodontoidea
- † Archetypomyidae
- † Bandaomys
- † Cercolabidae
- † Cricetopidae
- † Ctenodactyloidea
- † Cylindrodontidae
- † Downsimys
- † Echinomyidae
- † Ectropomys
- † Eocardidae
- † Epeiromys
- † Eryomyidae
- † Floresomys
- † Griphomys
- † Ischyromyidae
- † Jimomys
- † Laredomyidae
- † Luribayomys
- † Marfilomys
- † Megacricetodontidae
- † Meliakrouniomys
- † Odontomysopidae
- † Paciculus
- † Pairomys
- † Paramyidae
- † Prolapsus
- † Promysopidae
- † Protoptychidae
- † Pseudoparamys
- † Quercymys
- † Sciuravidae
- † Siphneidae
- † Texomys
- † Theridomyoidea
- † Yuomyidae
- † Zamoramys
Les rongeurs et l'Homme
Sauvegarde

Les rongeurs ne sont pas l'ordre de mammifères le plus menacé, néanmoins 168 espèces appartenant à 126 genres sont dans une situation préoccupante[83] sans que cela n'attire l'attention du grand public. Comme 76 % des genres de rongeurs ne comprennent qu'une seule espèce, une large diversité phylogénétique peut disparaitre avec l'extinction de seulement quelques espèces. En l'absence de connaissances très précises sur les espèces menacées, les efforts de sauvegarde portent sur des taxa supérieurs (sur les familles plutôt que sur les espèces par exemple) et sur des zones géographiques à risque[83]. Plusieurs espèces d'Oryzomys ont disparu depuis le XIXe siècle, probablement du fait de la perte de leur habitat, et de l'introduction d'espèces invasives[84]. En Colombie, Sphiggurus vestitus n'a été observé que dans deux zones montagneuses dans les années 1920, tandis que Santamartamys rufodorsalis est connu uniquement aux abords de sa localité type sur la côte des Caraïbes, ces espèces sont donc particulièrement vulnérables[85]. La Species Survival Commission de l'UICN a écrit « Nous pouvons conclure avec certitude que plusieurs rongeurs sud-américains étaient sérieusement menacés, principalement du fait de perturbations environnementales et de la chasse intensive »[86].
Trois espèces de rongeurs commensales de l'Homme se sont dispersées au travers du monde en suivant les déplacements humains, notamment dans les bateaux au moment de la période des Grandes découvertes, causant divers dommages aux espèces locales[87]. Ce sont le Rat brun, le Rat noir et la Souris commune, et on peut également ajouter à cette liste le Rat polynésien (Rattus exulans) dans le Pacifique. Par exemple, après que le Rat noir arrive sur l'Île Lord Howe en 1918, plus de 40 % des espèces d'oiseaux terrestres de l'île, dont la sous-espèce de Rhipidure à collier endémique de l'île Rhipidura fuliginosa cervina[88], vont disparaître dans les 10 années suivantes. Des extinctions d'espèces similaires ont été observés sur les Îles Midway (1943) et la Grande île du cap Sud (1962). Les programmes de sauvegarde de nombreuses espèces insulaires passent par l'éradication de ces rongeurs nuisibles, notamment en utilisant des rodenticides anticoagulants comme le brodifacoum[87]. Cette méthode a été fructueuse sur l'île de Lundy au Royaume-Uni, où l'éradication d'environ 40 000 Rats bruns a permis aux populations de Puffin des Anglais et de Macareux moine d'augmenter à nouveau[89],[90].
Utilisation

Les Hommes utilisent depuis très longtemps les peaux d'animaux pour se vêtir, car le cuir est solide et la fourrure forme une couverture externe isolante[3]. Les peuples indigènes d'Amérique du Nord utilisent à cette fin les peaux de castors, les tannant et les cousant ensemble pour faire des robes. Les Européens apprécient particulièrement la qualité de ces dernières, et le commerce nord-américain de la fourrure se développe et prend une importance majeure pour les premiers colons. En Europe, la douce couche de poils de jarre connue comme « laine de castor » était considérée comme idéale pour fourrer les vêtements, et permettait également de faire des chapeaux[91],[92]. Plus tard, le ragondin devient une source de fourrure meilleur marché et est élevé en grand nombre en Amérique et en Europe. Le changement des modes et l'arrivée de nouveaux matériaux a conduit cette branche de l'industrie de la fourrure animale à régresser depuis[93]. Le chinchilla a une fourrure douce et soyeuse et la demande pour celle-ci est devenue tellement importante qu'il a failli totalement disparaître à l'état sauvage avant que son élevage ne se développe et devienne la principale source de peaux[93].
Au moins 89 espèces de rongeurs, la plupart appartenant aux Hystricomorpha comme le cochon d'Inde, les agoutis et les capybaras, sont consommés par l'Homme. En 1985, il y avait au moins 42 sociétés différentes dans lesquelles on mangeait les rats[94]. Les cochons d'Inde sont élevés pour la consommation humaine depuis très longtemps. Entre 2500 et 1500 av. J.-C., ils constituent la principale source de viande de l'empire Inca. Les loirs étaient élevés par les Romains dans des pots spéciaux appelés « gliraria », ou dans de grands enclos extérieurs, où ils étaient engraissés avec des noix et des glands. Les loirs étaient également capturés à l'état sauvage à l'automne, quand ils étaient le plus gras, et étaient rôtis et plongés dans le miel ou cuits farcis avec un mélange de porc, de pignons de pin et de divers aromates. Des recherches ont montré qu'en Amazonie, dans les zones où les grands mammifères étaient rares, les pacas et agoutis représentaient environ 40 % de l'ensemble du gibier pris annuellement par les indigènes, mais dans les régions forestières où le grand gibier était prépondérant ils ne représentaient plus que 3 % des prises[94].
Les cochons d'Inde sont utilisés dans la cuisine à Cuzco, au Pérou, dans des plats comme le cuy al horno[3],[95]. Le traditionnel four andin, connu sous le nom de qoncha ou fogón, est fait de boue et d'argile et renforcé avec de la paille et des poils d'animaux comme les cochons d'Inde[96]. Au Pérou, on compte 20 millions de cochons d'Inde domestiques et 64 millions de carcasses sont produites chaque année pour la consommation humaine. Cet animal est une excellente source de nourriture, la chair étant constituée de 19 % de protéines[94]. Aux États-Unis, les écureuils, mais aussi les rats musqués, les porcs-épics et les marmottes sont consommés par l'Homme. Les Navajos mangent les chiens de prairie cuisinés dans la boue, tandis que les Paiutes consomment les géomys, les écureuils et les rats[94].
Les rongeurs, dont les Cochons d'Inde[97], les souris, les rats, les hamsters, les gerbilles, les chinchillas, les octodons et les tamias, peuvent constituer des animaux de compagnie faciles à conserver dans de petits espaces, chaque espèce ayant ses atouts et ses contraintes[98]. La plupart sont gardés dans des cages de taille adaptée, et ils ont des exigences en termes d'espace et d'interactions sociales diverses suivant les espèces. S'ils sont domestiqués très jeunes, ils sont généralement dociles et ne mordent pas. Les Cochons d'Inde ont une grande longévité et ont besoin d'une grande cage[99]. Les rats ont aussi besoin de beaucoup d'espace et peuvent devenir très dociles, apprendre des tours et sembler apprécier la compagnie de l'Homme. Les souris ont une durée de vie courte mais ont besoin de très peu d'espace. Les hamsters sont solitaires mais ont tendance à être plutôt actifs de nuit. Ils ont des comportements intéressants, mais s'ils ne sont pas manipulés fréquemment ils peuvent être agressifs. Les gerbilles ne sont généralement pas agressives, mordent rarement et sont des animaux sociables qui aiment la compagnie de l'Homme et de leurs congénères[100].

Les rongeurs sont régulièrement utilisés comme modèle lors de test sur les animaux en laboratoire[101],[102]. Les rats albinos sont pour la première fois utilisés dans des expériences en 1828, et deviennent par la suite le premier animal domestiqué pour des raisons purement scientifiques[103]. De nos jours, la Souris commune est le rongeur le plus fréquemment utilisé en laboratoire, et en 1979 on estime que 50 millions de ces animaux sont utilisés annuellement à travers le monde. Elles sont préférées du fait de leur petite taille, de leur fertilité, de leur courte durée de gestation et de la facilité avec laquelle on peut les manipuler. Par ailleurs elles sont intéressantes car elles sont sensibles aux infections qui affectent l'Homme. Elles sont utilisées dans des recherches concernant la génétique, la biologie du développement, la biologie cellulaire, l'oncologie et l'immunologie[104]. Les Cochons d'Inde étaient également largement utilisés dans les laboratoires jusqu'à la fin du XXe siècle ; environ 2,5 millions de Cochons d'Inde sont ainsi utilisés dans les laboratoires des États-Unis dans les années 1960[105], mais ce nombre décroit pour ne plus représenter que 375 000 animaux au milieu des années 1990[106]. En 2007, ils constituent 2 % de tous les animaux de laboratoire[105]. Les Cochons d'Inde ont joué un rôle majeur dans l'établissement de la théorie microbienne à la fin du XIXe siècle, à travers les expériences de Louis Pasteur, d'Émile Roux et de Robert Koch[107]. Ils ont été lancés en orbite dans l'espace plusieurs fois — la première fois par l'URSS dans le satellite Spoutnik 9 le 9 mars 1961, avec un retour fructueux[108]. Le Rat-taupe nu est le seul mammifère connu à être poïkilotherme ; il est utilisé pour des études sur la thermorégulation. Il se caractérise aussi par l'absence de production du neuro-transmetteur substance P, un fait qui intéresse les chercheurs travaillant sur la douleur[109].
Les rongeurs ont un odorat très développé, qui est utilisé par l'Homme pour détecter des odeurs ou des molécules chimiques[110]. Le Cricétome des savanes est ainsi capable de détecter le bacille de la tuberculose avec une sensibilité atteignant 86,6 %, et une spécificité (détectant l'absence de bacille) de plus de 93 % ; cette même espèce peut être entraînée pour détecter les mines[111],[112]. Les rats peuvent être utilisés dans des situations périlleuses comme dans les zones de désastres. Ils peuvent être entraînés à répondre à des ordres, qui peuvent être donnés à distance, et même être persuadés de s'aventurer dans des zones très éclairées, que les rats évitent normalement[113],[114],[115].
Des animaux nuisibles et vecteurs de maladies

De par leurs préférences alimentaires et leurs modes de vie (souvent fouisseurs), les rongeurs sont en concurrence avec l'Homme pour une partie de ses activités (culture, sylviculture[116]). Certaines espèces introduites hors de leur milieu sont devenues invasives et sources de dégâts (rat musqué, ragondin, écureuil gris par exemple, quand ils ont été introduits en Europe). Les gros rongeurs ne sont pas sources de pullulations, mais en raison de leur taille font des dégâts parfois spectaculaires. Les petits rongeurs qui se reproduisent très rapidement peuvent périodiquement pulluler et alors causer des dommages importants dans les champs, forêts, entrepôts alimentaires[116],[117]. Par exemple, en 2003, les quantités de riz perdues car consommées par des souris et des rats en Asie représentaient selon des estimations la quantité nécessaire pour nourrir 200 millions de personnes. La plupart des dégâts causés à travers le monde sont le fait d'un petit nombre d'espèces, principalement des rats et des souris[118]. En Indonésie et en Tanzanie, les rongeurs réduisent les rendements des cultures d'environ 15 %, tandis que dans certains cas extrêmes en Amérique du Sud elles sont amputées de 90 %. En Afrique, des rongeurs comme les Mastomys et Arvicanthis font des dégâts dans les céréales, les noix de terre, les légumes et le cacao. En Asie, les rats, les souris et certaines autres espèces comme Microtus brandti, Meriones unguiculatus et Eospalax baileyi détruisent une partie des récoltes de riz, sorgho, tubercules, légumes et noix. En Europe, en plus des rats et des souris, les espèces des genres Apodemus et Microtus ainsi qu'Arvicola terrestris causent de manière épisodique des dégâts dans les vergers, les légumes et les pâtures, aussi bien que dans les céréales. En Amérique du Sud, une gamme plus importante d'espèces de rongeurs est impliquée, parmi lesquelles Holochilus, Akodon, Calomys, Oligoryzomys, Phyllotis, Sigmodon et Zygodontomys, causant des dommages dans les cultures comme la canne à sucre, les fruits, les légumes et les tubercules[118].
Les rongeurs sont également d'importants vecteurs de maladies[119]. Le Rat noir, avec la puce qu'il porte, joue un rôle majeur dans la dissémination de la bactérie Yersinia pestis responsable de la peste bubonique[120] et est également un vecteur des organismes responsables du typhus, de la leptospirose, de la toxoplasmose et de la trichinose[119]. De nombreux rongeurs portent des orthohantavirus, comme ceux de Puumala, de Dobrava ou de Saaremaa, qui peuvent infecter l'homme[121]. Les rongeurs participent également à transmettre des maladies comme la babésiose, la leishmaniose cutanée, l'anaplasmose humaine, la maladie de Lyme, la fièvre hémorragique d'Omsk, l'encéphalomyélite de Powassan, la rickettsialpox, la fièvre récurrente mondiale, la fièvre pourprée des montagnes Rocheuses et la fièvre du Nil occidental[122].
Étant donné que les rongeurs sont une nuisance et qu'ils mettent en danger la santé publique, les sociétés humaines tentent souvent d'en contrôler la prolifération. Cela passe généralement par l'empoisonnement et le piégeage de ces animaux, des méthodes qui ne sont pas toujours sûres ou efficaces. Plus récemment, la lutte intégrée tente d'améliorer le contrôle des populations de rongeurs par une combinaison d'études visant à déterminer la taille et la répartition de la population de nuisibles, l'établissement de seuils de tolérance (niveau d'activité des animaux au-delà duquel il est nécessaire d'intervenir), d'interventions et d'évaluation de l'efficacité de ces interventions à partir d'études régulières. L'intervention peut comprendre l'éducation des populations, l'application d'une législation adaptée, la modification de l'habitat de ces animaux, la modification des pratiques agricoles et la lutte biologique en utilisant des pathogènes ou des prédateurs, ainsi que l'empoisonnement et le piégeage[123]. L'utilisation de pathogènes comme Salmonella a le défaut de pouvoir infecter l'Homme et les animaux domestiques, et les rongeurs deviennent souvent résistants. L'utilisation de prédateurs comme les furets, mangoustes et les varans se montre souvent insatisfaisante. Les chats domestiques et sauvages peuvent contrôler les populations de rongeurs efficacement, si la population de rongeurs n'est pas trop importante[124]. La pose d'affûts, de perchoirs et de nichoirs à rapaces est également une méthode de lutte contre la pullulation de nuisibles[125].
Annexes
Articles connexes
- Liste des familles et genres de rongeurs
- Liste des genres de rongeurs
- Liste des noms vernaculaires de rongeurs
Liens externes
- Notices dans des dictionnaires ou encyclopédies généralistes :
- Ressources relatives au vivant :
- Animal Diversity Web
- Australian Faunal Directory
- Dyntaxa
- EPPO Global Database
- EU-nomen
- Fauna Europaea
- Paleobiology Database
- Global Biodiversity Information Facility
- iNaturalist
- Interim Register of Marine and Nonmarine Genera
- Mammal Species of the World
- NBN Atlas
- Nederlands Soortenregister
- New Zealand Organisms Register
- Plazi
- Système d'information taxonomique intégré
- World Register of Marine Species
- Ressource relative à la santé :
- Zoologie, ostéologie, anatomie comparée
- ArchéoZooThèque : référentiel ostéologique des Rongeurs : photos classées par ordre, famille et espèce
- ArchéoZooThèque : dessins de squelettes de Rongeurs : fichiers disponibles aux formats vectoriel, image et PDF
- Références taxinomiques
- (en) Référence Mammal Species of the World (3e éd., 2005) : Rodentia Bowdich, 1821 (consulté le )
- (en) Référence Tree of Life Web Project : Rodentia (consulté le )
- (en) Référence Fauna Europaea : Rodentia (consulté le )
- (fr + en) Référence ITIS : Rodentia Bowdich, 1821 (consulté le )
- (en) Référence Paleobiology Database : Rodentia Bowditch 1821 (consulté le )
- (en) Référence WoRMS : Rodentia (+ liste familles + liste genres) (consulté le )
- (en) Référence Catalogue of Life : Rodentia Bowdich, 1821 (consulté le )
- Autres liens externes
- (en) Référence UICN : taxon Rodentia (consulté le )
- (en) Référence Animal Diversity Web : Rodentia (consulté le )
- (en) Référence North American Mammals : Rodentia (consulté le )
- (en) Référence NCBI : Rodentia (taxons inclus) (consulté le )
Notes et références
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Rodent » (voir la liste des auteurs).
- (en) Barbara A. Han, John Paul Schmidt, Sarah E. Bowden et John M. Drake, « Rodent reservoirs of future zoonotic diseases », Proceedings of the National Academy of Sciences, vol. 112, no 22, , p. 7039–7044 (ISSN 0027-8424 et 1091-6490, PMID 26038558, PMCID PMC4460448, DOI 10.1073/pnas.1501598112, lire en ligne, consulté le )
- (en) G. Single, C.R. Dickman et D.W. MacDonald, « Rodents », dans D.W. MacDonald, The Encyclopedia of Mammals, Oxford University Press, , 578–587 p. (ISBN 978-0-7607-1969-5)
- (en) Waggoner, Ben, « Introduction to the Rodentia », University of California Museum of Paleontology, (consulté le )
- (en) Nowak, R. M., Walker's Mammals of the World, Johns Hopkins University Press, (ISBN 0-8018-5789-9), p. 1244
- (en) Blashfield, Jean F., « Rodents », Science Encyclopedia (consulté le )
- (en) Brook A. Niemiec, Small Animal Dental, Oral and Maxillofacial Disease : A Colour Handbook, CRC Press, , 288 p. (ISBN 978-1-84076-630-1, lire en ligne), p. 13
- (en) Philip G. Cox et Nathan Jeffery, « Reviewing the Morphology of the Jaw-Closing Musculature in Squirrels, Rats, and Guinea Pigs with Contrast-Enhanced MicroCT », The Anatomical Record, vol. 294, , p. 915–928 (DOI 10.1002/ar.21381, lire en ligne)
- (en) Virginie Millien et Helene Bovy, « When teeth and bones disagree: body mass estimation of a giant extinct rodent », Journal of Mammalogy, vol. 91, no 1, , p. 11–18 (ISSN 0022-2372, DOI 10.1644/08-MAMM-A-347R1.1)
- (en) V. Millien, « The largest among the smallest: the body mass of the giant rodent Josephoartigasia monesi », Proceedings of the Royal Society B: Biological Sciences, vol. 275, no 1646, , p. 1953–1955 (ISSN 0962-8452, DOI 10.1098/rspb.2008.0087)
- (en) A. Rinderknecht et R.E. Blanco, « The largest fossil rodent », Proceedings of the Royal Society B: Biological Sciences, vol. 275, no 1637, , p. 923–928 (ISSN 0962-8452, DOI 10.1098/rspb.2007.1645)
- (en) R. Ernesto Blanco, Andrés Rinderknecht et Gustavo Lecuona, « The bite force of the largest fossil rodent (Hystricognathi, Caviomorpha, Dinomyidae) », Lethaia, vol. 45, no 2, , p. 157–163 (ISSN 0024-1164, DOI 10.1111/j.1502-3931.2011.00265.x)
- (en) Philip G. Cox, Andrés Rinderknecht et R. Ernesto Blanco, « Predicting bite force and cranial biomechanics in the largest fossil rodent using finite element analysis », Journal of Anatomy, vol. 226, no 3, , p. 215–223 (ISSN 0021-8782, DOI 10.1111/joa.12282)
- (en) Sid Perkins, « Ratzilla: Ancient giant rodent chomped like a crocodile », Science, (ISSN 0036-8075, DOI 10.1126/science.aaa7792, lire en ligne)
- (en) Emily H. Kay et Hopi E. Hoekstra, « Rodents », Current Biology, vol. 18, no 10, , R406–R410 (ISSN 0960-9822, DOI 10.1016/j.cub.2008.03.019)
- (en) « AnAge: The animal ageing and longevity database », Human Ageing and Genomics Resources (consulté le )
- (en) R. J. Berry, « The natural history of the house mouse », Field Studies Council, vol. 3, , p. 222 (lire en ligne)
- (en) « Heterocephalus glaber: Naked mole rat », Encyclopedia of Life (consulté le )
- (en) Schwartz, Charles Walsh et Schwartz, Elizabeth Reeder, The Wild Mammals of Missouri, University of Missouri Press, , 368 p. (ISBN 978-0-8262-1359-4, lire en ligne), p. 250
- (en) « Rattus norvegicus: Brown rat », Encyclopedia of Life (consulté le )
- (en) « Sciurus vulgaris: Eurasian red squirrel », Encyclopedia of Life (consulté le )
- (en) Angel E. Spotorno, C.A. Zuleta, J.P. Valladares, A.L. Deane et J.E. Jiménez, « Chinchilla laniger », Mammalian Species, vol. 758, , p. 1–9 (DOI 10.1644/758)
- (en) Sharon Vanderlip, The Guinea Pig Handbook, Barron's, (ISBN 0-7641-2288-6), p. 13
- (en) « Myocastor coypus: Coypu », Encyclopedia of Life (consulté le )
- (en) « Hydrochaeris hydrochaeris:Capybara », Encyclopedia of Life (consulté le )
- (en) A.I. Schulte-Hostedde, « Chapter 10: Sexual Size Dimorphism in Rodents », dans Jerry O. Wolff et Paul W. Sherman, Rodent Societies: An Ecological and Evolutionary Perspective, University of Chicago Press, , 117–119 p. (ISBN 978-0-226-90538-9)
- (en) Rebecca Stefoff, The Rodent Order, Marshall Cavendish, , 62–63, 71–73 (ISBN 978-0-7614-3073-5, lire en ligne)
- (en) R. W Jr. Thorington, Darrow, K. et Anderson, C. G., « Wing tip anatomy and aerodynamics in flying squirrels », Journal of Mammalogy, vol. 79, no 1, , p. 245–250 (DOI 10.2307/1382860, lire en ligne)
- (en) Lennart Hansson, « Habitat, food and population dynamics of the field vole Microtus agrestis (L.) in south Sweden », Viltrevy, vol. 8, , p. 268–278 (ISSN 0505-611X)
- (en) Matthew B. Connior, « Geomys bursarius (Rodentia: Geomyidae) », Mammalian Species, vol. 43, , p. 104–117 (ISSN 0076-3519, DOI 10.1644/879.1)
- (en) « Texan pocket gopher », NSRL: Museum of Texas Tech University (consulté le )
- (en) David Attenborough, The Life of Mammals, BBC Books, , 61–86 p. (ISBN 978-0-563-53423-5)
- (en) Dietland Müller-Schwarze et Lixing Sun, The Beaver : Natural History of a Wetlands Engineer, Cornell University Press, , 67–75 p. (ISBN 978-0-8014-4098-4, lire en ligne)
- (en) Stuart O. Landry, Jr., « The Rodentia as Omnivores », The Quarterly Review of Biology, vol. 45, no 4, , p. 351 (ISSN 0033-5770, DOI 10.1086/406647)
- (en) « Hydromys chrysogaster: Water rat », CSIRO, (consulté le )
- (en) « Northern grasshopper mouse », NSRL: Museum of Texas Tech University (consulté le )
- (en) Jennifer Jarvis, « Eusociality in a mammal: Cooperative breeding in naked mole-rat colonies », Science, vol. 212, no 4494, , p. 571–573 (DOI 10.1126/science.7209555)
- (en) John L. Hoogland, The Black-Tailed Prairie Dog : Social Life of a Burrowing Mammal, University of Chicago Press, , 557 p. (ISBN 978-0-226-35118-6, lire en ligne), p. 1
- (en) George A. Feldhamer, Bruce C. Thompson et Joseph A. Chapman, Wild Mammals of North America : Biology, Management, and Conservation, JHU Press, , 288–310 p. (ISBN 978-0-8018-7416-1, lire en ligne), chap. 15 (« Beaver »)
- (en) Anne Hanson, « Wild Norway rat behavior », Rat behavior and biology, (consulté le )
- (en) J.T. Winslow, N. Hastings, C.S. Carter, C.R. Harbaugh et T.R. Insel, « A role for central vasopressin in pair bonding in monogamous prairie voles », Nature, vol. 365, no 6446, , p. 545–548 (DOI 10.1038/365545a0)
- (en) Nigel C. Bennett et Jennifer U. M. Jarvis, « Cryptomys damarensis », Mammalian Species, vol. 756, no 1, , p. 1 (ISSN 0076-3519, DOI 10.1644/756)
- (en) Hiroyuki Arakawa, D. Caroline Blanchard, Keiko Arakawa, Christopher Dunlap et Robert J. Blanchard, « Scent marking behavior as an odorant communication in mice », Neuroscience and Biobehavioral Reviews, vol. 32, no 7, , p. 1236–1248 (DOI 10.1016/j.neubiorev.2008.05.012)
- (en) Warren G. Holmes et Jill M. Mateo, Rodent Societies : An Ecological and Evolutionary Perspective, University of Chicago Press, , 216–230 p. (ISBN 978-0-226-90538-9, lire en ligne), chap. 19 (« Kin Recognition in Rodents: Issues and Evidence »)
- (en) C.M. Sherwin, Comfortable Quarters For Laboratory Animals, Animal Welfare Institute, , 9e éd. (lire en ligne), « Comfortable quarters for mice in research institutions »
- (fr) Anton Vos, « Il est vraiment « phéromonal » », Campus, vol. 61, , p. 10-11 (lire en ligne)
- (en) Tore Bjorkoyli et Frank Rosell, « A test of the dear enemy phenomenon in the Eurasian beaver », Animal Behavior, vol. 63, no 6, , p. 1073–1078 (DOI 10.1006/anbe.2002.3010)
- (en) M. Vaché, J. Ferron et P. Gouat, « The ability of red squirrels (Tamiasciurus hudsonicus) to discriminate conspecific olfactory signatures », Canadian Journal of Zoology, vol. 79, no 7, , p. 1296–1300 (DOI 10.1139/z01-085)
- (en) Erin L. Shelley et Daniel T. Blumstein, « The evolution of vocal alarm communication in rodents », Behavioral Ecology, vol. 16, no 1, , p. 169–177 (DOI 10.1093/beheco/arh148)
- (en) C.N. Slobodchikoff, Andrea Paseka et Jennifer L. Verdolin, « Prairie dog alarm calls encode labels about predator colors », Animal Cognition, vol. 12, no 3, , p. 435–439 (DOI 10.1007/s10071-008-0203-y, lire en ligne)
- (en) Elke Zimmermann, Lisette Leliveld et Lisette Schehka, The Evolution of Emotional Communication : From Sounds in Nonhuman Mammals to Speech and Music in Man, Oxford University Press, , 392 p. (ISBN 978-0-19-164489-4, lire en ligne), chap. 8 (« Toward the evolutionary roots of affective prosody in human acoustic communication: A comparative approach to mammalian voices »), p. 123–124
- (en) C. Vanden Hole, P.A.A.G. Van Daele, N. Desmet, P. Devos et D. Adriaens, « Does sociality imply a complex vocal communication system? A case study for Fukomys micklemi (Bathyergidae, Rodentia) », Bioacoustics, vol. 23, no 2, , p. 143–160 (DOI 10.1080/09524622.2013.841085)
- (en) C.V. Long, « Vocalisations of the degu (Octodon degus), a social caviomorph rodent », Bioacoustics, vol. 16, , p. 223–244 (ISSN 0952-4622, DOI 10.1080/09524622.2007.9753579)
- (en) Leonardo Ancillotto, Giulia Sozio, Alessio Mortelliti et Danilo Russo, « Ultrasonic communication in Gliridae (Rodentia): the hazel dormouse (Muscardinus avellanarius) as a case study », Bioacoustics, vol. 23, no 2, , p. 129–141 (DOI 10.1080/09524622.2013.838146)
- (en) Jaak Panksepp et Jeff Burgdorf, « "Laughing" rats and the evolutionary antecedents of human joy? », Physiology & Behavior, vol. 79, no 3, , p. 533–547 (PMID 12954448, DOI 10.1016/S0031-9384(03)00159-8)
- (en) « Hearing range », Louisiana State University (consulté le )
- (en) S. Haverkamp, H. Waessle, J. Duebel, T. Kuner, G.J. Augustine, G. Feng et T. Euler, « The primordial, blue-cone color system of the mouse retina », Journal of Neuroscience, vol. 25, no 22, , p. 5438–5445 (DOI 10.1523/JNEUROSCI.1117-05.2005, lire en ligne)
- (en) Anne Hanson, « What do rats see? », sur Rat behavior and biology (consulté le )
- (en) John Pickrell, « Urine vision? How rodents communicate with UV light », sur National Geographic News, (consulté le )
- (en) C. Desjardins, J. A. Maruniak et F.H. Bronson, « Social rank in house mice: Differentiation revealed by ultraviolet visualization of urinary marking patterns », Science, vol. 182, no 4115, , p. 939–941 (PMID 4745598, DOI 10.1126/science.182.4115.939)
- (en) J. Viitala, E. Korpimäki, P. Palokangas et M. Koivula, « Attraction of kestrels to vole scent marks visible in ultraviolet light », Nature, vol. 373, no 6513, , p. 425–427 (DOI 10.1038/373425a0)
- (en) « Vibrational communication in mammals », sur Map of Life: Convergent evolution online, University of Cambridge, (consulté le )
- (en) J.A. Randall, « Evolution and function of drumming as communication in mammals », American Zoologist, vol. 41, , p. 1143–1156 (DOI 10.1093/icb/41.5.1143)
- (en) Jan A. Randall et Marjorie D. Matocq, « Why do kangaroo rats (Dipodomys spectabilis) footdrum at snakes? », Behavioral Ecology, vol. 8, , p. 404–413 (DOI 10.1093/beheco/8.4.404)
- (en) P.M. Narins, O.J. Reichman, J.U.M. Jarvis et E.R. Lewis, « Seismic signal transmission between burrows of the Cape mole-rat Georychus capensis », Journal of Comparative Physiology [A], vol. 170, , p. 13–22 (DOI 10.1007/BF00190397)
- (en) Jane Waterman, Rodent Societies : An Ecological and Evolutionary Perspective, University of Chicago Press, , 610 p. (ISBN 978-0-226-90538-9, lire en ligne), « Chapter 3: Male Mating Strategies in Rodents », p. 28–39
- (en) Nancy G. Soloman et Brain Keane, Rodent Societies : An Ecological and Evolutionary Perspective, University of Chicago Press, , 610 p. (ISBN 978-0-226-90538-9, lire en ligne), « Chapter 4: Reproductive Strategies in Female Rodents », p. 42–52
- (en) Betty McGuire et William E. Bernis, Rodent Societies : An Ecological and Evolutionary Perspective, University of Chicago Press, , 231–235 p. (ISBN 978-0-226-90538-9, lire en ligne), « Chapter 20: Parental Care »
- (en) Warren G. Holmes et Jill M. Mateo, Rodent Societies : An Ecological and Evolutionary Perspective, University of Chicago Press, , 610 p. (ISBN 978-0-226-90538-9, lire en ligne), « Chapter 19: Kin Recognition in Rodents: Issues and Evidence », p. 226–227
- (en) Luis A. Ebensperger et Daniel T. Blumsperger, Rodent Societies : An Ecological and Evolutionary Perspective, University of Chicago Press, , 610 p. (ISBN 978-0-226-90538-9, lire en ligne), « Chapter 23: Nonparental Infanticide », p. 274–278
- (en) J. L. Hoogland, « Infanticide in prairie dogs: Lactating females kill offspring of close kin », Science, vol. 230, no 4729, , p. 1037–1040 (PMID 17814930, DOI 10.1126/science.230.4729.1037)
- (en) Klaus Hackländera, Erich Möstlb et Walter Arnold, « Reproductive suppression in female Alpine marmots, Marmota marmota », Animal Behaviour, vol. 65, no 6, , p. 1133–1140 (DOI 10.1006/anbe.2003.2159)
- (en) Kristofer M. Helgen, « The amphibious murines of New Guinea (Rodentia, Muridae): the generic status of Baiyankamys and description of a new species of Hydromys », Zootaxa, vol. 913, , p. 1–20 (ISSN 1175-5326)
- (en) V.R. Parshad, « Rodent Control in India », Integrated Pest Management Reviews, vol. 4, no 2, , p. 97-126 (ISSN 1353-5226, DOI 10.1023/A:1009622109901, lire en ligne)
- (en) A. Janke, L. Martínez-Estévez, P. Balvanera, J. Pacheco et G. Ceballos, « Prairie dog decline reduces the supply of ecosystem services and leads to desertification of semiarid grasslands », PLoS ONE, vol. 8, no 10, , e75229 (DOI 10.1371/journal.pone.0075229)
- (en) Kirsten Krueger, « Feeding relationships among bison, pronghorn, and prairie dogs: an experimental analysis », Ecology, vol. 67, no 3, , p. 760-770 (ISSN 0012-9658, DOI 10.2307/1937699)
- (en) F. Pérez, C. Castillo-Guevara, G. Galindo-Flores, M. Cuautle et A. Estrada-Torres, « Effect of gut passage by two highland rodents on spore activity and mycorrhiza formation of two species of ectomycorrhizal fungi (Laccaria trichodermophora and Suillus tomentosus) », Botany, vol. 90, no 11, , p. 1084–1092 (ISSN 1916-2790, DOI 10.1139/b2012-086)
- (en) Denise Burchsted, Melinda Daniels, Robert Thorson et Jason Vokoun, « The river discontinuum: applying beaver modifications to baseline conditions for restoration of forested headwaters », BioScience, vol. 60, no 11, , p. 908–922 (ISSN 0006-3568, DOI 10.1525/bio.2010.60.11.7)
- (en) Justin Wright, Clive Jones et Alexander Flecker, « An ecosystem engineer, the beaver, increases species richness at the landscape scale », Oecologia, vol. 132, no 1, , p. 96–101 (ISSN 0029-8549, DOI 10.1007/s00442-002-0929-1)
- (en) Paul S. Kemp, Tom A. Worthington, Terence E.L. Langford, Angus R.J. Tree et Martin J. Gaywood, « Qualitative and quantitative effects of reintroduced beavers on stream fish », Fish and Fisheries, vol. 13, no 2, , p. 158–181 (ISSN 1467-2960, DOI 10.1111/j.1467-2979.2011.00421.x)
- « Rongeurs - L'encyclopedie canadienne »
- Mammal Species of the World (version 3, 2005), consulté le 8 octobre 2012
- Fossilworks Paleobiology Database, consulté le 20 mars 2015
- (en) G. Amori et S. Gippoliti, « A higher-taxon approach to rodent conservation priorities for the 21st century », Animal Biodiversity Conservation, vol. 26, no 2, , p. 1–18 (lire en ligne)
- (en) G. S. Morgan, « Quaternary land vertebrates of Jamaica », Geological Society of America Memoir, vol. 182, , p. 417–442 (DOI 10.1130/mem182-p417)
- (en) « Rodent Conservation Assessment », WAZA (consulté le )
- (en) Eduardo Gudynas, Rodents : A World Survey of Species of Conservation Concern : Based on the Proceedings of a Workshop of the IUCN/SSC Rodent Specialist Group, Held at the Fourth International Theriological Congress, August 17, 1985, Edmonton, Alberta, Canada, IUCN, , p. 23
- (en) A.P. Buckle et M.G.P. Fenn, « Rodent Control in the Conservation of Endangered Species », Proceedings of the 15th Vertebrate Pest Conference, Hyatt Newporter, Newport Beach, California, , Paper 12 (lire en ligne) 3–5 March 1992
- (en) K.A. Hindwood, « Birds of Lord Howe Island », Emu, vol. 40, , p. 1–86 (DOI 10.1071/mu940001)
- « Lundy puffins back from the brink », sur BBC Devon, (consulté le )
- Heather Mitchell, « Puffins a-plenty? New hope for Lundy and other UK seabird islands », RSPB, (consulté le )
- (en) Feinstein, Kelly, « Felting a beaver hat » [archive du ], sur Fashionable Felted Fur, UC Santa Cruz, (consulté le )
- (en) Harold A. Innis, The Fur Trade in Canada : An Introduction to Canadian Economic History, University of Toronto Press, , 463 p. (ISBN 978-0-8020-8196-4, lire en ligne), p. 9–12
- (en) « Excessive trade: Clothes and trimming », Granby Zoo (consulté le )
- (en) Lynwood A. Fiedler, « Rodents as a Food Source », Proceedings of the Fourteenth Vertebrate Pest Conference 1990, University of California, Davis, , p. 149–155
- (en) David Knowlton, « Guinea Pig, Pet or Festive Meal » [archive du ], sur Cuzco Eats, (consulté le )
- Walter Coraza Morveli et David Knowlton, « Traditional Mud Stoves and Ovens Make the Best Food » [archive du ], sur Cuzco Eats, (consulté le )
- (en) « Guinea pigs », RSPCA, (consulté le )
- (en) « Pet Rodents », RSPCA, (consulté le )
- (en) Jessie Blount Allen Charters, « The associative processes of the guinea pig: A study of the psychical development of an animal with a nervous system well medullated at birth », University of Chicago Press, vol. XIV, no 4, , p. 300–337 (lire en ligne)
- (en) Ray Broekel, Gerbil Pets and Other Small Rodents, Childrens Press, , 45 p. (ISBN 978-0-516-01679-5, lire en ligne), p. 5–20
- (en) « Introduction to the Rodentia », University of California Museum of Paleontology (consulté le )
- (en) Jerry O. Wolff et Paul W. Sherman, Rodent Societies : An Ecological and Evolutionary Perspective, University of Chicago Press, , 610 p. (ISBN 978-0-226-90538-9, lire en ligne), p. 3–8
- (en) George J. Krinke, Gillian R. Bullock et Tracie Bunton, The Laboratory Rat (Handbook of Experimental Animals), Academic Press, (ISBN 0-12-426400-X), « History, strains and models », p. 3–16
- (en) Herbert C. Morse, The Mouse in Biomedical Research : History, Genetics, and Wild Mice, Elsevier, , 320 p. (ISBN 978-0-323-15606-6, lire en ligne), « The Laboratory Mouse: A Historical Assessment », xi, 1
- (en) Shayne C. Gad, Animal Models in Toxicology, Boca Raton, Taylor & Francis, , seconde éd., 933 p. (ISBN 978-0-8247-5407-5 et 0-8247-5407-7), p. 334–402
- (en) John E. Harkness et Joseph E. Wagner, The Biology and Medicine of Rabbits and Rodents, Williams & Wilkins, , 372 p. (ISBN 0-683-03919-9), p. 30–39
- (en) Anita Guerrini, Experimenting with Humans and Animals : from Galen to animal rights, Baltimore, Johns Hopkins, , 165 p. (ISBN 0-8018-7196-4), p. 98–104
- (en) Tara Gray, « A Brief History of Animals in Space », National Aeronautics and Space Administration, (consulté le )
- (en) C. M. Sherwin, UFAW Handbook on the Care and Management of Laboratory Animals, Wiley-Blackwell, , « 25: The Husbandry and Welfare of Non-traditional Laboratory Rodents », p. 359–369
- (en) Michael Wines, « Gambian rodents risk death for bananas », sur The Age, (consulté le )
- Hassan Mhelela, « Giant rats trained to detect land mines and tuberculosis in Africa », BBC, (consulté le )
- Nicholas Bakalar, « Detecting Tuberculosis: No Microscopes, Just Rats », sur New York Times, (consulté le )
- (en) Ben Harder, « Scientists "Drive" rats by remote control », sur National Geographic, (consulté le )
- (en) O. Solon, « Man's mission to build remote control systems for dogs, roaches and sharks » [archive du ], sur Wired, (consulté le )
- (en) S. Xu, S. K. Talwar, E. S. Hawley, L. Li et J. K. Chapin, « A multi-channel telemetry system for brain microstimulation in freely roaming animals », Journal of Neuroscience Methods, vol. 133, nos 1–2, , p. 57–63 (DOI 10.1016/j.jneumeth.2003.09.012)
- F Caroulle et O Baubet, « Dégâts de rongeurs en forêt : Comment y remédier ? », Revue forestière française, vol. 58, , p. 449-462 (lire en ligne)
- B. G. Meerburg, G. R Singleton et H. Leirs, « The Year of the Rat ends: time to fight hunger! », Pest Management Science, vol. 65, no 4, , p. 351–2 (PMID 19206089, DOI 10.1002/ps.1718, lire en ligne)
- (en) N.C. Stenseth, H. Leirs, A. Skonhoft et al., « Mice, rats, and people: The bio-economics of agricultural rodent pests », Frontiers in Ecology and the Environment, vol. 1, no 77, , p. 367–375 (DOI 10.2307/3868189, JSTOR 3868189, lire en ligne [PDF])
- (en) B. G. Meerburg, G. R. Singleton et A. Kijlstra, « Rodent-borne diseases and their risks for public health », Critical Reviews in Microbiology, vol. 35, no 3, , p. 221–70 (PMID 19548807, DOI 10.1080/10408410902989837, lire en ligne [PDF])
- (en) M. McCormick, « Rats, communications, and plague: Toward an ecological history », Journal of Interdisciplinary History, vol. 34, no 1, , p. 1–25 (DOI 10.1162/002219503322645439, lire en ligne)
- « Rodent-borne diseases » [archive du ], European Centre for Disease Prevention and Control (consulté le )
- « Diseases indirectly transmitted by rodents », Centers for Disease Control and Prevention, (consulté le )
- (en) Centers for Disease Control and Prevention, Integrated pest management : conducting urban rodent surveys, Atlanta, US Department of Health and Human Services, (lire en ligne)
- (en) K. Wodzicki, « Prospects for biological control of rodent populations », Bulletin of the World Health Organization, vol. 48, no 4, , p. 461–467 (PMID 4587482, PMCID 2481104, lire en ligne)
- Christophe Viguier, Produire des fruits en agriculture biologique, Institut technique de l'agriculture biologique, , p. 57.
