Biostampa tridimensionale


La biostampa in tre dimensioni (in inglese: 3D bioprinting) è una tecnologia che permette, tramite una stampante in 3d, di produrre tessuti e organi. La biostampa in 3D deposita un biomateriale, detto biolink, strato su strato per creare strutture tissutali che possono essere usati in campo medico.[1] Allo stato attuale la biostampa si limita a creare tessuti e mini organi per facilitare la ricerca farmacologica.[2] Questa tecnologia comprende la stampa di matrici extracellulari e di cellule viventi.[3] Inoltre il bioprinting è in grado di generare impalcature che possono essere usate per rigenerare giunture e legamenti.[4]
Processo
La biostampa segue sostanzialmente tre passaggi: pre-bioprinting, bioprinting e post-bioprinting.[5][6]
Il pre-bioprinting consiste nella creazione di un modello che successivamente la stampante creerà. Un primo passaggio comprende la biopsia dell'organo. Le tecnologie usate per il bioprinting sono la tomografia computerizzata e la risonanza magnetica. Viene poi fatta una ricostruzione tomografica e le immagini ottenute vengono inviate alla stampante. Una volta creata l'immagine, alcune cellule vengono isolate e poi moltiplicate.[5] Queste cellule vengono mescolate con uno speciale materiale che fornisce ossigeno ed altri nutrienti per tenerle vive. In alcuni processi le cellule vengono incapsulate in sfere di 500 µm di diametro. L'aggregazione di cellule non richiede un'impalcatura e si inseriscono nel tessuto tubulare.[7]
Il secondo passo prevede che il bioink, cioè un misto di cellule, matrici e nutrienti, venga piazzato nella cartuccia e poi depositato.[8]
La terza fase, il post-bioprinting, è necessaria per stabilizzare la struttura, altrimenti il risultato finale è a rischio.[9] Dunque il tessuto stampato deve ricevere stimoli chimici e meccanici.[10]
Approcci
Attualmente i ricercatori stanno studiando tre diversi metodi per ottenere organi dal bioprinting, con la biomimetica, con l'assemblamento delle cellule e con l'uso di mini-tessuti.[11]
La biomimetica ha come scopo di creare tessuti e organi artificiali che sono identici a quelle naturali. La biomimetica richiede la duplicazione della forma, della struttura e dell'ambiente dell'organo o del tessuti.[12] L'applicazione della biomimetica nel bioprintng comporta la creazione di identiche parti cellulari ed extracellulari dell'organo. Il tessuto deve essere replicato in scala, poi bisogna comprendere il microambiente, l'organizzazione cellulare e la matrice extracellulare.[11]
L'auto-assemblamento si ricollega al processo di sviluppo degli organi in stato embrionale.[12] Quando le cellule sono al loro primo sviluppo, creano autonomamente la loro impalcatura extracellulare.[11]
Il terzo approccio consiste in una combinazione dei due precedenti. In questo caso i tessuti e gli organi sono costruiti partendo da componenti in miniatura.[11][12]
Stampanti
Simili alle normali stampanti a inchiostro, le biostampanti hanno tre componenti principali: l'hardware utilizzato, il tipo di bioinchiostro e il materiale su cui viene stampato (biomateriali).
I bioinchiostri sono componenti essenziali del processo di bioprinting. Sono composti da cellule viventi e integratori enzimatici per nutrire un ambiente che supporta le esigenze biologiche del tessuto stampato. L'ambiente creato dal bioinchiostro consente alla cellula di attaccarsi, crescere e differenziarsi nella sua forma adulta[13].
| Metodo di biostampa | Modalità di stampa | Vantaggi |
|---|---|---|
| Stampa diretta | Basata su estrusione[14] | Esecuzione semplice, nessun getto d'inchiostro |
| Estrusione coassiale | Basata su estrusione[15] | Formazione in un unico passaggio di costrutti multistrato |
| Indiretto | Basata su estrusione[16] | Richiede un "materiale sacrificale" rimovibile per supportare la formazione strutturale |
| Laser | Basata su laser[17] | Nessuna sollecitazione di taglio sulle cellule sospese nell'inchiostro |
| Droplet | Basata su goccioline[18] | Controllo preciso del flusso e della formazione dell'impalcatura |
Applicazioni
La biostampa 3D può essere utilizzata per ricostruire tessuti da varie regioni del corpo. Il precursore dell'adozione della stampa 3D nell'assistenza sanitaria è stata una serie di sperimentazioni condotte dai ricercatori del Boston Children's Hospital. Il team ha costruito manualmente vesciche urinarie sostitutive per 7 pazienti, realizzando scaffolds (strutture artificiali in grado di supportare la formazione di tessuti tridimensionali) con cellule dei pazienti e consentendo loro di crescere. Le sperimentazioni hanno avuto successo poiché i pazienti sono rimasti in buona salute per 7 anni dopo l'impianto, il che ha portato un ricercatore di nome Anthony Atala, a cercare modi per automatizzare il processo[19]. I pazienti con malattia della vescica allo stadio terminale possono ora essere curati utilizzando tessuti della vescica stessa bioingegnerizzati per ricostruire l'organo danneggiato[20]. Questa tecnologia può anche essere potenzialmente applicata a ossa, pelle, cartilagine e tessuto muscolare[21]. Sebbene un obiettivo a lungo termine della tecnologia della biostampa 3D sia quello di ricostruire un intero organo e ridurre al minimo il problema della mancanza di organi per il trapianto[22]. C'è stato poco successo nella biostampa di organi completamente funzionali, ad esempio fegato, pelle, menisco o pancreas[23][24][25].
La biostampa 3D contribuisce a significativi progressi nel campo medico dell'ingegneria tissutale consentendo di effettuare ricerche su materiali innovativi chiamati biomateriali[26][27].
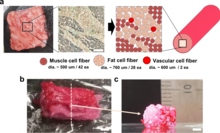
La biostampa può essere utilizzata anche per la carne coltivata. Nel 2021 è stata prodotta una carne coltivata simile alla bistecca, composta da tre tipi di fibre cellulari bovine. La carne di manzo simile al wagyū ha una struttura simile alla carne originale[28]. Questa tecnologia fornisce un'alternativa ai metodi naturali di raccolta della carne se l'industria del bestiame è afflitta da malattie. Inoltre, fornisce una possibile soluzione per ridurre l'impatto ambientale dell'industria del bestiame.
La biorisanamento utilizza microrganismi o, in tempi recenti, materiali di origine biologica, come enzimi, biocompositi, biopolimeri o nanoparticelle, per degradare biochimicamente i contaminanti in sostanze innocue, rendendolo un'alternativa ecologica ed economica; la biostampa 3D facilita la fabbricazione di strutture funzionali utilizzando questi materiali che migliorano i processi di biorisanamento, portando a un notevole interesse nell'applicazione di costrutti biostampati in 3D nel migliorare tale tecnologia[28].
La biostampa di biofilm utilizza gli stessi metodi di altri tipi di biostampa. Spesso, il biofilm inizia con un'estrusione di un polisaccaride per fornire struttura per la crescita del biofilm stesso. Un esempio di uno di questi polisaccaridi è l'alginato. La struttura dell'alginato può avere microbi incorporati al suo interno. Gli idrogel possono anche essere utilizzati per aiutare nella formazione di biofilm funzionali[29].
Utilizzi futuri
La biostampa ha anche possibili utilizzi in futuro nell'assistenza al trattamento delle acque reflue e nel controllo della corrosione[29]. Quando gli esseri umani entrano in contatto con biofilm ambientali, è possibile che si verifichino infezioni e rischi per la salute a lungo termine[30]. La penetrazione e l'espansione degli antibiotici all'interno di un biofilm è un'area di ricerca che può trarre vantaggio dalle tecniche di biostampa, per esplorare ulteriormente l'effetto dei biofilm ambientali sulla salute umana. La stampa di biofilm richiede ulteriori ricerche a causa dei dati pubblicati limitati e dei protocolli complessi[31].
Note
- ^ Roche CD, Brereton RJ, Ashton AW, Jackson C, Gentile C (2020). "Current challenges in three-dimensional bioprinting heart tissues for cardiac surgery". European Journal of Cardio-Thoracic Surgery. 58 (3): 500–510.
- ^ Hinton TJ, Jallerat Q, Palchesko RN, Park JH, Grodzicki MS, Shue HJ, et al. (October 2015). "Three-dimensional printing of complex biological structures by freeform reversible embedding of suspended hydrogels"
- ^ Roche CD, Sharma P, Ashton AW, Jackson C, Xue M, Gentile C (2021). "Printability, durability, contractility and vascular network formation in 3D bioprinted cardiac endothelial cells using alginate–gelatin hydrogels". Frontiers in Bioengineering and Biotechnology. 9: 110.
- ^ Nakashima Y, Okazak K, Nakayama K, Okada S, Mizu-uchi H (January 2017). "Bone and Joint Diseases in Present and Future". Fukuoka Igaku Zasshi = Hukuoka Acta Medica. 108 (1): 1–7.
- ^ a b Shafiee A, Atala A (March 2016). "Printing Technologies for Medical Applications". Trends in Molecular Medicine. 22 (3): 254–265.
- ^ Ozbolat IT (July 2015). "Bioprinting scale-up tissue and organ constructs for transplantation". Trends in Biotechnology. 33 (7): 395–400.
- ^ Chua CK, Yeong WY, Bioprinting: Principles and Applications, Singapore, World Scientific Publishing Co., 2015
- ^ Cooper-White M (1 March 2015). "How 3D Printing Could End The Deadly Shortage Of Donor Organs". Huffpost Science. TheHuffingtonPost.com, Inc. Retrieved 17 February 2016.
- ^ Shafiee A, Atala A (March 2016). "Printing Technologies for Medical Applications". Trends in Molecular Medicine. 22 (3): 254–265
- ^ ingh D, Thomas D (April 2019). "Advances in medical polymer technology towards the panacea of complex 3D tissue and organ manufacture". American Journal of Surgery. 217 (4): 807–808.
- ^ a b c d Murphy SV, Atala A (August 2014). "3D bioprinting of tissues and organs". Nature Biotechnology. 32 (8): 773–85.
- ^ a b c Yoo J, Atala A (2015). "Bio-printing: 3D printing comes to life".
- ^ Bioink Selection for 3D Bioprinting, su sigmaaldrich.com.
- ^ Pallab Datta, Bugra Ayan e Ibrahim T. Ozbolat, Bioprinting for vascular and vascularized tissue biofabrication, in Acta Biomaterialia, vol. 51, 15 marzo 2017, pp. 1–20, DOI:10.1016/j.actbio.2017.01.035. URL consultato il 19 ottobre 2024.
- ^ (EN) Prerak Gupta e Biman B. Mandal, Tissue‐Engineered Vascular Grafts: Emerging Trends and Technologies, in Advanced Functional Materials, vol. 31, n. 33, 2021-08, DOI:10.1002/adfm.202100027. URL consultato il 19 ottobre 2024.
- ^ Three-dimensional printing of complex biological structures by freeform reversible embedding of suspended hydrogels, su pmc.ncbi.nlm.nih.gov.
- ^ Raphaël Devillard, Emeline Pagès e Manuela Medina Correa, Chapter 9 - Cell Patterning by Laser-Assisted Bioprinting, collana Micropatterning in Cell Biology Part A, vol. 119, Academic Press, 1º gennaio 2014, pp. 159–174. URL consultato il 19 ottobre 2024.
- ^ Ahmed Munaz, Raja K. Vadivelu e James St. John, Three-dimensional printing of biological matters, in Journal of Science: Advanced Materials and Devices, vol. 1, n. 1, 1º marzo 2016, pp. 1–17, DOI:10.1016/j.jsamd.2016.04.001. URL consultato il 19 ottobre 2024.
- ^ (EN) Matthew Whitaker, The history of 3D printing in healthcare, in The Bulletin of the Royal College of Surgeons of England, vol. 96, n. 7, 2014-07, pp. 228–229, DOI:10.1308/147363514X13990346756481. URL consultato il 19 ottobre 2024.
- ^ The history of 3D printing in healthcare, su thelancet.com.
- ^ (EN) Nhayoung Hong, Gi‐Hoon Yang e JaeHwan Lee, 3D bioprinting and its in vivo applications, in Journal of Biomedical Materials Research Part B: Applied Biomaterials, vol. 106, n. 1, 2018-01, pp. 444–459, DOI:10.1002/jbm.b.33826. URL consultato il 19 ottobre 2024.
- ^ Kalyani Shinkar e Kawal Rhode, Could 3D extrusion bioprinting serve to be a real alternative to organ transplantation in the future?, in Annals of 3D Printed Medicine, vol. 7, 1º agosto 2022, pp. 100066, DOI:10.1016/j.stlm.2022.100066. URL consultato il 19 ottobre 2024.
- ^ 90-OR: 3D Bioprinting of a Bionic Pancreas with a Vascular System—Results of Transplantation in Large Animals, su diabetesjournals.org.
- ^ (EN) Adir C. Sommer e Eytan Z. Blumenthal, Implementations of 3D printing in ophthalmology, in Graefe's Archive for Clinical and Experimental Ophthalmology, vol. 257, n. 9, 1º settembre 2019, pp. 1815–1822, DOI:10.1007/s00417-019-04312-3. URL consultato il 19 ottobre 2024.
- ^ Novel Strategies in Artificial Organ Development: What Is the Future of Medicine?, su pmc.ncbi.nlm.nih.gov.
- ^ (EN) Japanese scientists produce first 3D-bioprinted, marbled Wagyu beef, su New Atlas, 25 agosto 2021. URL consultato il 19 ottobre 2024.
- ^ Dong-Hee Kang, Fiona Louis e Hao Liu, Engineered whole cut meat-like tissue by the assembly of cell fibers using tendon-gel integrated bioprinting, in Nature Communications, vol. 12, 1º agosto 2021, pp. 5059, DOI:10.1038/s41467-021-25236-9. URL consultato il 19 ottobre 2024.
- ^ a b 3D bioprinting in bioremediation: a comprehensive review of principles, applications, and future directions, su pmc.ncbi.nlm.nih.gov.
- ^ a b Emergent Biological Endurance Depends on Extracellular Matrix Composition of Three-Dimensionally Printed Escherichia coli Biofilms, DOI:10.1021/acssynbio.1c00290.s002. URL consultato il 19 ottobre 2024.
- ^ (EN) Yifei Liu, Xiudong Xia e Zhen Liu, The Next Frontier of 3D Bioprinting: Bioactive Materials Functionalized by Bacteria, in Small, vol. 19, n. 10, 2023-03, DOI:10.1002/smll.202205949. URL consultato il 19 ottobre 2024.
- ^ Tianyang Zhao, Yinuo Liu e Yichen Wu, Controllable and biocompatible 3D bioprinting technology for microorganisms: Fundamental, environmental applications and challenges, in Biotechnology Advances, vol. 69, 1º dicembre 2023, pp. 108243, DOI:10.1016/j.biotechadv.2023.108243. URL consultato il 19 ottobre 2024.
Bibliografia
- (EN) Christopher David Roche, Russell Brereton, Anthony Wayne Ashton, Christopher Jackson e Carmine Gentile, Current challenges in three-dimensional bioprinting heart tissues for cardiac surgery (PDF), in European Journal of Cardio-Thoracic Surgery, vol. 58, n. 3, Oxford, Oxford Academy, settembre 2020, pp. 500-510, DOI:10.1093/ejcts/ezaa093, PMID 32391914.
- (EN) Thoas Hinton, Quentin Jallerat, Rachelle Palchesko, Joon Hyung Park, Martin Grodzicki, Hao-Jan Shue, Mohamed Ramadan, Andrew Hudson e Adam Feinberg, Three-dimensional printing of complex biological structures by freeform reversible embedding of suspended hydrogels (PDF), in Science Advances, vol. 1, n. 9, ottobre 2015, pp. 1-10, DOI:10.1126/sciadv.1500758, PMID 26601312.
- (EN) Christopher David Roche, Poonam Sharma, Anthony Wayne Ashton, Christopher Jackson, Meilang Xue e Carmine Gentile, Printability, Durability, Contractility and Vascular Network Formation in 3D Bioprinted Cardiac Endothelial Cells Using Alginate–Gelatin Hydrogels (PDF), in Frontiers in Bioengineering and Biotechnology, vol. 9, febbraio 2021, DOI:10.3389/fbioe.2021.636257, PMID 33748085.
- (JA) Yasuharu Nakashima, Ken Okazak, Koichiet Nakayama, Seiji Okada, Hao-Jan Shue e Hideki Mizu-Uchi, Bone and Joint Diseases in Present and Future (abstract), in Fukuoka Igaku Zasshi, vol. 108, n. 1, febbraio 2017, pp. 1-7, PMID 29226660.
- (EN) Anthony Atala e Ashkan Shafiee, Printing Technologies for Medical Applications (PDF) (abstract), in Trends in Molecular Medicine, vol. 22, n. 3, CellPress, marzo 2016, pp. 254-265, DOI:10.1016/j.molmed.2016.01.003, PMID 26856235.
- (EN) Ibrahim Ozbolat, Bioprinting scale-up tissue and organ constructs for transplantation (PDF) (abstract), in Trends in Molecular Medicine, vol. 33, n. 7, Oxford, Oxford Academy, luglio 2015, pp. 395-400, DOI:10.1016/j.tibtech.2015.04.005, PMID 25978871.
- (EN) Chee Kai Chua e Wai Yee Yeong, Bioprinting - Principles and Applications, Singapore, World Scientific Publishing Co., 2015.
- (EN) Macrina Cooper-White, How 3D Printing Could End The Deadly Shortage Of Donor Organs, in Huffington Post, 3 gennaio 2015. URL consultato il 16 settembre 2021.
- (EN) Katherine Harmon, A sweet solution for replacing organs (PDF) (abstract), in Scientific American, vol. 308, n. 4, Nature Publishing Group, 2013, pp. 54-55, DOI:10.1038/scientificamerican0413-54 (archiviato dall'url originale il 17 febbraio 2016).
- (EN) Deepti Singh e Daniel Thomas, Advances in medical polymer technology towards the panacea of complex 3D tissue and organ manufacture, in American Journal of Surgery, vol. 217, n. 4, aprile 2019, pp. 807-808, DOI:10.1016/j.amjsurg.2018.05.012, PMID 29803500.
- (EN) Anthony Atala e Sean Murphy, 3D bioprinting of tissues and organs, in Nature Biotechnology, vol. 32, n. 8, agosto 2014, pp. 773-785, DOI:10.1038/nbt.2958, PMID 25093879.
- (EN) Anthony Atala e James Yoo, Bio-printing: 3D printing comes to life, in Manufacturing Engineering, supplemento Medical Manufacturing, 2015, pp. 63-66.
- (EN) John Manappallil, Basic Dental Materials, New Delhi, Jaypee Medical Brothers, 2015.
- (EN) 3d printing technogy at the service of health, in London Time, 28 gennaio 2016. URL consultato il 16 settembre 2021 (archiviato dall'url originale il 14 settembre 2016).
- (EN) Eric Lepowsky, Metin Muradoglu e Savas Tasoglu, Towards preserving post-printing cell viability and improving the resolution: Past, present, and future of 3D bioprinting theory (PDF), in Bioprinting, vol. 11, Elsevier, settembre 2018, pp. 1-17, DOI:10.1016/j.bprint.2018.e00034, ISSN 2405-8866.
- (EN) Zeming Gu, Jianzhong Fu, Hui Lin e Yong He, Development of 3D bioprinting: From printing methods to biomedical applications (PDF), in Asian Journal of Pharmaceutical Sciences, vol. 15, n. 5, settembre 2020, pp. 529-557, DOI:10.1016/j.ajps.2019.11.003, PMID 33193859.
- (EN) Soroosh Derakhshanfar, Rene Mbeleck, Kaige Xu, Xingying Zhang, Wen Zhong e Malcolm Xing, 3D bioprinting for biomedical devices and tissue engineering: A review of recent trends and advances (PDF), in Bioactive Materials, vol. 3, n. 2, giugno 2018, pp. 144-156, DOI:10.1016/j.bioactmat.2017.11.008, PMID 2974452.
- (EN) David Zopf, Marc Nelson, Richard Ohye, Scott Hollister e Glenn Green, Bioresorbable Airway Splint Created with a Three-Dimensional Printer (abstract), in The New England Journal of Medicine, vol. 368, n. 21, maggio 2013, pp. 2043-2045, DOI:10.1056/NEJMc1206319, PMID 23697530.
- (EN) Anthony Atala, Stuart Bauer, Shay Soker, James Yoo e Alan Retik, Tissue-engineered autologous bladders for patients needing cystoplasty (abstract), in Lancet, vol. 367, n. 9518, aprile 2006, pp. 1241-1246, DOI:10.1016/S0140-6736(06)68438-9, PMID 16631879.
Voci correlate
Altri progetti
 Wikimedia Commons contiene immagini o altri file su biostampa tridimensionale
Wikimedia Commons contiene immagini o altri file su biostampa tridimensionale