Epimero


In chimica si definiscono come epimeri i diastereoisomeri che presentano una differente configurazione presso un solo stereocentro.[1] I diastereoisomeri non sono specularmente sovrapponibili. Se un epimero viene incorporato all'interno di una struttura ad anello, esso viene chiamato anomero.
Nella nomenclatura chimica, a una delle coppie di epimeri viene dato il prefisso epi-, come ad esempio in chinino e epi-chinino. Quando le coppie sono enantiomeri, il prefisso diventa ent-.
Esempi
Gli zuccheri glucosio e galattosio sono epimeri.

Nell'α-glucosio, il gruppo -OH sul primo atomo (anomerico) di carbonio è in direzione opposta rispetto al gruppo metandiile del carbonio C-6 (in posizione assiale). Nel β-glucosio, il gruppo-OH è orientato nella stessa direzione del gruppo metilene (in posizione equatoriale).[2] Queste due molecole sono contemporaneamente epimeri e anomeri, come è indicato dalla designazione α-glucosio e β-glucosio.
 |

|
α-D-glucopiranosio |
β-D-glucopiranosio
|
Un altro esempio si trova ancora nella chimica degli zuccheri: il D-mannosio ed il D-glucosio differiscono solo per la configurazione del C2.
Gli stereoisomeri β-D-glucopiranosio e β-D-mannopiranosio sono epimeri perché differiscono solo nella stereochimica della posizione C-2. L'ossidrile del β-D-glucopiranosio è equatoriale (cioè nel piano dell'anello) mentre nel β-D-mannopiranosio l'ossidrile del C-2 è in conformazione assiale (fuori dal piano dell'anello). Queste due molecole sono epimeri ma non enantiomeri (gli enantiomeri hanno lo stesso nome, ma differiscono per la classificazione D e L). Non sono nemmeno zuccheri anomeri perché la stereochimica non coinvolge l'atomo di carbonio appropriato.
 |

|
β-D-glucopiranosio |
β-D-mannopiranosio
|
Doxorubicina e epirubicina sono due molecole strettamente collegate ed epimeri.

|
Doxorubicina–epirubicina
|
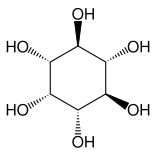
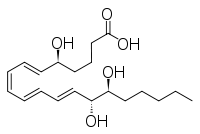
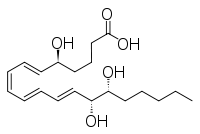
Altri due composti strettamente correlati sono inositolo ed epi-inositolo, lipossina ed epi-lipossina.
 |
 |
 |
|
Epi-inositolo
|
Inositolo
|
Lipossina
|
Epilipossina
|
Epimerizzazione
Il processo che porta all'interconversione di epimeri, cioè alla trasformazione di un epimero nella sua controparte chirale, prende il nome di epimerizzazione. Un esempio è la reazione di depolimerizzazione dei tannini condensati.
L'epimerizzazione può avvenire in modo spontaneo, e in questo caso si tratta generalmente di un processo lento, ma può anche venire catalizzata da enzimi, come nel caso dell'epimerizzazione tra gli zuccheri N-acetilglucosamina and N-acetilmannosamina, che è catalizzata da RENBP.
Note
Voci correlate
Collegamenti esterni
- (EN) Definizione IUPAC, su goldbook.iupac.org.
