Óxido de lítio
Óxido de lítioAlerta sobre risco à saúde
Nome IUPAC
Óxido de Lítio
Outros nomes
Monóxido de lítio
Identificadores
Número CAS
12057-24-8
PubChem
166630
Número RTECS
OJ6360000
Propriedades
Fórmula molecular
Li2 O
Massa molar
29.88 g/mol
Aparência
pó branco granulado
Densidade
2,01 g·cm–3 [ 1]
Ponto de fusão
1427 °C[ 1]
Solubilidade em água
decompõe-se[ 1] [ carece de fontes ] [ carece de fontes ]
log P
9.23
Índice de refracção (n D )
1.644[ 2]
Estrutura
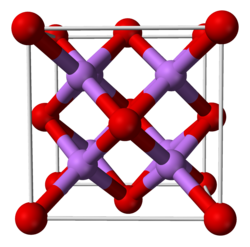
Estrutura cristalina
Antifluorite (cubic), cF12
Grupo de espaço
Fm3 m, No. 225
Geometria de
Tetrahedral (Li+ ); cubic (O2– )
Termoquímica
Entalpia padrão Δf H o 298
-20.01 kJ/g
Capacidade calorífica C p 298
18.105 J/g K
Riscos associados
Índice UE
Não listado
Principais riscos
Corrosivo, reage violentamente com água
Frases R
R34
Frases S
S26 S36/37/39 S45
Ponto de fulgor
Não inflamável
Compostos relacionados
Outros aniões /ânions
Sulfeto de lítio Fluoreto de lítio Nitreto de lítio
Outros catiões /cátions
Óxido de sódio Óxido de potássio Óxido de rubídio Óxido de césio Óxido de berílio
Compostos relacionados
Peróxido de lítio Superóxido de lítio Hidróxido de lítio
Página de dados suplementares
Estrutura e propriedades
n εr , etc.
Dados termodinâmicos
Phase behaviour
Dados espectrais
UV , IV , RMN , EM
Exceto onde denotado, os dados referem-se acondições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa .Alerta sobre risco à saúde .
Óxido de lítio 2 O ) ou lítia é um composto químico inorgânico .
Produção Óxido de lítio é formado quando o lítio é queimado ao ar e combina-se com o oxigênio , ou pela decomposição térmica do peróxido de lítio ou do hidróxido de lítio :
[ 3] [ 4]
4
L
i
+
O
2
⟶
2
L
i
2
O
{\displaystyle \mathrm {4\ Li+O_{2}\longrightarrow \ 2\ Li_{2}O} }
2
L
i
2
O
2
→
195
∘
C
2
L
i
2
O
+
O
2
{\displaystyle \mathrm {2\ Li_{2}O_{2}{\xrightarrow {195^{\circ }C}\ 2\ Li_{2}O\ +O_{2} }
2
L
i
O
H
⟶
L
i
2
O
+
H
2
O
{\displaystyle \mathrm {2\ LiOH\longrightarrow Li_{2}O+H_{2}O} }
Usos Óxido de lítio é usado como um fundente em esmaltes cerâmicos; e cria colorações azuis com cobre e rosas com cobalto . Óxido de lítio reage com água e vapor e deve ser isolado deles.
Seu uso está também sendo investigado para valorações em espectroscopia de monitoramento de degradação de emissão não-destrutiva com sistemas de revestimento de barreira térmica. Ele pode ser adicionado como um co-dopante com ítria na cerâmica de zircônia para alto revestimento, sem um grande decréscimo na expectativa de vida em serviço do revestimento. A alta temperatura, o óxido de lítio emite um padrão espectral muito detectável, o qual aumenta em intensidade ao longo da degradação do revestimento. Implementação permitiria monitoramento in situ de tais sistemas, possibilitando um eficiente meio para predizer tempo de vida até a falha ou necessária manutenção.
Ver também Referências
↑ a b c Base de dados Óxido de lítio
↑ Pradyot Patnaik. Handbook of Inorganic Chemicals . McGraw-Hill, 2002, ISBN 0-07-049439-8
↑ A. F. Holleman, E. Wiberg, N. Wiberg, Lehrbuch der Anorganischen Chemie. 101. Auflage, de Gruyter, 1995, ISBN 3-11-012641-9 , S. 1152.
↑ Georg Brauer (1978). Handbuch der Präparativen Anorganischen Chemie . II . [S.l.: s.n.] p. 951. ISBN 3-432-87813-3 Ligações externas
The article is a derivative under the Creative Commons Attribution-ShareAlike License .
A link to the original article can be found here and attribution parties here
By using this site, you agree to the Terms of Use . Gpedia ® is a registered trademark of the Cyberajah Pty Ltd