Dissulfeto de hidrogênio
| Dissulfeto de hidrogênio Alerta sobre risco à saúde | |
|---|---|

|
|
| Nome IUPAC | Dissulfeto de hidrogênio |
| Outros nomes | Hidrogênio polissulfeto |
| Propriedades | |
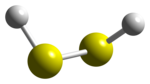
| Fórmula molecular | H2S2 |
| Aparência | Líquido incolor |
| Densidade | 1,33 g/cm³ |
| Ponto de fusão |
-89,6 °C |
| Ponto de ebulição |
70.7 °C, 344 K, 159 °F |
| Riscos associados | |
| Classificação UE | Altamente Inflamável (F+) Muito Tóxico (T+) Perigoso para o meio ambiente (N) |
| Ponto de fulgor | Líquido inflamável |
| Compostos relacionados | |
| Outros aniões/ânions | Peróxido de hidrogênio |
| Compostos relacionados | Sulfeto de hidrogênio (H2S) Trissulfano (H2S3) Polissulfanos (H2Sx, x > 1) |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
Dissulfeto de hidrogênio é um composto inorgânico, na qual este também se identifica pela fórmula H2S2. Ele é um líquido incolor, extremamente instável, e tem um cheiro desagradável parecido com o sulfeto de hidrogênio (H2S). O dissulfeto de hidrogênio pode, através de - alterações artificiais do clima do local específico, ser redefinido como um composto gasoso. Porém mesmo assim, ele continua instável nesta forma.
O dissulfeto de hidrogênio, por ter uma instabilidade específica, decompõe-se rapidamente em sulfeto de hidrogênio, enxofre[1] ou por função de diversos outros fatores.
Uso
Dissulfeto de hidrogênio pode ser usado para separar água pesada de água normal, ou até mesmo, fazer água pesada para usinas nucleares.
O dissulfeto de hidrogênio pode ter também um posicionamento muito importante na área da agricultura, onde pode ser usado como um desinfetante nesta.
Metodologia para obtê-lo ou encontra-lo
O dissulfeto de hidrogênio, por sempre buscar se-decompor rapidamente, é rapidamente desfeito após eventos naturais, fazendo com que este seja um produto transitório durante esses eventos, e por isso é quase impossível encontra-lo. E normalmente é feito através de laboratórios: oxidando os compostos de enxofre e reduzindo-os até dissulfeto de hidrogênio.
Riscos
A decomposição do dissulfeto de hidrogênio é exotérmica, e pode liberar vapores tóxicos. É recomendado que o indivíduo sempre opte por preparar-se com uma roupa adequada, pois a inalação ou contato com o dissulfeto de hidrogênio pode ser radicalmente perigoso, e dependendo da concentração pode ser fatal.
O dissulfeto de hidrogênio deve ser manuseado corretamente para evitar o contato deste em eventos ou objetos que podem causar fogo, pois ele é extremamente inflamável.
E é necessário que ele fique incluído em lugares adequados e apenas nestes, pois ele pode poluir o meio ambiente.
Referências
- ↑ Factories, India Office of the Chief Adviser (1959). Survey of carbon disulphide, hydrogen sulphide, and sulphur dioxide hazards in the viscose rayon industry in India. [New Delhi]: Office of the Chief Adviser, Factories