Acid formic
| Acid formic | |
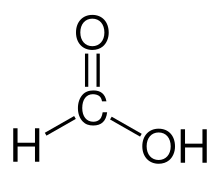 | |
 | |
 Acid formic 85% | |
| Nume IUPAC | Acid formic |
|---|---|
| Alte denumiri | Acid metanoic |
| Identificare | |
| Număr CAS | 64-18-6 |
| ChEMBL | CHEMBL116736 |
| PubChem CID | 18971002 284, 18971002 |
| Informații generale | |
| Formulă chimică | CH2O2 |
| Masă molară | 46,03 g/mol |
| Proprietăți | |
| Densitate | 1,22 g/cm3 |
| Starea de agregare | lichidă |
| Punct de topire | 8 °C |
| Punct de fierbere | 100,8 °C (se descompune) |
| Solubilitate | bună în apă, etanol și glicol |
| Presiune de vapori | 28 hPa |
| Indice de refracție(nD) | 1,3714 |
| Viscozitate | dinamică 0,16 poiseuille |
| Sunt folosite unitățile SI și condițiile de temperatură și presiune normale dacă nu s-a specificat altfel. | |
| Modifică date / text | |
Acidul formic (nume sistematic: acid metanoic) este acidul carboxilic care are formula chimică H-COOH. Acidul formic se folosește ca solvent organic în industrie, la fabricarea insecticidelor și în industria tăbăcăriei. Sărurile sale se numesc formiați, un exemplu fiind formiatul de sodiu.
Obținere
Acidul formic se poate obține, în doi pași, prin reacția dintre hidroxid de sodiu și monoxid de carbon și acidulare cu acid sulfuric:
Se mai poate obține concomitent cu dioxid de carbon prin încălzirea rapidă a acidului oxalic la peste 200 °C[2]
Reacții
Acest acid este un compus agent reducător. Este oxidat de permanganat:
- ; în prezență de H2SO4;
Utilizare
Poate fi folosit în oxidare electrochimică în pile de combustie cu acid formic.
Note
- ^ „acid formic”, formic acid (în engleză), PubChem, accesat în
- ^ Nenițescu, ediția a VIII-a (1980), p. 758
Bibliografie
- C. D. Nenițescu, Chimie organică, ediția a VIII-a, vol I, Editura Didactică și Pedagogică, București, 1980
| ||||||||

![{\displaystyle HCOOH+[O]\longrightarrow CO_{2}+H_{2}O}](https://wikimedia.org/api/rest_v1/media/math/render/svg/0d0ca8dc35afe6838a0b593e211ef027dccbcbf8)

