叠氮化银
| 叠氮化银 | |
|---|---|

| |
| 识别 | |
| CAS号 | 13863-88-2 |
| PubChem | 61698 |
| ChemSpider | 55601 |
| SMILES |
|
| InChI |
|
| InChIKey | QBFXQJXHEPIJKW-UHFFFAOYAJ |
| 性质 | |
| 化学式 | AgN3 |
| 摩尔质量 | 149.888 g·mol⁻¹ |
| 外观 | 白色固体,见光分解为紫黑色 |
| 密度 | 4.42 g/cm3 (固体) |
| 熔点 | 252 °C |
| 沸点 | 297 °C |
| 溶解性(其他溶剂) | 2.0 x 10-8 g/L |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
叠氮化银(化学式:AgN3),白色固体,难溶于水和碱液,可溶于稀硝酸,具爆炸性。 爆炸温度300℃。
制取
- AgNO3(𝑎𝑞) + NaN3(𝑎𝑞) → AgN3(𝑠) + NaNO3(𝑎𝑞)
叠氮酸与硝酸银在溶液中的反应非常灵敏,可以用来检验溶液中少于百万分之一的叠氮酸。联胺可以从硝酸银溶液中沉淀叠氮化银,也可以将银(Ⅰ)还原为单质银。
性质
该化合物不稳定,温度高于250°C时分解放出氮气,高于300°C时就会爆炸性分解为银和氮气:
- 2 AgN3(𝑠) → 3 N2(𝑔) + 2 Ag(𝑠)
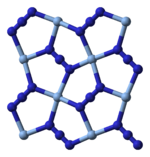
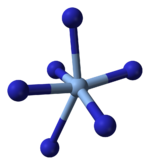
X射线晶体学显示AgN3中的银为平面正方形配位,与四个叠氮配体相连,并且每个叠氮配体以另一端与两个银配位,形成配位聚合物型的层状结构,层间有微弱的Ag-N作用。也可以认为Ag+是以4+2的高度变形八面体型与同一平面的4个叠氮根和上下平面的2个叠氮根配位,而叠氮根则在两端分别以2+1的形式与银离子配位。[1]
 |
 |
 |
 |
参见
参考资料
- ^ Schmidt, C. L. Dinnebier, R.; Wedig, U.; Jansen, M. Crystal Structure and Chemical Bonding of the High-Temperature Phase of AgN3. Inorganic Chemistry. 2007, 46: 907–916. doi:10.1021/ic061963n.