துத்தநாக குளோரைடு

| |
| |
| பெயர்கள் | |
|---|---|
| ஐயூபிஏசி பெயர்
துத்தநாக குளோரைடு
| |
| வேறு பெயர்கள்
துத்தநாக(II)குளோரைடு
துத்தநாக டைகுளோரைடு | |
| இனங்காட்டிகள் | |
| 7646-85-7 | |
| ATC code | B05XA12 |
| ChEBI | CHEBI:49976 |
| ChEMBL | ChEMBL1200679 |
| ChemSpider | 5525 |
| EC number | 231-592-0 |
| யேமல் -3D படிமங்கள் | Image |
| பப்கெம் | 3007855 |
| வே.ந.வி.ப எண் | ZH1400000 |
| |
| UNII | 86Q357L16B |
| UN number | 2331 |
| பண்புகள் | |
| ZnCl2 | |
| வாய்ப்பாட்டு எடை | 136.315 g/mol |
| தோற்றம் | white crystalline solid நீர் உறிஞ்சும் திறன் and very deliquescent |
| மணம் | odorless |
| அடர்த்தி | 2.907 g/cm3 |
| உருகுநிலை | 292 °C (558 °F; 565 K) |
| கொதிநிலை | 756 °C (1,393 °F; 1,029 K) |
| 4320 g/L (25 °C) | |
| கரைதிறன் | soluble in எத்தனால், கிளிசரால் and அசிட்டோன் |
| மதுசாரம்-இல் கரைதிறன் | 4300 g/L |
| கட்டமைப்பு | |
| ஒருங்கிணைவு வடிவியல் |
நான்முக முக்கோணகம், linear in the gas phase |
| தீங்குகள் | |
| பொருள் பாதுகாப்பு குறிப்பு தாள் | External MSDS |
| ஈயூ வகைப்பாடு | Harmful (Xn) Corrosive (C) Dangerous for the environment (N) |
| R-சொற்றொடர்கள் | R22, R34, R50/53 |
| S-சொற்றொடர்கள் | (S1/2), S26, S36/37/39, S45, S60, S61 |
| Lethal dose or concentration (LD, LC): | |
LD50 (Median dose)
|
350 mg/kg, rat (oral) |
| தொடர்புடைய சேர்மங்கள் | |
| ஏனைய எதிர் மின்னயனிகள் | துத்தநாக புளோரைட்டு துத்தநாக புரோமைடு துத்தநாக அயோடைடு |
| ஏனைய நேர் மின்அயனிகள் | காட்மியம் குளோரைடு Mercury(II) chloride |
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |
துத்தநாக குளோரைடு (Zinc Chloride) என்பது ZnCl2 என்ற மூலக்கூறு வாய்பாடு கொண்ட ஒரு வேதியியல் சேர்மமாகும். ஒன்பது விதமான படிக வடிவங்களில் காணப்படும் இவ்வுப்பு நிறமற்றதாகவோ வெள்ளை நிறத்திலோ இருக்கிறது. எளிதில் நீரில் கரையக்கூடிய துத்தநாக குளோரைடு தானே நீர்த்துப் போகக்கூடியதாகவும் நீரை உறிஞ்சும் தன்மையும் கொண்டுள்ளது. எனவே இதனுடைய உப்பு மாதிரிகள் சுற்றுச் சூழல் காற்றின் ஈரப்பதத்தில் இருந்தும் பாதுகாப்பாக வைக்கப்படுகின்றன. துத்தநாக குளோரைடு நெசவு பதப்படுத்தும் தொழில், உலோகவியல் மற்றும் வேதிப்பொருட்களை உற்பத்தி செய்யும் வேதித் தொகுப்பு முதலியவற்றில் பரவலாக பயன்படுகிறது. மிக அரிதாக கிடைக்கும் Zn5(OH)8CL2 என்ற சைமன் கோலைட் என்ற தாதுப் பொருளில் துத்தநாக குளோரைடு பகுதிப்பொருளாகக் காணப்படுகிறது.
அமைப்பும் பண்புகளும்
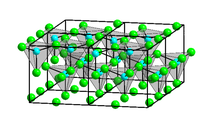
நான்கு வேறுபட்ட பண்முக படிக வடிவங்களில் துத்தநாக குளோரைடு அறியப்படுகிறது. அவை α, β, γ, மற்றும் δ, என்பனவாகும். ஒவ்வொரு வகையிலும் Zn2+ அயனிகள் நான்கு முகங்களிலும் குளோரைடு அயனிகளுடன் இணைந்துள்ளன[1].
கீழே உள்ள அட்டவணையில் a, b, c ஆகியன புறஅளவு மாறிலிகளையும். Z ஒவ்வொரு அலகு செல்லுக்கும் நிகரான கட்டமைப்பு அளவுருக்களையும் ρ என்பது கணக்கிடப்பட்ட கட்டமைப்பு உருவளவுகளின் அடர்த்தியையும் குறிக்கின்றன[2][3][4] .
நீரற்ற தூய சாய்சதுரபடிக வடிவக் துத்தநாக குளோரைடு (δ) சுற்றுச்சூழல் ஈரப்பதத்தால் பாதிக்கப்பட்டு மற்ற படிக வடிவங்களுக்கு வேகமாக மாறிவிடுகிறது. உறிஞ்சப்பட்ட நீரில் உள்ள OH அயனிகள் இந்த மாற்றத்தை நிகழ்த்துகின்றன என்று விளக்கமளிப்பது சாத்தியமாகிறது[1] உருகிய துத்தநாக குளோரைடு விரைவாக குளிர்ச்சியடைந்து படிக வடிவமில்லாத திடமான கண்ணாடியைக் கொடுக்கிறது. இத்திறன் உருகும் திரவத்தில் உள்ள படிக அமைப்பால் நிகழ்கிறது [5].
நீரற்ற உப்பின் சகப்பிணைப்புத் தன்மையை அதனுடைய குறைவான 2750 செல்சியஸ்[6] உருகுநிலை சுட்டிக்காட்டுகிறது. ஈதர் கரைப்பானில் இதனுடைய அதிக கரைதிறன் சக இணைப்பிற்கான கூடுதலான ஆதாரமாகிறது. ஈத்தரில் துத்தநாக குளோரைடு கரையும் போது ZnCl2L2 என்ற மூலக்கூறு வாய்பாடு கொண்ட கூட்டு விளைபொருளாக உருவாகிறது. இங்கு L என்பது ஈந்தணைவியான O(C2H5)2. ஐ குறிக்கிறது.
வாயு நிலையில் துத்தநாக குளோரைடு மூலக்கூறுகள் பிணைப்பின் நீளம் 205 pm [7] கொண்ட நேர் கோடு வடிவமைப்பில் உள்ளன. உருகிய ZnCl2 அதன் உருகுநிலையில் உயர் பாகுநிலையிலும் ஒப்பீட்டளவில் குறைந்த மின் கடத்தியாக வெப்பநிலையை[7][8] குறிப்பிடும்படியாக அதிகரிக்கிறது. உருகலில் ப்ல்பகுதி அமைப்பு முறை[9] காணப்படுகிறது என ராமன் சிதறல் ஆய்வும் நான்முகத் தொகுப்பு வடிவமைப்பு முறை காணப்படுவதாக நியூத்திரன் சிதறல் ஆய்வும் [10] சுட்டிக்காட்டுகின்றன.
நீரேறிகள்
துத்தநாக குளோரைடின் ZnCl2(H2O)n ஐந்து நீரேறிகள் கண்டறியப்பட்டுள்ளன. இங்கு n = 1,1.5,2.5,3 மற்றும் 4 ஆகும் [11]. நான்முக வடிவமைப்பு நீரேறி ZnCl2(H2O)4 துத்தநாக குளோரைடு கரைசலில் இருந்து கெட்டியாகிவிடுகிறது [11].
தயாரிப்பும் தூய்மையாக்கலும்
துத்தநாகம் மற்றும் ஐதரசன் குளோரைடு வினை புரிவதால் நீரற்ற துத்தநாக குளோரைடு கிடைக்கிறது. இதைப்போலவே நீரேறிகளையும் நீர்த்த கரைசல்களையும் துத்தநாக உலோகத்துடன் ஐதரோகுளோரிக் காடி சேர்த்து தயாரித்துக் கொள்ளலாம்.
- Zn(s) + 2 HCl → ZnCl2 + H2(g)
துத்தநாக ஆக்சைடு மற்றும் துத்தநாக சல்பைடு சேர்மங்கள் ஐதரோகுளோரிக் காடியுடன் வினை புரிவதாலும் துத்தநாக குளோரைடு பெறலாம்.
- ZnS(s) + 2 HCl(aq) → ZnCl2(aq) + H2S(g)
| வடிவம் | சமச்சீர் | பியர்சன் குறியீடு | தொகுதி | எண் | a (nm) | b (nm) | c (nm) | Z | ρ (g/cm3) |
|---|---|---|---|---|---|---|---|---|---|
| α | நாற்கோணகம் | tI12 | I42d | 122 | 0.5398 | 0.5398 | 0.64223 | 4 | 3.00 |
| β | நாற்கோணகம் | tP6 | P42/nmc | 137 | 0.3696 | 0.3696 | 1.071 | 2 | 3.09 |
| γ | ஒற்றைச் சரிவு | mP36 | P21c | 14 | 0.654 | 1.131 | 1.23328 | 12 | 2.98 |
| δ | சாய்சதுரம் | oP12 | Pna21 | 33 | 0.6125 | 0.6443 | 0.7693 | 4 | 2.98 |
மற்ற தனிமங்களைப் போலல்லாமல் துத்தநாகம் 2+ என்ற ஒரே ஆக்சிசனேற்ற நிலையில் இருப்பதால் குளோரைடை தூய்மைப்படுத்துவது எளிமையகிறது.துத்தநாக குளோரைடு வணிக மாதிரிகள் பொதுவாக தண்ணீர் மற்றும் நீராற் பகுத்தலில் விளையும் அசுத்தப் பொருட்களைக் கொண்டிருக்கின்றன. இத்தகைய மாதிரிகள் ஈரொட்சேனை மறு படிக்மாக்குதல் மூலம் சுத்திகரிக்கலாம். நீரற்ற மாதிரிகளை ஐதரசன் குளோரைடு வளிமக் கற்றையில் பதங்கமாதலுக்கு உட்படுத்தி பின்னர் இதை 400 °C அளவுக்கு உலர் [[நைதரசன் வளிமம| நைதரசன் வளிமக் கற்றையில் சூடாக்கப்படுகிறது. இறுதியாக துத்தநாக குளோரைடை தையோனில் குளோரைடுடன்[12] சேர்த்து சூடாக்குவதன் மூலம் தூய்மைப்படுத்தப்படுகிறது.
மேற்கோள்கள்
- ↑ 1.0 1.1 Wells, A. F. (1984). Structural Inorganic Chemistry. Oxford: Clarendon Press. பன்னாட்டுத் தரப்புத்தக எண் 0-19-855370-6.
- ↑ Oswald, H. R.; Jaggi, H. (1960). "Zur Struktur der wasserfreien Zinkhalogenide I. Die wasserfreien Zinkchloride". Helvetica Chimica Acta 43 (1): 72–77. doi:10.1002/hlca.19600430109.
- ↑ Brynestad, J.; Yakel, H. L. (1978). "Preparation and Structure of Anhydrous Zinc Chloride". Inorganic Chemistry 17 (5): 1376–1377. doi:10.1021/ic50183a059.
- ↑ Brehler, B. (1961). "Kristallstrukturuntersuchungen an ZnCl2". Zeitschrift für Kristallographie 115 (5-6): 373–402. doi:10.1524/zkri.1961.115.5-6.373.
- ↑ Mackenzie, J. D.; Murphy, W. K. (1960). "Structure of Glass-Forming Halides. II. Liquid Zinc Chloride". The Journal of Chemical Physics 33 (2): 366–369. doi:10.1063/1.1731151.
- ↑ Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann. பன்னாட்டுத் தரப்புத்தக எண் 0080379419.
- ↑ 7.0 7.1 Prince, R. H. (1994). King, R. B. (ed.). Encyclopedia of Inorganic Chemistry. John Wiley & Sons. பன்னாட்டுத் தரப்புத்தக எண் 0-471-93620-0.
- ↑ Ray, H. S. (2006). Introduction to Melts: Molten Salts, Slags and Glasses. Allied Publishers. பன்னாட்டுத் தரப்புத்தக எண் 81-7764-875-6.
- ↑ Danek, V. (2006). Physico-Chemical Analysis of Molten Electrolytes. Elsevier. பன்னாட்டுத் தரப்புத்தக எண் 0-444-52116-X.
- ↑ Price, D. L.; Saboungi, M.-L.; Susman, S.; Volin, K. J.; Wright, A. C. (1991). "Neutron Scattering Function of Vitreous and Molten Zinc Chloride". Journal of Physics: Condensed Matter 3 (49): 9835–9842. doi:10.1088/0953-8984/3/49/001.
- ↑ 11.0 11.1 Holleman, A. F.; Wiberg, E. (2001). Inorganic Chemistry. San Diego: Academic Press. பன்னாட்டுத் தரப்புத்தக எண் 0-12-352651-5.
{cite book}: CS1 maint: multiple names: authors list (link) - ↑ Pray, A. P. (1990). Inorganic Syntheses. Vol. 28. New York: J. Wiley & Sons. pp. 321–322. பன்னாட்டுத் தரப்புத்தக எண் 0-471-52619-3. Describes the formation of anhydrous LiCl, CuCl2, ZnCl2, CdCl2, ThCl4, CrCl3, FeCl3, CoCl2, and NiCl2 from the corresponding hydrates.
| குளோரைடுகள் | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| HCl | He | ||||||||||||||||||
| LiCl | BeCl2 | BCl3 B2Cl4 |
CCl4 | NCl3 ClN3 |
Cl2O ClO2 Cl2O7 |
ClF ClF3 ClF5 |
Ne | ||||||||||||
| NaCl | MgCl2 | AlCl AlCl3 |
SiCl4 | P2Cl4 PCl3 PCl5 |
S2Cl2 SCl2 SCl4 |
Cl2 | Ar | ||||||||||||
| KCl | CaCl CaCl2 |
ScCl3 | TiCl2 TiCl3 TiCl4 |
VCl2 VCl3 VCl4 VCl5 |
CrCl2 CrCl3 CrCl4 |
MnCl2 | FeCl2 FeCl3 |
CoCl2 CoCl3 |
NiCl2 | CuCl CuCl2 |
ZnCl2 | GaCl2 GaCl3 |
GeCl2 GeCl4 |
AsCl3 AsCl5 |
Se2Cl2 SeCl4 |
BrCl | KrCl | ||
| RbCl | SrCl2 | YCl3 | ZrCl3 ZrCl4 |
NbCl4 NbCl5 |
MoCl2 MoCl3 MoCl4 MoCl5 MoCl6 |
TcCl4 | RuCl3 | RhCl3 | PdCl2 | AgCl | CdCl2 | InCl InCl2 InCl3 |
SnCl2 SnCl4 |
SbCl3 SbCl5 |
Te3Cl2 TeCl4 |
ICl ICl3 |
XeCl XeCl2 | ||
| CsCl | BaCl2 | HfCl4 | TaCl5 | WCl2 WCl3 WCl4 WCl5 WCl6 |
Re3Cl9 ReCl4 ReCl5 ReCl6 |
OsCl4 | IrCl2 IrCl3 IrCl4 |
PtCl2 PtCl4 |
AuCl AuCl3 |
Hg2Cl2, HgCl2 |
TlCl | PbCl2, PbCl4 |
BiCl3 | PoCl2, PoCl4 |
AtCl | RnCl2 | |||
| FrCl | RaCl2 | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |||
| ↓ | |||||||||||||||||||
| LaCl3 | CeCl3 | PrCl3 | NdCl2, NdCl3 |
PmCl3 | SmCl2, SmCl3 |
EuCl2, EuCl3 |
GdCl3 | TbCl3 | DyCl2, DyCl3 |
HoCl3 | ErCl3 | TmCl2 TmCl3 |
YbCl2 YbCl3 |
LuCl3 | |||||
| AcCl3 | ThCl4 | PaCl5 | UCl3 UCl4 UCl5 UCl6 |
NpCl4 | PuCl3 | AmCl2 AmCl3 |
CmCl3 | BkCl3 | CfCl3 | EsCl3 | Fm | Md | No | LrCl3 | |||||