Cerium(IV) oksida

| |
| |
| Nama | |
|---|---|
| Nama IUPAC
Serium(IV) oksida
| |
| Nama lain
Seri oksida,
Ceria, Serium dioksida | |
| Penanda | |
| |
Model 3D (JSmol)
|
|
| 3DMet | {3DMet} |
| ChEBI | |
| ChemSpider | |
| Nomor EC | |
PubChem CID
|
|
| Nomor RTECS | {value} |
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| |
| Sifat | |
| CeO2 | |
| Massa molar | 172,115 g/mol |
| Penampilan | padatan putih atau kuning pucat, agak hidroskopis |
| Densitas | 7,215 g/cm3 |
| Titik lebur | 2.400 °C (2.670 K) |
| Titik didih | 3.500 °C (3.770 K) |
| tidak larut | |
| +26,0·10−6 cm3/mol | |
| Struktur | |
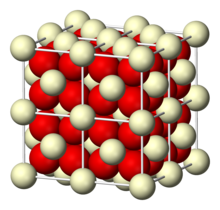
| kubus (fluorit)[1] | |
| Bahaya | |
| Senyawa terkait | |
Senyawa terkait
|
Serium(III) oksida |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
Serium(IV) oksida, juga dikenal sebagai seri oksida, seri dioksida, seria, serium oksida atau serium dioksida, adalah oksida logam logam tanah jarang serium. Ia adalah bubuk kuning putih pucat dengan rumus kimia CeO2. Ia adalah produk komersial penting dan perantara dalam pemurnian unsur Ce dari bijihnya. Sifat khas dari bahan ini adalah konversi reversibelnya menjadi oksida nonstoikiometri.[2]
Produksi
Cerium terjadi secara alami sebagai campuran dengan unsur tanah jarang lainnya dalam bijih utamanya bastnaesit dan monazit. Setelah ekstraksi ion logam dalam larutan basa, Ce dipisahkan dari campuran tersebut dengan penambahan suatu oksidator yang diikuti dengan penyesuaian pH. Langkah ini mengeksploitasi rendahnya kelarutan CeO2 dan fakta bahwa unsur tanah jarang lainnya tidak teroksidasi.[2]
Cerium(IV) oksida dibentuk melalui kalsinasi dari cerium oksalat atau cerium hidroksida.
Cerium juga membentuk cerium(III) oksida, Ce, yang tidak stabil yang akan teroksidasi menjadi cerium(IV) oksida.[3]
Perilaku struktur dan defek
Cerium oksida mengadopsi struktur fluorit, grup ruang Fm3m, #225 yang mengandung 8 koordinasi Ce4+ dan 4 koordinasi O2−. Pada suhu tinggi ia melepaskan oksigen untuk menghasilkan suatu bentuk non-stoikiometris yang kekurangan anion yang mempertahankan kisi fluorit. Bahan ini memiliki rumus CeO(2-x) dengan 0 < < 0,28.[4] Nilai bergantung pada suhu maupun tekanan parsial oksigen. Persamaan
telah ditunjukkan untuk memprediksi kesetimbangan non stoikiometri pada berbagai tekanan parsial oksigen (103 − 10−4 Pa) dan suhu (1000−1900 °C).[5]
Bentuk non stoikiometri memiliki warna biru sampai hitam, dan menunjukkan konduksi ionik dan elektronik dengan ion yang paling signifikan pada suhu > 500 °C.[6]
Jumlah kekosongan oksigen sering diukur dengan menggunakan spektroskopi fotoelektron sinar-X untuk membandingkan rasio Ce terhadap Ce.
Kimia defek
Pada ceria fase fluorit yang paling stabil, ia menunjukkan beberapa cacat tergantung pada tekanan parsial oksigen atau keadaan tegangan material.[7][8]
Cacat utama yang menjadi perhatian adalah kekosongan oksigen dan polaron kecil (elektron dilokalisasi pada kation cerium). Peningkatan jumlah defek oksigen meningkatkan laju difusi oksida dalam kisi sebagaimana tercermin dalam peningkatan konduktivitas ionik. Faktor-faktor ini merekomendasikan ceria sebagai elektrolit padat dalam sel bahan bakar oksida padat. Ceria yang tak didoping maupun didoping sama-sama menunjukkan konduktivitas elektronik yang tinggi pada tekanan parsial oksigen yang rendah karena reduksi ion serium yang menyebabkan pembentukan polaron kecil. Karena atom oksigen dalam kristal ceria terjadi pada bidang datar, difusi anion ini bersifat halus. Tingkat difusi meningkat seiring peningkatan konsentrasi defek.
Aplikasi pemolesan
Aplikasi utama ceria adalah untuk pemolesan, terutama planarisasi kimia-mekanik (chemical-mechanical planarisation, CMP).[2] Untuk tujuan ini, ia telah menggantikan banyak oksida lainya yang telah digunakan terlebih dahulu, seperti besi oksida dan zirkonia.[9] [10]
Kegunaan lain
CeO2 digunakan untuk menghilangkan warna kaca dengan mengubah ketakmurnian ferro yang berwarna hijau menjadi ferri oksida yang hampir tak berwarna.[2]
Cerium oksida telah dijumpai digunakan dalam filter inframerah, sebagai suatu oksidator dalam konverter katalitik dan sebagai pengganti torium dioksida dalam mantel pijar.[11]
Katalisis
Interkonvertibilitas bahan CeOx adalah dasar penggunaan ceria untuk katalis oksidasi. Satu contoh kecil tetapi dapat memberikan ilustrasi penggunaannya adalah pada dinding oven swaresik sebagai katalis oksidasi hidrokarbon selama proses pembersihan suhu tinggi. Contoh kecil lainnya tetapi terkenal adalah perannya dalam oksidasi gas alam dalam mantel gas.[12]

Ceria telah digunakan sebagai sensor konverter katalitik dalam aplikasi otomotif, mengendalikan rasio gas buang untuk mengurangi NOx dan karbon monoksida.
Konduksi campuran
Oleh karena konduksi ionik dan listrik cerium dioksida cukup signifikan, maka ia cocok digunakan sebagai konduktor campuran.[13]
Penelitian
Sel bahan bakar
Ceria adalah bahan yang menarik untuk digunakan sebagai sel bahan bakar oksida padat (bahasa Inggris: solid oxide fuel cell, (SOFC)) karena konduktivitas ion oksigennya yang relatif tinggi (yaitu, atom-atom oksigen mudah bergerak melewatinya) pada suhu sedang (500–650 °C) dan entalpi asosiasi yang lebih rendah daripada sistem Zirkonia.[14]
Pemisahan air
Siklus cerium(IV) oksida–cerium(III) oksida atau siklus CeO/Ce adalah proses pemisahan air secara termokimia dua tahap, yang mendasarkan pada cerium(IV) oksida dan cerium(III) oksida untuk produksi hidrogen.[15]
Referensi
- ^ Pradyot Patnaik. Handbook of Inorganic Chemicals. McGraw-Hill, 2002, ISBN 0-07-049439-8
- ^ a b c d Reinhardt, K.; Winkler, H. (2000), "Cerium Mischmetal, Cerium Alloys, and Cerium Compounds", Ullmann's Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, doi:10.1002/14356007.a06_139
- ^ Thermodynamic data Diarsipkan October 29, 2013, di Wayback Machine.
- ^ William Hayes, A.M. Stoneham (2004), Defects and Defect Processes in Nonmetallic Solids, Dover Publications, ISBN 978-0486434834
- ^ Bulfin, B.; Lowe, A. J.; Keogh, K. A.; Murphy, B. E.; Lübben, O.; Krasnikov, S. A.; Shvets, I. V. (2013). "Analytical Model of CeO2 Oxidation and Reduction". The Journal of Physical Chemistry C. 117 (46): 24129–24137. doi:10.1021/jp406578z.
- ^ Ghillanyova, K; Galusek, D (2011). "Chapter 1: Ceramic oxides". Dalam Riedel, Ralf; Chen, I-Wie. Ceramics Science and Technology, Materials and Properties, vol 2. John Wiley & Sons. ISBN 978-3-527-31156-9.
- ^ Munnings,, C; SPS Badwal; D Fini (2014). "Spontaneous stress-induced oxidation of Ce ions in Gd-doped ceria at room temperature". Ionics. 20 (8): 1117–1126. doi:10.1007/s11581-014-1079-2.
- ^ Badwal, SPS; Daniel Fini; Fabio Ciacchi; Christopher Munnings; Justin Kimpton; John Drennan (2013). "Structural and microstructural stability of ceria – gadolinia electrolyte exposed to reducing environments of high temperature fuel cells". J. Mater. Chem. A. 1 (36): 10768. doi:10.1039/C3TA11752A.
- ^ Properties of Common Abrasives (Boston Museum of Fine Arts)
- ^ MFA Materials database.
- ^ Cerium dioxide Diarsipkan 2013-03-02 di Wayback Machine.. nanopartikel.info
- ^ Greenwood, Norman N.; Earnshaw, A. (1997), Chemistry of the Elements (edisi ke-2), Oxford: Butterworth-Heinemann, ISBN 0-7506-3365-4
- ^ "Mixed conductors". Max Planck institute for solid state research. Diakses tanggal 16 September 2016.
- ^ "Electrical conductivity of the ZrO2–Ln2O3 (Ln=lanthanides) system". Solid State Ionics. 121: 133–139. doi:10.1016/S0167-2738(98)00540-2.
- ^ Hydrogen production from solar thermochemical water splitting cycles Diarsipkan August 30, 2009, di Wayback Machine.. solarpaces.org

![{\displaystyle {\Bigg (}{\frac {x}{0.35-x}{\Bigg )}=106000\,\,[\mathrm {Pa} ^{0.217}]\times P_{O_{2}^{\,\,-0.217}\exp {\Bigg (}{\frac {-195.6\,\,[\mathrm {k\,J\,mol} ^{-1}]}{RT}{\Bigg )}](https://wikimedia.org/api/rest_v1/media/math/render/svg/e9870811c9ad406d2fa67ef509d3b0269aebd608)