แก๊สมีสกุล
| แก๊สมีสกุล | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||
| ↓ คาบ | |||||||||||
| 1 | ฮีเลียม (He) 2 | ||||||||||
| 2 | นีออน (Ne) 10 | ||||||||||
| 3 | อาร์กอน (Ar) 18 | ||||||||||
| 4 | คริปตอน (Kr) 36 | ||||||||||
| 5 | ซีนอน (Xe) 54 | ||||||||||
| 6 | เรดอน (Rn) 86 | ||||||||||
| 7 | โอกาเนสซอน (Og) 118 | ||||||||||
|
คำอธิบาย
| |||||||||||
แก๊สมีสกุล หรือ แก๊สมีตระกูล (ในอดีตเรียกว่า แก๊สเฉื่อย หรือบางครั้งใช้ชื่อว่า aerogens[1]) เป็นกลุ่มของธาตุทางเคมีที่มีสมบัติคล้ายกัน ภายใต้ภาวะมาตรฐานสำหรับอุณหภูมิและความดันธาตุเหล่านี้ต่างไม่มีกลิ่น ไม่มีสี เป็นแก๊สอะตอมเดี่ยวซึ่งไม่มีความว่องไวต่อปฏิกริยาเคมี แก๊สมีสกุลที่เกิดในธรรมชาติทั้งหกธาตุ ได้แก่ ฮีเลียม (He), นีออน (Ne), อาร์กอน (Ar), คริปทอน (Kr), ซีนอน (Xe) และเรดอน (Rn)
โอกาเนสซอน (Og) เป็นธาตุสังเคราะห์มีความเป็นกัมมันตรังสีสูงมาก แม้ว่า IUPAC จัดโอกาเนสซอนเป็นแก๊สมีสกุลหรือหมู่ที่ 18[2] มันอาจไม่เฉื่อยทางเคมีเหมือนธาตุอื่นในหมู่เดียวกัน และถูกทำนายว่าจะสลายและแผ่กัมมันตรังสีเนื่องจากปรากฏการณ์สัมพัทธ์ เนื่องจากครึ่งชีวิตที่สั้นเพียง 0.7 ไมโครวินาทีของไอโซโทปตัวเดียว ทำให้คุณสมบัติทางเคมีของโอกาเนสซอนยังไม่มีการศึกษามากนัก
สำหรับหกคาบแรกของตารางธาตุ แก๊สมีสกุลเป็นสมาชิกของธาตุหมู่ 18 อย่างแท้จริง แก๊สมีสกุลมักจะไม่ว่องไวต่อปฏิกิริยาเคมีอย่างมาก ยกเว้นภายใต้สภาวะสุดขั้ว ความเฉื่อยของแก๊สมีสกุลทำให้มันสามารถประยุกต์ได้หลากหลาย เนื่องจากความสามารถในการเกิดปฏิกิริยาน้อย เช่นการเติมอาร์กอนในหลอดไส้ร้อนแบบธรรมดาเพื่อป้องกันไม่ให้ไส้หลอดทังสเตนเกิดการออกซิไดส์ และฮีเลียมใช้เติมถังแก๊สสำหรับหายใจสำหรับนักดำน้ำลึก เพื่อป้องกันภาวะเป็นพิษจากแก๊สออกซิเจน แก๊สไนโตรเจนและแก๊สคาร์บอนไดออกไซด์
คุณสมบัติของแก๊สมีสกุลสามารถอธิบายด้วยทฤษฎียุคใหม่ของโครงสร้างอะตอม เปลือกชั้นนอกของเวเลนซ์อิเล็กตรอนเต็ม ทำให้มันมีแนวโน้มน้อยที่เกิดปฏิกิริยาเคมี และสามารถเกิดสารประกอบของแก๊สมีสกุลเพียงร้อยสารประกอบเท่านั้น จุดหลอมเหลวและจุดเดือดมีค่าแตกต่างกันน้อยกว่า 10 องศาเซลเซียส (18 องศาฟาเรนไฮต์) แสดงว่าแก๊สมีสกุลมีสถานะเป็นของเหลวในช่วงอุณหภูมิที่แคบ
นีออน อาร์กอน คริปทอนและซีนอนสามารถแยกออกจากอากาศ ในโรงแยกอากาศด้วยวิธีลิเคอแฟคชันและการกลั่นลำดับส่วน สามารถรวบรวมฮีเลียมได้จากแหล่งแก๊สธรรมชาติ ซึ่งประกอบด้วยฮีเลียมเข้มข้นสูงในแก๊สธรรมชาติ ด้วยเทคนิคการแยกแก๊สแบบอุณหภูมิต่ำ และเรดอนมักแยกจากการสลายให้กัมมันตรังสีของสารประกอบเรเดียม ทอเรียมหรือยูเรเนียม แก๊สมีสกุลสามารถประยุกต์ใช้ในหลายอุตสาหกรรม เช่นหลอดไฟ การเชื่อมและการสำรวจอวกาศ ถังแก๊สฮีเลียม-ออกซิเจนสำหรับหายใจ นิยมใช้ในการดำน้ำลึกที่ความลึก 55 เมตร (180 ฟุต) จากระดับน้ำทะเล หลังจากที่ความเสี่ยงที่เกิดจากความไวไฟของแก๊สไฮโดรเจนเป็นที่แจ่มแจ้งในวินาศภัยฮินเดินบวร์ค จึงแทนที่ไฮโดรเจนด้วยฮีเลียมในเรือเหาะและอื่น ๆ
ประวัติ
แก๊สมีสกุล แปลมาจากคำว่า Edelgas ในภาษาเยอรมัน คำดังกล่าวถูกใช้คำครั้งแรกในปี ค.ศ. 1898 โดยฮิวโก้ เอิร์ดแมนน์[3] เพื่อบ่งบอกถึงระดับความว่องไวต่อปฏิกิริยาที่ต่ำ ตั้งชื่อดังกล่าวด้วยเหตุผลเดียวกับ "โลหะมีสกุล" ซึ่งมีค่าความว่องไวต่อปฏิกิริยาที่ต่ำเช่นเดียวกัน อีกชื่อของแก๊สมีสกุลอย่างแก๊สเฉื่อยไม่ได้รับความนิยมแล้ว เนื่องจากสารประกอบของแก๊สมีสกุลเป็นที่รู้จักมากกว่าเดิม[4] และ แก๊สหายาก ซึ่งเป็นอีกชื่อที่เคยใช้[5] ไม่ถูกต้อง เพราะการสลายตัวของกัมมันตภาพรังสีโพแทสเซียม-40 ทำให้อาร์กอนเป็นส่วนประกอบของบรรยากาศของโลกมากถึง 0.94% โดยปริมาตร และ 1.3% โดยมวล[6]

ปีแยร์ ฌ็องซ็องและนอร์แมน ล็อกเยอร์ค้นพบธาตุใหม่ในวันที่ 18 สิงหาคม ค.ศ. 1868 ขณะมองไปที่ชั้นโครโมสเฟียร์ของดวงอาทิตย์ และตั้งชื่อมันว่าฮีเลียม จากคำว่า ἥλιος (hḗlios)[7] ซึ่งมีความหมายในภาษากรีกว่าดวงอาทิตย์ การวิเคราะห์ทางเคมีที่สามารถพิสูจน์ว่าฮีเลียมเป็นแก๊สมีสกุลเกิดขึ้นในภายหลัง ก่อนการพิสูจน์ดังกล่าว เมื่อปี ค.ศ. 1784 นักเคมีและนักฟิสิกส์ชาวอังกฤษ เฮนรี คาเวนดิชค้นพบสารจำนวนน้อยในอากาศที่มีความว่องไวต่อปฏิกิริยาต่ำกว่าไนโตรเจน[8] ต่อมาในปี ค.ศ. 1895 จอห์น วิลเลียม สตรัทท์ หรือ ลอร์ดเรย์ลี ค้นพบว่าสารไนโตรเจนตัวอย่างจากอากาศมีความหนาแน่นต่างจากไนโตรเจนที่ได้จากปฏิกิริยาเคมี ร่วมกันกับนักวิทยาศาสตร์ชาวสกอตแลนด์ วิลเลียม แรมซีย์จากยูนิเวอร์ซิตีคอลลิจลันเดิน เรย์ลีได้ตั้งทฤษฎีขึ้นว่าไนโตรเจนที่สกัดได้จากอากาศปนเปื้อนกับแก๊สอื่น นำไปสู่การทดลองที่ประสบความสำเร็จในการสกัดธาตุใหม่อย่างอาร์กอน ซึ่งตั้งชื่อจากคำภาษากรีกว่า ἀργός (argós ซึ่งมีความหมายว่า "ไม่ได้ใช้งาน" หรือ "ขี้เกียจ")[8] การค้นพบใหม่ทำให้พวกเขาตระหนักว่ามีแก๊สจำนวนมากหายไปจากตารางธาตุ ในการทดลองเพื่อหาธาตุอาร์กอน แรมซีย์ก็ยังพบวิธีสกัดฮีเลียมเป็นครั้งแรก ขณะให้ความร้อนแก่แร่ธาตุชื่อคลีเวต หลังได้รับหลักฐานการมีอยู่ของธาตุฮีเลียมและอาร์กอน ใน ค.ศ. 1902 ดมีตรี เมนเดเลเยฟได้เพิ่มแก๊สมีสกุลทั้งสองลงในกลุ่มที่ 0 ของลำดับการเรียงธาตุของเขา ภายหลังรู้จักในชื่อตารางธาตุ[9]
แรมซีย์ทำการทดลองหาแก๊สมีสกุลต่อไป ด้วยการใช้วิธีการกลั่นแบบลำดับส่วนในการแยกอากาศเหลวกลายเป็นส่วนประกอบต่างๆ จน ค.ศ. 1898 เขาได้ค้นพบธาตุคริปทอน, นีออน, และซีนอน ซึ่งตั้งชื่อตามคำภาษากรีกว่า κρυπτός (kryptós, "หาย"), νέος (néos, "ใหม่") และ ξένος (ksénos, "แปลก") ตามลำดับ เรดอนถูกค้นพบตั้งแต่ ค.ศ. 1898 โดยฟรีดริช แอ็นสท์ ดอร์น[10] และตั้งชื่อจากการแผ่รังสีเรเดียม แต่เรดอนเพิ่งจัดเป็นแก๊สมีสกุลหลัง ค.ศ. 1904 เมื่อค้นพบว่าคุณสมบัติต่าง ๆ มีลักษณะเหมือนกับแก๊สมีสกุลอื่นๆ [11] เรย์ลีและแรมซีย์ได้รับรางวัลโนเบล ประจำ ค.ศ. 1904 ในสาขาฟิสิกส์และเคมีตามลำดับ จากการค้นพบการมีอยู่ของแก๊สมีสกุล[12][13] เจ. อี. เซเดอร์บลอม นายกราชบัณฑิตยสภาวิทยาศาสตร์แห่งสวีเดนกล่าวไว้ว่า "การค้นพบกลุ่มของธาตุใหม่ทั้งหมด โดยที่ยังไม่มีธาตุใดเป็นต้นแบบของกลุ่มอยู่เลย นับเป็นสิ่งที่ยิ่งใหญ่และมีเอกลักษณ์มากในประวัติศาสตร์ของเคมี สิ่งนี้จะเป็นความก้าวหน้าที่สำคัญต่อการค้นคว้า" การค้นคว้าเกี่ยวกับแก๊สมีสกุลมีส่วนช่วยอย่างมากในการพัฒนาองค์ความรู้ด้านโครงสร้างอะตอม ใน ค.ศ. 1895 นักเคมี ชาวฝรั่งเศส อ็องรี มัวซ็องได้พยายามสร้างปฏิกิริยาเคมีระหว่างฟลูออรีนที่มีคุณสมบัติอิเล็กโตรเนกาทิวิตีสูง และอาร์กอน หนึ่งในแก๊สมีสกุล แต่การทดลองกลับล้มเหลว การเตรียมสารประกอบอาร์กอนยังเป็นไปไม่ได้จนจบคริสต์ศตวรรษที่ 20 แต่การท้าทายความเป็นไปได้ดังกล่าวทำให้เกิดทฤษฎีของโครงสร้างอะตอมใหม่ ๆ ตามมา ด้วยความรู้จากการทดลองที่ผ่านมา เมื่อ ค.ศ. 1913 นักฟิสิกส์ชาวเดนิช นิลส์ โปร์เสนอทฤษฎีโครงสร้างอะตอมว่า อิเล็กตรอนในอะตอมต่างเรียงอยู่ภายในชั้นพลังงานรอบนิวเคลียส และธาตุทั้งหมดในแก๊สมีสกุลยกเว้นฮีเลียม ล้วนมีอิเล็กตรอนในระดับพลังงานวงนอกครบ 8 อิเล็กตรอนเสมอ[11] ต่อมาใน ค.ศ. 1916 กิลเบิร์ต เอ็น ลิวอิสได้คิดค้นกฎออกเตตซึ่งสามารถสรุปได้ว่าการจับตัวครบแปดของอิเล็กตรอนในระดับพลังงานวงนอกเป็นการจัดเรียงตัวที่เสถียรที่สุดสำหรับอะตอมใดๆ โดยธาตุที่มีการจัดรูปแบบนี้จะไม่ตอบสนองต่อธาตุอื่น ๆ เนื่องจากไม่ต้องการอิเล็กตรอนมารวมในระดับพลังงานวงนอกอีกแล้ว[14]
ใน ค.ศ. 1962 นักเคมี นีล บาร์ตเลตต์ค้นพบซีนอนเฮกซะฟลูออโรแพลทิเนต[15] สารประกอบของแก๊สมีสกุลที่ค้นพบเป็นครั้งแรก สารประกอบของแก๊สมีสกุลชนิดอื่นค้นพบในเวลาต่อมา เช่น สารประกอบของธาตุเรดอนอย่างเรดอนไดฟลูออไรด์ (RnF
2) [16] ค้นพบใน ค.ศ. 1962 จากรอยสารกัมมันตภาพรังสี สารประกอบของธาตุคริปทอนอย่างคริปทอนไดฟลูออไรด์ (KrF
2)[17]ค้นพบใน ค.ศ. 1963 ส่วนสารประกอบอาร์กอนตัวแรกที่เสถียรบันทึกไว้ใน ค.ศ. 2000 เมื่ออาร์กอนฟลูออโรไฮไดรด์ (HArF) เกิดการจับตัวที่อุณหภูมิ 40 เคลวิน (−233.2 องศาเซลเซียส; −387.7 องศาฟาเรนไฮต์)[18]
ในเดือนตุลาคม ค.ศ. 2006 นักวิทยาศาสตร์จากสถาบันร่วมเพื่อการวิจัยนิวเคลียร์และห้องปฏิบัติการแห่งชาติ ลอว์เรนซ์ ลิเวอร์มอร์สามารถสังเคราะห์โอกาเนสซอนซึ่งเป็นธาตุที่ 17 ในกลุ่มที่ 18 ของตารางธาตุ[19]ได้สำเร็จ โดยการรวมตัวของแคลิฟอร์เนียมกับแคลเซียม[20]
สมบัติทางกายภาพและอะตอม
| สมบัติ[11][21] | ฮีเลียม | นีออน | อาร์กอน | คริปทอน | ซีนอน | เรดอน | โอกาเนสซอน |
|---|---|---|---|---|---|---|---|
| ความหนาแน่น (g/dm3) | 0.1786 | 0.9002 | 1.7818 | 3.708 | 5.851 | 9.97 | 7200 (ค่าทำนาย)[22] |
| จุดเดือด (K) | 4.4 | 27.3 | 87.4 | 121.5 | 166.6 | 211.5 | 450±10 (ค่าทำนาย)[22] |
| จุดหลอมเหลว (K) | –[23] | 24.7 | 83.6 | 115.8 | 161.7 | 202.2 | 325±15 (ค่าทำนาย)[22] |
| ความร้อนแฝงของการกลายเป็นไอ (kJ/mol) | 0.08 | 1.74 | 6.52 | 9.05 | 12.65 | 18.1 | – |
| การละลาย ในน้ำที่อุณหภูมิ 20 °C (cm3/kg) | 8.61 | 10.5 | 33.6 | 59.4 | 108.1 | 230 | – |
| เลขอะตอม | 2 | 10 | 18 | 36 | 54 | 86 | 118 |
| รัศมีอะตอม (จากการคำนวณ) (pm) | 31 | 38 | 71 | 88 | 108 | 120 | – |
| พลังงานไอออไนเซชัน (kJ/mol) | 2372 | 2080 | 1520 | 1351 | 1170 | 1037 | 839 (ค่าทำนาย)[24] |
| อิเล็กโตรเนกาทิวิตี[25] | 4.16 | 4.79 | 3.24 | 2.97 | 2.58 | 2.60 | 2.59[26] |
สำหรับข้อมูลเพิ่มเติม ดูต่อที่ แก๊สมีสกุล (หน้าข้อมูล)
แก๊สมีสกุลมีแรงระหว่างอะตอมที่อ่อน ส่งผลให้จุดเดือดและจุดหลอมเหลวต่ำมาก แก๊สมีสกุลเป็นแก๊สอะตอมเดี่ยวภายใต้ภาวะมาตรฐาน รวมถึงเป็นธาตุที่มีมวลอะตอมสูงกว่าธาตุที่เป็นของแข็งทั่วไป[11] ฮีเลียมมีปริมาณที่เป็นเอกลักษณ์กว่าธาตุอื่น โดยมีจุดเดือดที่ 1 บรรยากาศมาตรฐานต่ำกว่าสสารอื่น ฮีเลียมเป็นธาตุเดียวที่แสดงสมบัติของของไหลยวดยิ่งและเป็นธาตุเดียวที่ไม่สามารถทำให้เป็นของแข็งด้วยการลดอุณหภูมิที่ความดันบรรยากาศ[27] (ปรากฏการณ์นี้สามารถอธิบายด้วยกลศาสตร์ควอนตัมว่าพลังงานจุดศูนย์มากเกินไปที่จะเกิดการเยือกแข็ง)[28] – ต้องให้ความดัน 25 บรรยากาศมาตรฐาน (2,500 กิโลปาสกาล; 370 ปอนด์ต่อตารางนิ้ว) ที่อุณหภูมิ 0.95 เคลวิน (−272.200 องศาเซลเซียส; −457.960 องศาฟาเรนไฮต์) เพื่อเปลี่ยนให้ฮีเลียมเป็นของแข็ง[27] ในขณะที่ต้องใช้ความดันประมาณ 115 kbar สำหรับอุณหภูมิห้อง[29] แก๊สมีสกุลจนถึงซีนอนมีไอโซโทปที่เสถียรหลายไอโซโทป เรดอนไม่มีไอโซโทปเสถียร โดยไอโซโทปที่คงตัวได้นานที่สุดคือ Rn-222 ด้วยครึ่งชีวิต 3.8 วันและสลายเป็นฮีเลียมกับพอโลเนียม ซึ่งจะสลายต่อเป็นตะกั่ว จุดหลอมเหลวและจุดเดือดจะเพิ่มขึ้นไล่จากบนลงล่างของหมู่

อะตอมของแก๊สมีสกุลเช่นเดียวกันกับอะตอมในหมู่ส่วนใหญ่ มีรัศมีอะตอมเพิ่มขึ้นอย่างต่อเนื่องจากคาบหนึ่งไปอีกคาบหนึ่งเนื่องจากการเพิ่มจำนวนของอิเล็กตรอน ขนาดของอะตอมสัมพันธ์กับสมบัติหลายประการ ตัวอย่างเช่นพลังงานไอออไนเซชันลดลงกลับกันกับรัศมีที่เพิ่มขึ้น เนื่องจากเวเลนซ์อิเล็กตรอนในแก๊สมีสกุลที่ใหญ่กว่าจะห่างจากนิวเคลียสทำให้อิเล็กตรอนไม่ได้กระจุกตัวอย่างแน่นในอะตอมเท่ากับแก๊สมีสกุลที่เล็กกว่า แก๊สมีสกุลมีพลังงานไอออไนเซชันมากที่สุดเมื่อเทียบกับธาตุในคาบเดียวกัน ซึ่งแสดงให้เห็นถึงความเสถียรของการจัดเรียงอิเล็กตรอนและสัมพันธ์กับความไม่ว่องไวต่อปฏิกิริยาเคมี[21] แต่อย่างไรก็ตาม แก๊สมีสกุลที่หนักบางธาตุมีพลังงานไอออไนเซชันน้อยพอที่จะเปรียบเทียบกับธาตุและโมเลกุลอื่น ข้อมูลเชิงลึกระบุว่าซีนอนมีพลังงานไอออไนเซชันเท่ากับโมเลกุลออกซิเจน ทำให้บาร์ทเล็ตพยายามออกซิไดส์ซีนอนด้วยแพลทตินัมเฮกซะฟลูออไรด์(PtF6) ซึ่งเป็นตัวออกซิไดซ์ที่แรงมากพอให้เกิดปฏิกิริยากับออกซิเจน[15] แก๊สมีสกุลไม่สามารถรับอิเล็กตรอนจากไอออนลบ เนื่องจากมีสัมพรรคภาพอิเล็กตรอนน้อยกว่าศูนย์[30]
สมบัติทางกายภาพของแก๊สมีสกุลกำหนดโดยแรงแวนเดอร์วาลส์ระหว่างอะตอมที่อ่อน แรงดึงดูดเพิ่มขึ้นตามขนาดของอะตอมเนื่องจากการเพิ่มขึ้นของสภาพมีขั้วได้ และการลดลงของพลังงานไอออนไนเซชัน นั่นส่งผลให้เกิดแนวโน้มของค่าต่าง ๆ ไล่จากบนลงล่างตามธาตุหมู่ 18 โดยรัศมีอะตอมและแรงระหว่างอะตอมจะเพิ่มขึ้น ทำให้จุดเดือด จุดหลอมเหลว ความร้อนแฝงของการกลายเป็นไอและความสามารถในการละลาย ส่วนการเพิ่มขึ้นของความหนาแน่นเกิดจากการเพิ่มของมวลอะตอม[21]
แก๊สมีสกุลมีสมบัติใกล้เคียงแก๊สอุดมคติภายใต้ภาวะมาตรฐาน แต่เมื่อพิจารณาค่าเบี่ยงเบนจากกฎของแก๊สอุดมคติจะนำไปสู่การศึกษาเกี่ยวกับแรงระหว่างโมเลกุล ศักย์เลนนาร์ด-โจนส์มักใช้ในการจำลองปฏิสัมพันธ์ระหว่างโมเลกุล เป็นโมเดลที่เสนอในปี ค.ศ. 1924 โดย โจห์น เลนนาร์ด-โจนส์ จากข้อมูลที่ทดลองกับอาร์บอนก่อนที่กลศาสตร์ควอนตัมจะให้เครื่องมือสำหรับการทำความเข้าใจเรื่องแรงระหว่าโมเลกุลด้วยหลักการแรกเริ่ม[31] การวิเคราะห์เชิงทฤษฎีของปฏิสัมพันธ์เหล่านี้สามารถทำได้ง่ายเพราะแก๊สมีสกุลเป็นแก๊สอะตอมเดี่ยวและเป็นทรงกลม หมายความว่าปฏิสัมพันธ์ระหว่างอะตอมไม่ขึ้นกับทิศทางหรือมีสมบัติเป็นไอโซทรอปิก
สมบัติทางเคมี
แก๊สมีสกุลไม่มีสี ไม่มีกลิ่น ไม่มีรส และไม่ติดไฟภายใต้สภาวะมาตรฐาน[32]ครั้งหนึ่งพวกมันถูกระบุว่าเป็นหมู่ 0 ในตารางธาตุเพราะเชื่อว่าพวกมันมีวาเลนซ์เป็นศูนย์ ซึ่งหมายความว่าอะตอมของพวกมันไม่สามารถรวมตัวกับธาตุอื่นเพื่อสร้างสารประกอบได้ อย่างไรก็ตาม มีการค้นพบในภายหลังว่าบางชนิดก่อตัวเป็นสารประกอบ ทำให้ฉลากนี้เลิกใช้ไป[11]
การจัดเรียงอิเล็กตรอน
ข้อมูลเพิ่มเติม: การจัดเรียงอิเล็กตรอนของธาตุ (หน้าข้อมูล)
เช่นเดียวกับกลุ่มอื่นๆ ธาตุในหมู่นี้ในนี้แสดงรูปแบบในโครงแบบอิเล็กตรอน โดยเฉพาะชั้นนอกสุดที่ส่งผลให้เกิดพฤติกรรมทางเคมี:
| เลขอะตอม | ธาตุ | จำนวนอิเล็กตรอน/ชั้น |
|---|---|---|
| 2 | ฮีเลียม | 2 |
| 10 | นีออน | 2, 8 |
| 18 | อาร์กอน | 2, 8, 8 |
| 36 | คริปทอน | 2, 8, 18, 8 |
| 54 | ซีนอน | 2, 8, 18, 18, 8 |
| 86 | เรดอน | 2, 8, 18, 32, 18, 8 |
| 118 | โอกาเนสซอน | 2, 8, 18, 32, 32, 18, 8 (คาดคะเน) |
แก๊สมีสกุลมีเวเลนซ์อิเล็กตรอนเต็ม เวเลนซ์อิเล็กตรอนเป็นอิเล็กตรอนวงนอกสุดของอะตอมและโดยปกติจะเป็นอิเล็กตรอนเพียงตัวเดียวที่ร่วมสร้างพันธะเคมี อะตอมที่มีเวเลนซ์อิเล็กตรอนเต็มวงจะเสถียรมาก ดังนั้นจึงไม่มีแนวโน้มที่จะสร้างพันธะเคมี และมีแนวโน้มน้อยที่จะได้รับหรือสูญเสียอิเล็กตรอน[33] อย่างไรก็ตาม แก๊สมีสกุลที่หนักกว่า เช่น เรดอน จะจับกันด้วยแรงแม่เหล็กไฟฟ้าน้อยกว่าแก๊สมีสกุลที่เบากว่า เช่น ฮีเลียม ทำให้ง่ายต่อการกำจัดอิเล็กตรอนภายนอกออกจากแก๊สมีสกุลหนัก
ใช้ร่วมกับสัญกรณ์โครงแบบอิเล็กตรอนเพื่อสร้างสัญกรณ์แก๊สมีสกุล ในการทำเช่นนี้ แก๊สมีสกุลที่ใกล้ที่สุดซึ่งอยู่ก่อนหน้าองค์ประกอบที่เป็นปัญหาจะเขียนขึ้นก่อน จากนั้นจึงจัดโครงแบบอิเล็กตรอนต่อจากจุดนั้นไปข้างหน้า ตัวอย่างเช่น สัญกรณ์อิเล็กตรอนของฟอสฟอรัสคือ 1s2 2s2 2p6 3s2 3p3 ในขณะที่สัญลักษณ์ของแก๊สมีสกุลคือ [Ne] 3s2 3p3 สัญกรณ์ที่กะทัดรัดกว่านี้ทำให้ระบุธาตุได้ง่ายขึ้น และสั้นกว่าการเขียนสัญกรณ์ทั้งหมดของออร์บิทัลเชิงอะตอม[34]
แก๊สมีสกุลจะข้ามขอบเขตระหว่างบล็อก—ฮีเลียมเป็นธาตุบล็อก s ในขณะที่สมาชิกที่เหลือคือธาตุบล็อก p—ซึ่งผิดปกติในกลุ่ม IUPAC กลุ่ม IUPAC อื่น ๆ ทั้งหมดมีองค์ประกอบจากแต่ละบล็อก สิ่งนี้ทำให้เกิดความไม่สอดคล้องกันในแนวโน้มทั่วทั้งตาราง และด้วยเหตุนี้นักเคมีบางคนจึงเสนอว่าควรย้ายฮีเลียมไปยังหมู่ 2 เพื่อให้เข้ากับธาตุ s2 อื่น ๆ[35][36][37] แต่โดยทั่วไปแล้วไม่ได้นำการเปลี่ยนแปลงนี้มาใช้
สารประกอบ
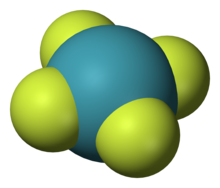
4 ซึ่งเป็นหนึ่งในสารประกอบของแก๊สมีสกุลกลุ่มแรกที่ถูกค้นพบ
แก๊สมีสกุลมีความไวต่อปฏิกิริยาเคมีที่ต่ำมาก; ดังนั้นจึงมีการสร้างสารประกอบของแก๊สมีสกุล เพียงไม่กี่ร้อยรายการเท่านั้น สารประกอบ ที่เป็นกลางซึ่งฮีเลียมและนีออนมีส่วนร่วมใน พันธะเคมี ยังไม่ก่อตัวขึ้น (แม้ว่าจะมีไอออนที่มีฮีเลียมอยู่บ้าง และมีหลักฐานทางทฤษฎีบางอย่างสำหรับไอออนที่เป็นกลางซึ่งมีฮีเลียมอยู่บ้าง) ในขณะที่ซีนอน คริปทอน และอาร์กอนแสดงปฏิกิริยาเพียงเล็กน้อยเท่านั้น[38] ความไวต่อปฏิกิริยาเป็นไปตามลำดับ Ne < He < Ar < Kr < Xe < Rn ≪ Og
ในปี ค.ศ. 1933 ไลนัส พอลิง ทำนายว่าแก๊สมีสกุลที่หนักกว่าสามารถสร้างสารประกอบที่มีฟลูออรีนและออกซิเจน เขาทำนายการมีอยู่ของ krypton hexafluoride (KrF
6) และ xenon hexafluoride (XeF
6) โดยสันนิษฐานว่า XeF
8 อาจมีอยู่เป็นสารประกอบที่ไม่เสถียร และเสนอว่า xenic acid สามารถสร้างเกลือ perxenate ได้[39][40] การคาดคะเนเหล่านี้แสดงให้เห็นว่าโดยทั่วไปมีความแม่นยำ ยกเว้นว่า XeF
8 ในขณะนี้ถือว่าไม่เสถียรทั้งทางอุณหพลศาสตร์และทางจลนพลศาสตร์เคมี[41]
สารประกอบซีนอนเป็นสารประกอบของแก๊สมีสกุลจำนวนมากที่สุดที่ก่อตัวขึ้น[42] ส่วนใหญ่มีอะตอมของซีนอนใน สถานะออกซิเดชัน ที่ +2, +4, +6 หรือ +8 ที่สร้างพันธะกับอะตอมที่มี ไฟฟ้าลบ สูง เช่น ฟลูออรีนหรือออกซิเจน เช่นใน ซีนอนไดฟลูออไรด์ (XeF
2), ซีนอนเตตระฟลูออไรด์ (XeF
4), ซีนอนเฮกซาฟลูออไรด์ (XeF
6), ซีนอนเตตรอกไซด์ (XeO
4) และโซเดียมเปอร์ซีเนต (Na
4XeO
6) ซีนอนทำปฏิกิริยากับฟลูออรีนเพื่อสร้างซีนอนฟลูออไรด์จำนวนมากตามสมการต่อไปนี้:
- Xe + F2 → XeF6
- Xe + 2F2 → XeF4
- Xe + 3F2 → XeF6
บางส่วนของ สารประกอบเหล่านี้พบว่าใช้ใน การสังเคราะห์ทางเคมี เป็นตัวออกซิไดซ์; โดยเฉพาะอย่างยิ่ง XeF
2 มีจำหน่ายในเชิงพาณิชย์และสามารถใช้เป็นตัวแทน fluorinating[43] ในปี ค.ศ. 2007 มีการระบุสารประกอบของซีนอนประมาณห้าร้อยตัวที่จับกับธาตุอื่นๆ รวมทั้งสารประกอบออร์แกนซีนอน (ที่มีซีนอนจับกับคาร์บอน) และซีนอนจับกับไนโตรเจน คลอรีน ทอง ปรอท และซีนอนเอง[38][44] สารประกอบของซีนอนที่จับกับโบรอน ไฮโดรเจน โบรมีน ไอโอดีน เบริลเลียม กำมะถัน ไททาเนียม ทองแดง และเงิน ยังพบได้เฉพาะที่อุณหภูมิต่ำในแก๊สมีสกุล matrices หรือในแก๊สมีสกุลที่มีความเร็วเหนือเสียง[38]
เรดอนมีปฏิกิริยามากกว่าซีนอน และสร้างพันธะเคมีได้ง่ายกว่าซีนอน อย่างไรก็ตาม เนื่องจากกัมมันตภาพรังสีสูงและครึ่งชีวิตสั้นของ เรดอนไอโซโทป จึงเกิดเรดอนเพียงไม่กี่ ฟลูออไรด์ และ ออกไซด์ เท่านั้น[45] เรดอนก้าวไปสู่พฤติกรรมของโลหะมากกว่าซีนอน ไดฟลูออไรด์ RnF2 เป็นไอออนิกสูง และ Rn2+ ประจุบวกจะเกิดขึ้นในสารละลายฮาโลเจนฟลูออไรด์ ด้วยเหตุผลนี้ อุปสรรคทางจลนพลศาสตร์ทำให้ยากที่จะออกซิไดซ์เรดอนเกินสถานะ +2 มีเพียงการทดลองตามรอยเท่านั้นที่ประสบความสำเร็จในการทำเช่นนั้น อาจสร้าง RnF4 , RnF6 และ RnO3[46][47][48]
คริปทอนมีปฏิกิริยาน้อยกว่าซีนอน แต่มีรายงานสารประกอบหลายตัวที่มีคริปทอนใน สถานะออกซิเดชัน ที่ +2[38] คริปทอนไดฟลูออไรด์ มีความโดดเด่นที่สุดและจำแนกได้ง่ายที่สุด ภายใต้สภาวะที่รุนแรง คริปทอนจะทำปฏิกิริยากับฟลูออรีนเพื่อสร้าง KrF2 ตามสมการต่อไปนี้:
- Kr + F2 → KrF2
สารประกอบที่คริปทอนสร้างพันธะเดี่ยวกับไนโตรเจนและออกซิเจนก็มีลักษณะเช่นกัน[49] แต่จะคงที่ต่ำกว่า −60 องศาเซลเซียส (−76 องศาฟาเรนไฮต์) และ −90 องศาเซลเซียส (−130 องศาฟาเรนไฮต์) ตามลำดับ[38]
อะตอมของคริปทอนจับกันทางเคมีกับอโลหะอื่นๆ (ไฮโดรเจน คลอรีน คาร์บอน) รวมถึง โลหะทรานซิชัน บางส่วน (ทองแดง เงิน ทอง) ที่ยังสังเกตพบ แต่ที่อุณหภูมิต่ำในเมทริกซ์แก๊สมีสกุลเท่านั้น หรือในเครื่องบินไอพ่นที่มีความเร็วเหนือเสียง[38] มีการใช้เงื่อนไขที่คล้ายกันเพื่อให้ได้สารประกอบสองสามชนิดแรกของอาร์กอนในปี ค.ศ. 2000 เช่น อาร์กอนฟลูออโรไฮไดรด์ (HArF) และบางส่วนจับกับโลหะทรานซิชันช่วงปลายอย่างทองแดง เงิน และทอง[38] ในปี ค.ศ. 2007 ยังไม่มีข้อมูลโมเลกุลที่เป็นกลางที่เสถียรซึ่งเกี่ยวข้องกับฮีเลียมหรือนีออนที่มีพันธะโควาเลนต์[38]
การคาดคะเนจากแนวโน้มจากการทำนายว่าออกาเนสสันควรเป็นแก๊สมีสกุลที่มีปฏิกิริยามากที่สุด การบำบัดทางทฤษฎีที่ซับซ้อนมากขึ้นบ่งชี้ว่ามีปฏิกิริยามากกว่าที่คาดการณ์ไว้ ถึงจุดที่มีการตั้งคำถามเกี่ยวกับการใช้คำอธิบายของ 'แก๊สมีสกุล'[50] โอกาเนสซอนคาดว่าจะค่อนข้างเหมือน ซิลิคอน หรือ ดีบุก ในหมู่ 14:[51] องค์ประกอบปฏิกิริยาที่มีสถานะ +4 ทั่วไปและสถานะ +2 ทั่วไปน้อยกว่า[52][53] ซึ่งที่อุณหภูมิและความดันห้องไม่ได้เป็นแก๊สแต่เป็นสารกึ่งตัวนำที่เป็นของแข็ง จำเป็นต้องมีการทดสอบเชิงประจักษ์ / เชิงทดลองเพื่อตรวจสอบการคาดการณ์เหล่านี้[22][54] (ในทางกลับกัน ฟลีโรเวียม แม้จะอยู่ในหมู่ 14 แต่คาดการณ์ว่าจะระเหยผิดปกติ ซึ่งบ่งชี้ถึงคุณสมบัติคล้ายแก๊สมีสกุล)[55][56]
แก๊สมีสกุลรวมถึงฮีเลียมสามารถสร้าง โมเลกุลไอออน ที่เสถียรในเฟสของแก๊ส วิธีที่ง่ายที่สุดคือ ฮีเลียมไฮไดรด์โมเลกุลไอออน, HeH+ ค้นพบในปี ค.ศ. 1925[57] เนื่องจากประกอบด้วยธาตุที่มีมากที่สุด 2 ชนิดในเอกภพ ได้แก่ ไฮโดรเจนและฮีเลียม จึงเชื่อว่าเกิดขึ้นตามธรรมชาติในตัวกลางระหว่างดวงดาว และในที่สุดก็ตรวจพบในเดือนเมษายน ค.ศ. 2019 โดยใช้อากาศกล้องโทรทรรศน์โซเฟีย. นอกจากไอออนเหล่านี้แล้ว ยังมีแก๊สมีสกุลที่เป็นกลาง excimer อีกหลายชนิด เหล่านี้เป็นสารประกอบเช่น ArF และ KrF ที่เสถียรเฉพาะเมื่ออยู่ในสถานะกระตุ้น; บางส่วนพบการใช้งานใน excimer laser
นอกจากสารประกอบที่อะตอมของแก๊สมีสกุลมีส่วนร่วมใน พันธะโควาเลนต์ แล้ว แก๊สมีสกุลยังก่อตัวเป็นสารประกอบ ที่ไม่ใช่โควาเลนต์ clathrates อธิบายครั้งแรกในปี ค.ศ. 1949[58] ประกอบด้วยอะตอมของแก๊สมีสกุลที่ติดอยู่ภายในโพรงของ ผลึกขัดแตะ ของสารอินทรีย์และอนินทรีย์บางชนิด เงื่อนไขที่จำเป็นสำหรับการก่อตัวของพวกมันคืออะตอมแก๊สมีสกุล จะต้องมีขนาดที่เหมาะสมเพื่อให้พอดีกับโพรงของโครงตาข่ายคริสตัลโฮสต์ ตัวอย่างเช่น อาร์กอน คริปทอน และซีนอนสร้างคลาเทรตด้วย ไฮโดรควิโนน แต่ฮีเลียมและนีออนไม่มีเพราะพวกมันมีขนาดเล็กเกินไปหรือไม่เพียงพอ[59] นีออน อาร์กอน คริปทอน และซีนอนยังก่อตัวเป็นคลาเทรตไฮเดรต ซึ่งแก๊สมีสกุลขังอยู่ในน้ำแข็ง[60]
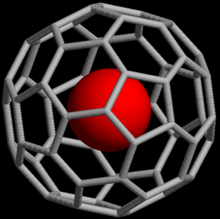
แก๊สมีสกุลสามารถก่อตัวเป็น เอนโดฮีดรัล ฟูลเลอรีน ซึ่งอะตอมของแก๊สมีสกุลขังอยู่ภายในโมเลกุล ฟูลเลอรีน ในปี ค.ศ. 1993 มีการค้นพบว่าเมื่อ C
60 ซึ่งเป็นโมเลกุลทรงกลมที่ประกอบด้วย 60 คาร์บอน อะตอม สัมผัสกับแก๊สมีสกุลที่ความดันสูง ซับซ้อน เช่น He@C
60 สามารถสร้างขึ้นได้ (สัญลักษณ์ @ ระบุว่ามีเขาอยู่ภายใน C
60 แต่ไม่ผูกพันโควาเลนต์กับมัน)[61] ในปี ค.ศ. 2008 เอ็นโดฮีดรัลคอมเพล็กซ์ที่มีฮีเลียม นีออน อาร์กอน คริปทอน และซีนอนได้สร้างขึ้นแล้ว[62] พบสารประกอบเหล่านี้ใช้ในการศึกษาโครงสร้างและความว่องไวต่อปฏิกิริยาของฟูลเลอรีนโดยวิธี นิวเคลียร์ แมกเนติก เรโซแนนซ์ ของอะตอมของแก๊สมีสกุล[63]

2 อธิบายด้วยโมเดลพันธะ 3 อะตอมกลาง 4 อิเล็กตรอน
สารประกอบของแก๊สมีสกุลเช่น ซีนอนไดฟลูออไรด์ (XeF
2) ถูกพิจารณาว่าเป็น ไฮเปอร์วาเลนต์ เนื่องจากพวกมันละเมิด กฎออกเตต พันธะในสารประกอบดังกล่าวสามารถอธิบายได้โดยใช้แบบจำลอง พันธะสามศูนย์สี่อิเล็กตรอน[64][65] แบบจำลองนี้เสนอครั้งแรกในปี ค.ศ. 1951 พิจารณาถึงพันธะของอะตอมคอลลิเนียร์สามตัว ตัวอย่างเช่น พันธะใน XeF
2 อธิบายโดยชุดของทฤษฎีออร์บิทัลเชิงโมเลกุล (MO) สามชุดที่ได้มาจาก p-orbital บนแต่ละอะตอม พันธะผลลัพธ์จากการรวมกันของ p-orbital ที่เติมจาก Xe กับ p-orbital ที่เติมครึ่งหนึ่งจากแต่ละอะตอม F ทำให้เกิดออร์บิทัลที่มีพันธะที่เติมเต็ม, ออร์บิทัลที่ไม่มีพันธะที่เติม และว่างเปล่า ออร์บิทัลโมเลกุลแบบต้านพันธะ การโคจรของโมเลกุลที่ถูกครอบครองสูงสุด อยู่ในช่วงปลายของอะตอมทั้งสอง สิ่งนี้แสดงถึงตำแหน่งของประจุที่อำนวยความสะดวกโดยค่าอิเล็กโทรเนกาติวิตีสูงของฟลูออรีน[66]
คุณสมบัติทางเคมีของแก๊สมีสกุลที่หนักกว่า คริปทอนและซีนอน ได้รับการยอมรับอย่างดี เคมีของสารที่เบากว่า อาร์กอนและฮีเลียมยังอยู่ในช่วงเริ่มต้น ในขณะที่ยังไม่สามารถระบุสารประกอบของนีออนได้
ปริมาณในธรรมชาติและการผลิต
ปริมาณของแก๊สมีสกุลในเอกภพมีค่าลดลง เมื่อแก๊สมีเลขอะตอมเพิ่มขึ้น ฮีเลียมเป็นธาตุที่พบได้มากที่สุดในเอกภพถัดมาจากไฮโดรเจนโดยมีเศษส่วนมวลประมาณ 24% ฮีเลียมส่วนใหญ่ในเอกภพเกิดขึ้นระหว่างการสังเคราะห์นิวเคลียสของบิกแบง ในภายหลัง ปริมาณฮีเลียมยังคงเพิ่มขึ้นอย่างต่อเนื่องจากการหลอมรวมของไฮโดรเจนในการสังเคราะห์นิวเคลียสของดาวฤกษ์(และเพิ่มขึ้นน้อยมากจากการสลายให้อนุภาคแอลฟาของธาตุหนัก)[67][68] ปริมาณของแก๊สบนโลกเป็นไปตามแนวโน้มที่แตกต่างกัน เช่น ฮีเลียมเป็นแก๊สมีสกุลที่มีมากที่สุดเป็นอันดับที่สามในชั้นบรรยากาศ เหตุผลก็คือไม่มีฮีเลียมดั้งเดิมในชั้นบรรยากาศ เนื่องจากมีมวลอะตอมน้อย ทำให้ฮีเลียมไม่สามารถลอยต้านสนามแรงโน้มถ่วงของโลก[69]ได้ ฮีเลียมบนโลกมาจากการสลายตัวของธาตุหนักอย่างยูเรเนียมและทอเรียมที่พบบนเปลือกโลก และมีแนวโน้มที่จะสะสมในแหล่งแก๊สธรรมชาติ[69] ในทางตรงกันข้าม ปริมาณของอาร์กอนเพิ่มขึ้นจากการสลายให้อนุภาคบีตาของธาตุโพแทสเซียม-40 เพื่อสร้างอาร์กอน-40 โพแทสเซียมสามารถพบได้บนเปลือกโลก และเป็นไอโซโทปของอาร์กอนที่มีปริมาณมากที่สุดบนโลก แม้จะค่อนข้างหายากในระบบสุริยะก็ตาม กระบวนการสลายอนุภาคนี้เป็นส่วนของวิธีการจับคู่โพแทสเซียมอาร์กอน[70] ซีนอนเป็นธาตุที่มีความอุดมสมบูรณ์ต่ำมากในชั้นบรรยากาศ จนมีข้อสงสัยว่าซีนอนหายไปได้อย่างไร ทฤษฎีหนึ่งกล่าวว่าซีนอนที่หายไปน่าจะอยู่ในรวมตัวกับแร่ธาตุในแผ่นเปลือกโลก[71] หลังจากการค้นพบซีนอนไดออกไซด์ การวิจัยแสดงให้เห็นว่าซีนอนสามารถใช้แทนซิลิกอนในควอตซ์ได้[72] เรดอนเกิดขึ้นในธรณีภาคเนื่องจากการสลายให้อนุภาคแอลฟาของเรเดียม โดยเรดอนสามารถซึมผ่านรอยแตกเข้าไปในอาคารและสะสมในพื้นที่ที่มีการระบายอากาศไม่ดี เนื่องจากเป็นธาตุที่มีความเป็นกัมมันตภาพรังสีสูง เรดอนจึงเป็นอันตรายต่อสุขภาพอย่างมาก ทางสถิติเรดอนเป็นตัวแปรหนึ่งที่ทำให้อัตราการเสียชีวิตด้วยโรคมะเร็งปอดมีค่าประมาณ 21,000 คนต่อปีในสหรัฐอเมริกา[73] ออกาเนสสันเป็นธาตุที่ไม่สามารถเกิดขึ้นในธรรมชาติ และสร้างได้จากการสังเคราะห์โดยนักวิทยาศาสตร์เท่านั้น
| ปริมาณที่มีอยู่ | ฮีเลียม | นีออน | อาร์กอน | คริปตอน | ซีนอน | เรดอน |
|---|---|---|---|---|---|---|
| ระบบสุริยะ (ต่อหนึ่งอะตอมซิลิกอน)[74] | 2343 | 2.148 | 0.1025 | 5.515 × 10−5 | 5.391 × 10−6 | – |
| ชั้นบรรยากาศโลก (อัตราส่วนปริมาตร ppm)[75] | 5.20 | 18.20 | 9340.00 | 1.10 | 0.09 | (0.06–18) × 10−19[76] |
| หินอัคนี (อัตราส่วนมวลในล้านส่วน)[21] | 3 × 10−3 | 7 × 10−5 | 4 × 10−2 | – | – | 1.7 × 10−10 |
สำหรับการใช้งานในปริมาณมาก สกัดฮีเลียมด้วยวิธีการกลั่นแบบลำดับส่วนจากแก๊สธรรมชาติ ซึ่งมีฮีเลียมเป็นส่วนประกอบมากถึง 7%[77]
นีออน อาร์กอน คริปทอน และ ซีนอน สามารถผลิตได้จากอากาศด้วยวิธีลิเคอแฟคชัน เพื่อเปลี่ยนแก๊สเป็นของเหลว และวิธีการกลั่นแบบลำดับส่วน เพื่อแยกสารประกอบต่าง ๆ ออกจากกัน ส่วนการผผลิตทำโดยการสกัดแก๊สธรรมชาติ และสกัดเรดอนจากการสลายกัมมันตภาพรังสีของสารประกอบเรเดียม[11] ราคาของแก๊สมีสกุลขึ้นอยู่กับปริมาณที่พบทางธรรมชาติ โดยอาร์กอนมีราคาที่ต่ำที่สุด ในขณะที่ซีนอนมีราคาสูงที่สุด ตารางด้านล่างแสดงราคาของแก๊สแต่ละชนิดในปี ค.ศ. 2004 ภายในห้องปฏิบัติการ สหรัฐอเมริกา
| แก๊ส | ราคาเมื่อ ค.ศ. 2004 (ดอลลาร์ต่อลูกบาศก์เมตร)[78] |
|---|---|
| ฮีเลียม (เกรดอุตสาหกรรม) | 4.20–4.90 |
| ฮีเลียม (เกรดห้องทดลอง) | 22.30–44.90 |
| อาร์กอน | 2.70–8.50 |
| นีออน | 60–120 |
| คริปตอน | 400–500 |
| ซีนอน | 4000–5000 |
การใช้ประโยชน์

แก๊สมีสกุลมีจุดเดือดและจุดหลอมเหลวที่ต่ำมาก ซึ่งทำให้แก๊สเหล่านี้ใช้เป็นสารทำความเย็นในเชิงอติสีตศาสตร์ โดยเฉพาะฮีเลียมเหลว[79] ซึ่งเดือดที่ 4.2 เคลวิน (−268.95 องศาเซลเซียส; −452.11 องศาฟาเรนไฮต์) นำไปใช้สร้างแม่เหล็กตัวนำยิ่งยวด สำหรับการสร้างภาพด้วยเรโซแนนซ์แม่เหล็ก (MRI) และนิวเคลียร์แมกเนติกเรโซแนนซ์สเปกโทรสโกปี (NMR)[80] นีออนเหลวถึงแม้จะไม่สามารถลดอุณหภูมิจนเท่าฮีเลียมเหลว นีออนเหลวยังนำไปใช้ในงานด้านอติสีตศาสตร์เนื่องจากมีวิสัยสามารถทำความเย็นมากกว่าฮีเลียมเหลว 40 เท่าและมากกว่าไฮโดรเจนเหลว 3 เท่า[76]
ฮีเลียมใช้เป็นองค์ประกอบของแก๊สสำหรับหายใจแทนที่ไนโตรเจน เนื่องจากมีความสามารถในการละลายในของไหลต่ำโดยเฉพาะไขมัน แก๊สทั่วไปมักถูกดูดซึมโดยเลือดและเนื้อเยื่อภายใต้ความดันเช่นการดำน้ำลึก ทำให้เกิดภาวะเซื่องซึมเรียกว่าภาวะเมาไนโตรเจน[81] แต่ด้วยที่ฮีเลียมมีความสามารถในการละลายต่ำ ฮีเลียมจึงซึมเข้าเยื่อหุ้มเซลล์ได้น้อย เมื่อใช้ฮีเลียมเป็นส่วนผสมของแก๊สสำหรับหายใจเช่นใน trimix หรือ heliox จึงช่วยลดอาการเซื่องซึมของนักประดาน้ำภายใต้ความลึก[82] ความสามารถในการละลายของฮีเลียมที่น้อยมีประโยชน์ในการรักษาโรคลดความกดหรือ the bends[11][83] เมื่อมีปริมาณแก๊สละลายในร่างกายลดลงหมายความว่าจะเกิดฟองแก๊สจำนวนน้อยลงที่ความดันที่ต่ำลง นอกจากนี้อาร์กอนยังเป็นตัวเลือกที่ดีที่สุดสำหรับการดำน้ำลึกแบบ drysuit[84] และฮีเลียมยังใช้เป็นแก๊สเติมแกนของเตาปฏิกรณ์นิวเคลียร์[85]

ตั้งแต่วินาศภัยฮินเดินบวร์คในปี ค.ศ. 1937[86] แก๊สลอยตัวในเรือเหาะและลูกโป่งใช้ฮีเลียมทดแทนไฮโดรเจน เนื่องจากความเบาและความไม่ติดไฟ แม้ว่าจะมีแรงลอยตัวลดลง 8.6%[87][11]
ในการประยุกต์ใช้ มีใช้แก๊สมีสกุลในบรรยากาศเฉื่อย อาร์กอนใช้ในการสังเคราะห์สารประกอบที่ไวต่ออากาศนั่นคือไวต่อไนโตรเจน อาร์กอนแข็งใช้ในการศึกษาสารประกอบที่ไม่เสถียรมากเช่นสารมัธยันตร์ที่ไวต่อปฏิกิริยา โดยการกักในเมทริกซ์เฉื่อยที่อุณหภูมิต่ำมาก[88] ฮีเลียมใช้เป็นตัวกลางนำพาในเทคนิคแก๊สโครมาโทกราฟี เป็นแก๊สเติมในเทอร์โมมิเตอร์และในอุปกรณ์ตรวจวัดการแผ่รังสีเช่นเครื่องนับไกเกอร์–มึลเลอร์และห้องฟอง[78] ฮีเลียมและอาร์กอนมักใช้เป็นกำบังสำหรับการเชื่อมอาร์กและการกระจายของโลหะไร้สกุลในบรรยากาศขณะเชื่อมหรือตัดโลหะ รวมถึงกระบวนการทางโลหการและการผลิตซิลิคอนในอุตสาหกรรมสารกึ่งตัวนำ[76]

แก๊สมีสกุลมักใช้ในการจัดแสงเพราะมีความไวต่อปฏิกิริยาเคมีต่ำ อาร์กอนจะผสมกับไนโตรเจนใช้เติมในหลอดไส้ร้อนแบบธรรมดา[76] คริปทอนใช้ในหลอดไฟประสิทธิภาพสูง ซึ่งให้อุณหภูมิสีและประสิทธิภาพสูงกว่า เนื่องจากสามารถลดอัตราการขาดของแกนหลอดไฟได้ดีกว่าอาร์กอน หลอดแฮโลเจนใช้คริปทอนประสมกับสารประกอบของไอโอดีนหรือโบรมีนปริมาณน้อย[76] แก๊สมีสกุลเรืองแสงให้สีที่โดดเด่นเมื่อใช้ในหลอดแก๊สคายประจุเช่น หลอดไฟนีออน แม้ว่าหลอดไฟจะเรียกชื่อตามแก๊สนีออนแต่ก็ประกอบด้วยแก๊สชนิดอื่นและสารเรืองแสง ซึ่งทำให้เกิดเฉดสีหลากหลายได้เป็นสีส้มอมแดงของนีออน ซีนอนมักใช้ในหลอดไฟซีนอนอาร์ค เนื่องจากสเปกตรัมที่เกือบต่อเนื่องคล้ายกับแสงอาทิตย์ จึงมักประยุกต์ในเครื่องฉายภาพยนตร์และไฟหน้ารถ[76]
แก๊สมีสกุลใช้ในเอ็กไซเมอร์เลเซอร์ ซึ่งสร้างจากโมเลกุลที่ถูกกระตุ้นด้วยไฟฟ้าและคงสภาพในระยะเวลาสั้นเรียกว่าเอ็กไซเมอร์ โมเลกุลเอ็กไซเมอร์ที่ใช้ในเลเซอร์อาจเป็นไดเมอร์ของแก๊สมีสกุลเช่น Ar2, Kr2 หรือ Xe2 หรือที่นิยมใช้คือแก๊สมีสกุลที่รวมตัวกับธาตุฮาโลเจนในรูปโมเลกุลเอ็กไซเมอร์เช่น ArF, KrF, XeF หรือ XeCl เลเซอร์เหล่านี้สร้างรังสีอัลตราไวโอเล็ต ซึ่งเนื่องจากความยาวคลื่นที่สั้น (193 นาโนเมตรสำหรับ ArF และ 248 นาโนเมตรสำหรับ KrF) ทำให้ใช้ในงานภาพถ่ายรังสีแม่นยำสูงได้ เอ็กไซเมอเลเซอร์ใช้ในด้านอุตสาหกรรม การแพทย์และวิทยาศาสตร์อย่างหลากหลาย นอกจากนี้ยังใช้ในงานด้านไมโครลิโธกราฟีและด้านการสร้างชิ้นส่วนจุลภาค ซึ่งมีความสำคัญในการผลิตวงจรรวม และการผ่าตัดด้วยเลเซอร์ได้แก่การขยายหลอดเลือดด้วยเลเซอร์และการผ่าตัดตา[89]
แก๊สมีสกุลบางชนิดมีการประยุกต์ใช้โดยตรงในทางการแพทย์ บางครั้งฮีเลียมจะใช้ช่วยเหลือผู้ป่วยหอบหืดให้หายใจดีขึ้น[76] ซีนอนใช้เป็นยาสลบเพราะความสามารถในการละลายในไขมันที่สูง ทำให้เกิดฤทธิ์มากกว่าไนตรัสออกไซด์ที่ใช้โดยทั่วไปและเนื่องจากมันถูกกำจัดจากร่างกายโดยทันที ทำให้ผู้ป่วยฟื้นตัวเร็วขึ้น[90] ซีนอนประยุกต์ในการถ่ายภาพรังสีทางการแพทย์ของปอดด้วยเทคนิค hyperpolarized MRI[91] เรดอนซึ่งไวต่อปฏิกิริยามากและมีปริมาณน้อยใช้ในการรังสีบำบัด[11]
แก๊สมีสกุลโดยเฉพาะซีนอนใช้มากในเครื่องยนต์ไอออนเนื่องจากความเฉื่อยของมัน เนื่องจากเครื่องยนต์ไอออนไม่ได้ขับเคลื่อนด้วยปฏิกิริยาเคมี เชื้อเพลิงที่เฉื่อยเชิงเคมีใช้ป้องกันการเกิดปฏิกิริยาที่ไม่พึงประสงค์ระหว่างเชื้อเพลิงรวมถึงสิ่งอื่นในเครื่องยนต์
โอกาเนสซอนถูกค้นพบในบริบทของงานวิจัยเพื่อค้นพบธาตุใหม่เท่านั้น ทำให้ยังผลิตในปริมาณน้อยและไม่เสถียร จึงยังไม่มีการประยุกต์ใช้โอกาเนสซอน
สีในหลอดไฟ

|

|

|

|

|

|

|

|

|

|

|

|

|

|

|
| ฮีเลียม | นีออน | อาร์กอน | คริปทอน | ซีนอน |
สีของแก๊สขึ้นอยู่กับหลากหลายปัจจัยได้แก่:[92]
- พารามิเตอร์การคายประจุ (ค่าความหนาแน่นกระแสไฟฟ้าและสนามไฟฟ้าในแต่ละบริเวณ อุณหภูมิ ฯลฯ – ความหลากหลายของสีจากการเปล่งแสดงในแถวบนสุด);
- ความบริสุทธิ์ของแก๊ส (ถึงแม้มีแก๊สปนเปื้อนปริมาณน้อยก็ยังส่งผลต่อสีได้);
- วัสดุของกระเปาะคายประจุ – บริเวณป้องกันรังสีอัลตราไวโอเลตและองค์ประกอบสีน้ำเงินในกระเปาะแถวล่างสุดสร้างจากแก้วครัวเรือนหนา
ดูเพิ่ม
เชิงอรรถ
- ↑ Bauzá, Antonio; Frontera, Antonio (2015). "Aerogen Bonding Interaction: A New Supramolecular Force?". Angewandte Chemie International Edition. 54 (25): 7340–3. doi:10.1002/anie.201502571. PMID 25950423.
- ↑ Koppenol, W. (2016). "How to name new chemical elements" (PDF). Pure and Applied Chemistry. DeGruyter. doi:10.1515/pac-2015-0802. hdl:10045/55935. S2CID 102245448.
- ↑ Renouf, Edward (1901). "Noble gases". Science. 13 (320): 268–270. Bibcode:1901Sci....13..268R. doi:10.1126/science.13.320.268. S2CID 34534533.
- ↑ Ozima 2002, p. 30
- ↑ Ozima 2002, p. 4
- ↑ "argon". Encyclopædia Britannica. 2008.
- ↑ Oxford English Dictionary (1989), s.v. "helium". Retrieved 16 December 2006, from Oxford English Dictionary Online. Also, from quotation there: Thomson, W. (1872). Rep. Brit. Assoc. xcix: "Frankland and Lockyer find the yellow prominences to give a very decided bright line not far from D, but hitherto not identified with any terrestrial flame. It seems to indicate a new substance, which they propose to call Helium."
- ↑ 8.0 8.1 Ozima 2002, p. 1
- ↑ Mendeleev 1903, p. 497
- ↑ Partington, J. R. (1957). "Discovery of Radon". Nature. 179 (4566): 912. Bibcode:1957Natur.179..912P. doi:10.1038/179912a0. S2CID 4251991.
- ↑ 11.0 11.1 11.2 11.3 11.4 11.5 11.6 11.7 11.8 "Noble Gas". Encyclopædia Britannica. 2008.
- ↑ Cederblom, J. E. (1904). "The Nobel Prize in Physics 1904 Presentation Speech".
- ↑ Cederblom, J. E. (1904). "The Nobel Prize in Chemistry 1904 Presentation Speech".
- ↑ Gillespie, R. J.; Robinson, E. A. (2007). "Gilbert N. Lewis and the chemical bond: the electron pair and the octet rule from 1916 to the present day". The Journal of Computational Chemistry. 28 (1): 87–97. doi:10.1002/jcc.20545. PMID 17109437.
- ↑ 15.0 15.1 Bartlett, N. (1962). "Xenon hexafluoroplatinate Xe+[PtF6]−". Proceedings of the Chemical Society (6): 218. doi:10.1039/PS9620000197.
- ↑ Fields, Paul R.; Stein, Lawrence; Zirin, Moshe H. (1962). "Radon Fluoride". Journal of the American Chemical Society. 84 (21): 4164–4165. doi:10.1021/ja00880a048.
- ↑ Grosse, A. V.; Kirschenbaum, A. D.; Streng, A. G.; Streng, L. V. (1963). "Krypton Tetrafluoride: Preparation and Some Properties". Science. 139 (3559): 1047–1048. Bibcode:1963Sci...139.1047G. doi:10.1126/science.139.3559.1047. PMID 17812982.
- ↑ Khriachtchev, Leonid; Pettersson, Mika; Runeberg, Nino; Lundell, Jan; Räsänen, Markku (2000). "A stable argon compound". Nature. 406 (6798): 874–876. Bibcode:2000Natur.406..874K. doi:10.1038/35022551. PMID 10972285. S2CID 4382128.
- ↑ Barber, Robert C.; Karol, Paul J.; Nakahara, Hiromichi; Vardaci, Emanuele & Vogt, Erich W. (2011). "Discovery of the elements with atomic numbers greater than or equal to 113 (IUPAC Technical Report)*" (PDF). Pure and Applied Chemistry. IUPAC. 83 (7). doi:10.1515/ci.2011.33.5.25b. สืบค้นเมื่อ 30 May 2014.
- ↑ Oganessian, Yu. Ts.; Utyonkov, V.; Lobanov, Yu.; Abdullin, F.; Polyakov, A.; และคณะ (2006). "Synthesis of the isotopes of elements 118 and 116". Physical Review C. 74 (4): 44602. Bibcode:2006PhRvC..74d4602O. doi:10.1103/PhysRevC.74.044602.
- ↑ 21.0 21.1 21.2 21.3 Greenwood 1997, p. 891
- ↑ 22.0 22.1 22.2 22.3 Smits, Odile; Mewes, Jan-Michael; Jerabek, Paul; Schwerdtfeger, Peter (2020). "Oganesson: A Noble Gas Element That Is Neither Noble Nor a Gas". Angewandte Chemie International Edition. 59 (52): 23636–23640. doi:10.1002/anie.202011976. PMC 7814676. PMID 32959952.
- ↑ Liquid helium will only solidify if exposed to pressures well above atmospheric pressure, an effect explainable with quantum mechanics
- ↑ Winter, Mark (2020). "Organesson: Properties of Free Atoms". WebElements: THE periodic table on the WWW. สืบค้นเมื่อ 30 December 2020.
- ↑ Allen, Leland C. (1989). "Electronegativity is the average one-electron energy of the valence-shell electrons in ground-state free atoms". Journal of the American Chemical Society. 111 (25): 9003–9014. doi:10.1021/ja00207a003.
- ↑ Tantardini,Christian; Oganov, Artem R. (2021). "Thermochemical Electronegativities of the Elements". Nature Communications. 12 (1): 2087–2095. Bibcode:2021NatCo..12.2087T. doi:10.1038/s41467-021-22429-0. PMC 8027013. PMID 33828104.
- ↑ 27.0 27.1 Wilks, John (1967). "Introduction". The Properties of Liquid and Solid Helium. Oxford: Clarendon Press. ISBN 978-0-19-851245-5.
- ↑ "John Beamish's Research on Solid Helium". Department of Physics, University of Alberta. 2008. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 31 May 2008.
- ↑ Pinceaux, J.-P.; Maury, J.-P.; Besson, J.-M. (1979). "Solidification of helium, at room temperature under high pressure" (PDF). Journal de Physique Lettres. 40 (13): 307–308. doi:10.1051/jphyslet:019790040013030700. S2CID 40164915.
- ↑ Wheeler, John C. (1997). "Electron Affinities of the Alkaline Earth Metals and the Sign Convention for Electron Affinity". Journal of Chemical Education. 74 (1): 123–127. Bibcode:1997JChEd..74..123W. doi:10.1021/ed074p123.; Kalcher, Josef; Sax, Alexander F. (1994). "Gas Phase Stabilities of Small Anions: Theory and Experiment in Cooperation". Chemical Reviews. 94 (8): 2291–2318. doi:10.1021/cr00032a004.
- ↑ Mott, N. F. (1955). "John Edward Lennard-Jones. 1894–1954". Biographical Memoirs of Fellows of the Royal Society. 1: 175–184. doi:10.1098/rsbm.1955.0013.
- ↑ Wiley-VCH (2003). Ullmann's Encyclopedia of Industrial Chemistry – Volume 23. John Wiley & Sons. p. 217.
- ↑ Ozima 2002, p. 35
- ↑ CliffsNotes 2007, p. 15
- ↑ Grochala, Wojciech (1 November 2017). "On the position of helium and neon in the Periodic Table of Elements". Foundations of Chemistry. 20 (2018): 191–207. doi:10.1007/s10698-017-9302-7.
- ↑ Bent Weberg, Libby (18 January 2019). ""The" periodic table". Chemical & Engineering News. 97 (3). เก็บจากแหล่งเดิมเมื่อ 1 February 2020. สืบค้นเมื่อ 27 March 2020.
- ↑ Grandinetti, Felice (23 April 2013). "Neon behind the signs". Nature Chemistry. 5 (2013): 438. Bibcode:2013NatCh...5..438G. doi:10.1038/nchem.1631. PMID 23609097.
- ↑ 38.0 38.1 38.2 38.3 38.4 38.5 38.6 38.7 Grochala, Wojciech (24 สิงหาคม 2007). "Atypical compounds of gases, which have been called noble" (PDF). Chemical Society Reviews. 36 (10): 1632–1655. doi:10.1039/b702109g. PMID 17721587. S2CID 13525010.
- ↑ Pauling, Linus (1933). "The Formulas of Antimonic Acid and the Antimonates". Journal of the American Chemical Society. 55 (5): 1895–1900. doi:10.1021/ja01332a016.
- ↑ Holloway 1968
- ↑ Seppelt, Konrad (1979). "Recent developments in the Chemistry of Some Electronegative Elements". Accounts of Chemical Research. 12 (6): 211–216. doi:10.1021/ar50138a004.
- ↑ Moody, G. J. (1974). "A Decade of Xenon Chemistry". Journal of Chemical Education. 51 (10): 628–630. Bibcode:1974JChEd..51..628M. doi:10.1021/ed051p628. สืบค้นเมื่อ 16 October 2007.
- ↑ Zupan, Marko; Iskra, Jernej; Stavber, Stojan (1998). "Fluorination with XeF2. 44. Effect of Geometry and Heteroatom on the Regioselectivity of Fluorine Introduction into an Aromatic Ring". The Journal of Organic Chemistry. 63 (3): 878–880. doi:10.1021/jo971496e. PMID 11672087.
- ↑ Harding 2002, pp. 90–99
- ↑ .Avrorin, V. V.; Krasikova, R. N.; Nefedov, V. D.; Toropova, M. A. (1982). "The Chemistry of Radon". Russian Chemical Reviews. 51 (1): 12–20. Bibcode:1982RuCRv..51...12A. doi:10.1070/RC1982v051n01ABEH002787. S2CID 250906059.
- ↑ Stein, Lawrence (1983). "The Chemistry of Radon". Radiochimica Acta. 32 (1–3): 163–171. doi:10.1524/ract.1983.32.13.163. S2CID 100225806.
- ↑ Liebman, Joel F. (1975). "Conceptual Problems in Noble Gas and Fluorine Chemistry, II: The Nonexistence of Radon Tetrafluoride". Inorganic and Nuclear Chemistry Letters. 11 (10): 683–685. doi:10.1016/0020-1650(75)80185-1.
- ↑ Seppelt, Konrad (2015). "Molecular Hexafluorides". Chemical Reviews. 115 (2): 1296–1306. doi:10.1021/cr5001783. PMID 25418862.
- ↑ Lehmann, J (2002). "The chemistry of krypton". Coordination Chemistry Reviews. 233–234: 1–39. doi:10.1016/S0010-8545(02)00202-3.
- ↑ Roth, Klaus (2017). "Ist das Element 118 ein Edelgas?" [Is Element 118 a Noble Gas?]. Chemie in unserer Zeit (ภาษาเยอรมัน). 51 (6): 418–426. doi:10.1002/ciuz.201700838.
Translated into English by W. E. Russey and published in three parts in ChemViews Magazine:
Roth, Klaus (3 April 2018). "New Kids on the Table: Is Element 118 a Noble Gas? – Part 1". ChemViews Magazine. doi:10.1002/chemv.201800029.
Roth, Klaus (1 May 2018). "New Kids on the Table: Is Element 118 a Noble Gas? – Part 2". ChemViews Magazine. doi:10.1002/chemv.201800033.
Roth, Klaus (5 June 2018). "New Kids on the Table: Is Element 118 a Noble Gas? – Part 3". ChemViews Magazine. doi:10.1002/chemv.201800046. - ↑ Kulsha, A. V. "Есть ли граница у таблицы Менделеева?" [Is there a boundary to the Mendeleev table?] (PDF). www.primefan.ru (ภาษารัสเซีย). สืบค้นเมื่อ 8 September 2018.
- ↑ Fricke, Burkhard (1975). Superheavy elements: a prediction of their chemical and physical properties. Recent Impact of Physics on Inorganic Chemistry. Structure and Bonding. Vol. 21. pp. 89–144. doi:10.1007/BFb0116498. ISBN 978-3-540-07109-9. สืบค้นเมื่อ 4 October 2013.
- ↑ Russian periodic table poster by A. V. Kulsha and T. A. Kolevich
- ↑ Mewes, Jan-Michael; Smits, Odile Rosette; Jerabek, Paul; Schwerdtfeger, Peter (25 July 2019). "Oganesson is a Semiconductor: On the Relativistic Band‐Gap Narrowing in the Heaviest Noble‐Gas Solids". Angewandte Chemie. 58 (40): 14260–14264. doi:10.1002/anie.201908327. PMC 6790653. PMID 31343819.
- ↑ Kratz, J. V. (2012-08-01). "The impact of the properties of the heaviest elements on the chemical and physical sciences". Radiochimica Acta (ภาษาอังกฤษ). 100 (8–9): 569–578. doi:10.1524/ract.2012.1963. ISSN 2193-3405. S2CID 97915854.
- ↑ "Indication for a volatile element 114" (PDF). doc.rero.ch.
- ↑ Hogness, T. R.; Lunn, E. G. (1925). "The Ionization of Hydrogen by Electron Impact as Interpreted by Positive Ray Analysis". Physical Review. 26 (1): 44–55. Bibcode:1925PhRv...26...44H. doi:10.1103/PhysRev.26.44.
- ↑ Powell, H. M. & Guter, M. (1949). "An Inert Gas Compound". Nature. 164 (4162): 240–241. Bibcode:1949Natur.164..240P. doi:10.1038/164240b0. PMID 18135950. S2CID 4134617.
- ↑ Greenwood 1997, p. 893
- ↑ Dyadin, Yuri A.; และคณะ (1999). "Clathrate hydrates of hydrogen and neon". Mendeleev Communications. 9 (5): 209–210. doi:10.1070/MC1999v009n05ABEH001104.
- ↑ Saunders, M.; Jiménez-Vázquez, H. A.; Cross, R. J.; Poreda, R. J. (1993). "Stable compounds of helium and neon. He@C60 and Ne@C60". Science. 259 (5100): 1428–1430. Bibcode:1993Sci...259.1428S. doi:10.1126/science.259.5100.1428. PMID 17801275. S2CID 41794612.
- ↑ Saunders, Martin; Jimenez-Vazquez, Hugo A.; Cross, R. James; Mroczkowski, Stanley; Gross, Michael L.; Giblin, Daryl E.; Poreda, Robert J. (1994). "Incorporation of helium, neon, argon, krypton, and xenon into fullerenes using high pressure". Journal of the American Chemical Society. 116 (5): 2193–2194. doi:10.1021/ja00084a089.
- ↑ Frunzi, Michael; Cross, R. Jame; Saunders, Martin (2007). "Effect of Xenon on Fullerene Reactions". Journal of the American Chemical Society. 129 (43): 13343–6. doi:10.1021/ja075568n. PMID 17924634.
- ↑ Greenwood 1997, p. 897
- ↑ Weinhold 2005, pp. 275–306
- ↑ Pimentel, G. C. (1951). "The Bonding of Trihalide and Bifluoride Ions by the Molecular Orbital Method". The Journal of Chemical Physics. 19 (4): 446–448. Bibcode:1951JChPh..19..446P. doi:10.1063/1.1748245.
- ↑ Weiss, Achim. "Elements of the past: Big Bang Nucleosynthesis and observation". Max Planck Institute for Gravitational Physics. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 8 February 2007. สืบค้นเมื่อ 23 June 2008.
- ↑ Coc, A.; และคณะ (2004). "Updated Big Bang Nucleosynthesis confronted to WMAP observations and to the Abundance of Light Elements". Astrophysical Journal. 600 (2): 544–552. arXiv:astro-ph/0309480. Bibcode:2004ApJ...600..544C. doi:10.1086/380121. S2CID 16276658.
- ↑ 69.0 69.1 Morrison, P.; Pine, J. (1955). "Radiogenic Origin of the Helium Isotopes in Rock". Annals of the New York Academy of Sciences. 62 (3): 71–92. Bibcode:1955NYASA..62...71M. doi:10.1111/j.1749-6632.1955.tb35366.x. S2CID 85015694.
- ↑ Scherer, Alexandra (16 January 2007). "40Ar/39Ar dating and errors". Technische Universität Bergakademie Freiberg. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 14 October 2007. สืบค้นเมื่อ 26 June 2008.
- ↑ Sanloup, Chrystèle; Schmidt, Burkhard C.; และคณะ (2005). "Retention of Xenon in Quartz and Earth's Missing Xenon". Science. 310 (5751): 1174–1177. Bibcode:2005Sci...310.1174S. doi:10.1126/science.1119070. PMID 16293758. S2CID 31226092.
- ↑ Tyler Irving (May 2011). "Xenon Dioxide May Solve One of Earth's Mysteries". L'Actualité chimique canadienne (Canadian Chemical News). คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 9 February 2013. สืบค้นเมื่อ 18 May 2012.
- ↑ "A Citizen's Guide to Radon". U.S. Environmental Protection Agency. 26 November 2007. สืบค้นเมื่อ 26 June 2008.
- ↑ Lodders, Katharina (10 July 2003). "Solar System Abundances and Condensation Temperatures of the Elements" (PDF). The Astrophysical Journal. The American Astronomical Society. 591 (2): 1220–1247. Bibcode:2003ApJ...591.1220L. doi:10.1086/375492. S2CID 42498829. คลังข้อมูลเก่าเก็บจากแหล่งเดิม (PDF)เมื่อ 7 November 2015. สืบค้นเมื่อ 1 September 2015.
- ↑ "The Atmosphere". National Weather Service. สืบค้นเมื่อ 1 June 2008.
- ↑ 76.0 76.1 76.2 76.3 76.4 76.5 76.6 Häussinger, Peter; Glatthaar, Reinhard; Rhode, Wilhelm; Kick, Helmut; Benkmann, Christian; Weber, Josef; Wunschel, Hans-Jörg; Stenke, Viktor; Leicht, Edith; Stenger, Hermann (2002). "Noble gases". Ullmann's Encyclopedia of Industrial Chemistry. Wiley. doi:10.1002/14356007.a17_485. ISBN 3-527-30673-0.
- ↑ Winter, Mark (2008). "Helium: the essentials". University of Sheffield. สืบค้นเมื่อ 14 July 2008.
- ↑ 78.0 78.1 Hwang, Shuen-Chen; Lein, Robert D.; Morgan, Daniel A. (2005). "Noble Gases". Kirk Othmer Encyclopedia of Chemical Technology. Wiley. pp. 343–383. doi:10.1002/0471238961.0701190508230114.a01.
- ↑ "Neon". Encarta. 2008.
- ↑ Zhang, C. J.; Zhou, X. T.; Yang, L. (1992). "Demountable coaxial gas-cooled current leads for MRI superconducting magnets". IEEE Transactions on Magnetics. IEEE. 28 (1): 957–959. Bibcode:1992ITM....28..957Z. doi:10.1109/20.120038.
- ↑ Fowler, B.; Ackles, K. N.; Porlier, G. (1985). "Effects of inert gas narcosis on behavior—a critical review". Undersea Biomedical Research. 12 (4): 369–402. ISSN 0093-5387. OCLC 2068005. PMID 4082343. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 25 ธันวาคม 2010. สืบค้นเมื่อ 8 เมษายน 2008.
- ↑ Bennett 1998, p. 176
- ↑ Vann, R. D., บ.ก. (1989). "The Physiological Basis of Decompression". 38th Undersea and Hyperbaric Medical Society Workshop. Bethesda, Md.: Undersea and Hyperbaric Medical Society. 75: 437. OCLC 78563877. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 7 ตุลาคม 2008. สืบค้นเมื่อ 31 พฤษภาคม 2008.
- ↑ Maiken, Eric (1 August 2004). "Why Argon?". Decompression. สืบค้นเมื่อ 26 June 2008.
- ↑ Horhoianu, G.; Ionescu, D. V.; Olteanu, G. (1999). "Thermal behaviour of CANDU type fuel rods during steady state and transient operating conditions". Annals of Nuclear Energy. 26 (16): 1437–1445. doi:10.1016/S0306-4549(99)00022-5.
- ↑ "Disaster Ascribed to Gas by Experts". The New York Times. 7 May 1937. p. 1.
- ↑ Freudenrich, Craig (2008). "How Blimps Work". HowStuffWorks. สืบค้นเมื่อ 3 July 2008.
- ↑ Dunkin, I. R. (1980). "The matrix isolation technique and its application to organic chemistry". Chem. Soc. Rev. 9: 1–23. doi:10.1039/CS9800900001.
- ↑ Basting, Dirk; Marowsky, Gerd (2005). Excimer Laser Technology. Springer. ISBN 3-540-20056-8.
- ↑ Sanders, Robert D.; Ma, Daqing; Maze, Mervyn (2005). "Xenon: elemental anaesthesia in clinical practice". British Medical Bulletin. 71 (1): 115–135. doi:10.1093/bmb/ldh034. PMID 15728132.
- ↑ Albert, M. S.; Balamore, D. (1998). "Development of hyperpolarized noble gas MRI". Nuclear Instruments and Methods in Physics Research A. 402 (2–3): 441–453. Bibcode:1998NIMPA.402..441A. doi:10.1016/S0168-9002(97)00888-7. PMID 11543065.
- ↑ Ray, Sidney F. (1999). Scientific photography and applied imaging. Focal Press. pp. 383–384. ISBN 0-240-51323-1.
บรรณานุกรม
| แหล่งข้อมูลห้องสมุดเกี่ยวกับ Noble gas |
- Bennett, Peter B.; Elliott, David H. (1998). The Physiology and Medicine of Diving. SPCK Publishing. ISBN 0-7020-2410-4.
- Bobrow Test Preparation Services (5 December 2007). CliffsAP Chemistry. CliffsNotes. ISBN 978-0-470-13500-6.
- Greenwood, N. N.; Earnshaw, A. (1997). Chemistry of the Elements (2nd ed.). Oxford:Butterworth-Heinemann. ISBN 0-7506-3365-4.
- Harding, Charlie J.; Janes, Rob (2002). Elements of the P Block. Royal Society of Chemistry. ISBN 0-85404-690-9.
- Holloway, John H. (1968). Noble-Gas Chemistry. London: Methuen Publishing. ISBN 0-412-21100-9.
- Mendeleev, D. (1902–1903). Osnovy Khimii (The Principles of Chemistry) (ภาษารัสเซีย) (7th ed.). New York, Collier.
- Ozima, Minoru; Podosek, Frank A. (2002). Noble Gas Geochemistry. Cambridge University Press. ISBN 0-521-80366-7.
- Weinhold, F.; Landis, C. (2005). Valency and bonding. Cambridge University Press. ISBN 0-521-83128-8.




